Circulation | 心梗促癌,补给营养被癌细胞利用
- boke
- 2024-04-16
- 11:04 上午
心力衰竭与癌症都是常见的疾病,临床研究显示,抗癌治疗会加速心衰,而心衰则会增加癌症发病风险,这将恶化患者的预后,并对治疗方案产生负面影响。
心衰和癌症之间的联系是复杂的,现在还不完全清楚。一部分原因是二者具有共同的风险因素,例如吸烟、糖尿病等。最近的研究提出了一个更让人信服的解释:受伤心脏所释放的循环因子会加速肿瘤生长。不过,心衰和癌症之间的联系还没有被完全揭示。
了解心脑血管疾病与癌症之间的联系机制,有助于识别患有癌症风险较高的心血管疾病患者,更早进行风险分层、预防和治疗。
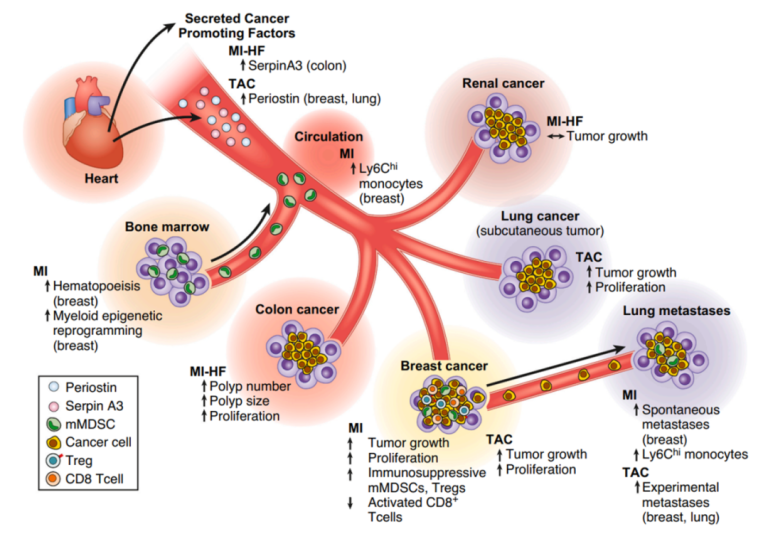
心脑血管疾病对癌症的影响[1]
将心衰和癌症联系起来的一个潜在机制是通过小细胞外囊泡(small extracellular vesicles,sEVs)。sEVs(<200nm)由细胞主动分泌,内含RNA、细胞因子、趋化因子、生长因子等多种生物分子,sEVs比单一信号因子更为强大,是细胞之间传递生物信息的重要手段,它还可以介导心脏和其他器官之间的交流,sEVs在心脏病和癌症等疾病过程中发挥着重要作用。然而,来自衰竭心脏的sEVs能否以及如何促进肿瘤生长尚不清楚。
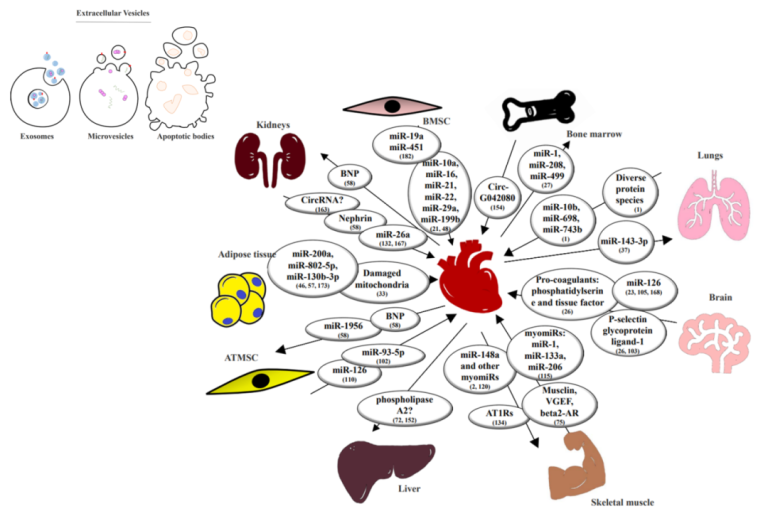
近日,《循环》期刊的一项研究发现[3],心脏sEVs,尤其是在心肌梗死后,心脏间充质基质细胞修复心脏所释放的sEVs(cMSC-sEVs),携带了多种促癌因子。当癌细胞摄取cMSC-sEVs后,会加速肿瘤的生长和转移。
使用螺内酯治疗可以降低cMSC-sEVs水平,并显著抑制心肌梗死对肿瘤的促进作用。该研究结果为心肌梗死与癌症之间的联系机制提供了新的见解,心脏细胞外囊泡可用于心脏病和癌症患者的风险分层和治疗靶点,此外,该研究结果可能也适用于其他心脑血管疾病和癌症之间的联系。

在癌症小鼠模型中,心肌梗死后左心室功能不全(LVD)发生后肿瘤生长加速;检测sEVs显示,LVD小鼠心脏产生的sEVs是对照组的两倍多,并具有促肿瘤特性。
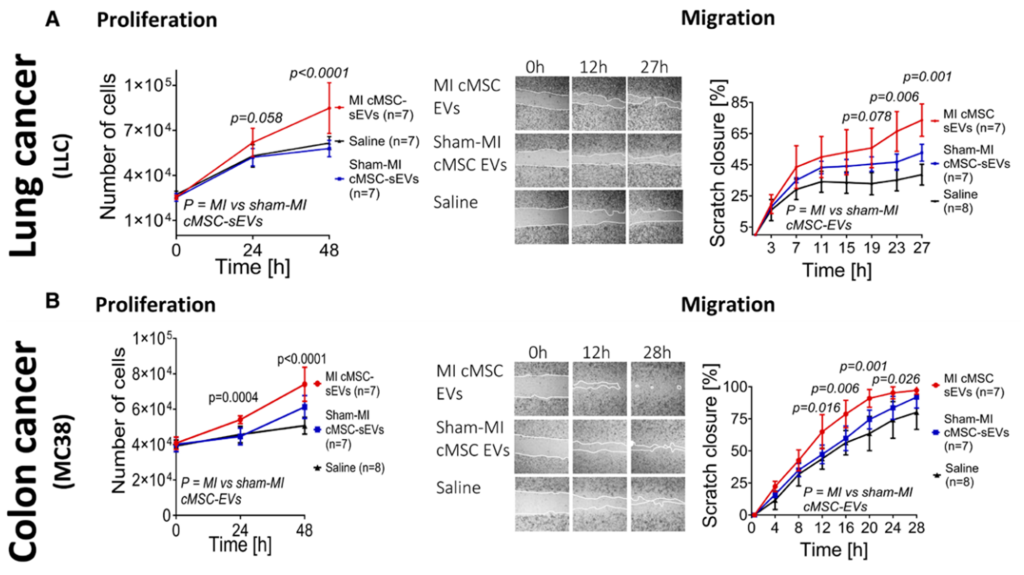
LVD小鼠产生的sEVs能够促进肿瘤增殖和迁移[3]
这些在心肌梗死后有心脏产生的大量促肿瘤sEVs,来自心脏组织损伤、修复期间被激活的心脏间充质基质细胞(MSCs),本是修复心脏的营养,可能“好心办了坏事”。
使用螺内酯治疗,在没有发生心肌梗死的小鼠中使用螺内酯治疗并不能抑制其肿瘤增殖,说明螺内酯本身并不具有抗肿瘤特性;而在心肌梗死小鼠中,螺内酯可以使cMSC-sEVs水平减少28%,肿瘤生长得到了明显被抑制。
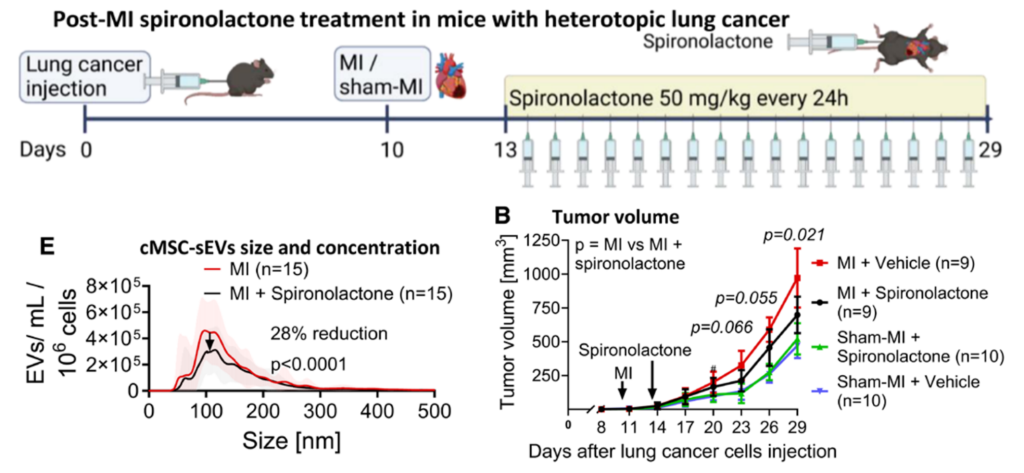
螺内酯治疗降低cMSC-sEVs水平并抑制肿瘤生长[3]
参考资料
1. Koelwyn G J, Aboumsallem J P, Moore K J, et al. Reverse cardio-oncology: Exploring the effects of cardiovascular disease on cancer pathogenesis[J]. Journal of molecular and cellular cardiology, 2022, 163: 1-8.
2. Gabisonia K, Khan M, Recchia F A. Extracellular vesicle-mediated bidirectional communication between heart and other organs[J]. American Journal of Physiology-Heart and Circulatory Physiology, 2022, 322(5): H769-H784.
3. Caller T, Rotem I, Shaihov-Teper O, et al. Small Extracellular Vesicles From Infarcted and Failing Heart Accelerate Tumor Growth[J]. Circulation, 2024.


