NCCN 2025.V2.0 | 黑色素瘤的精准诊断与治疗
- boke
- 2026-05-12
- 9:39 上午
皮肤黑色素瘤
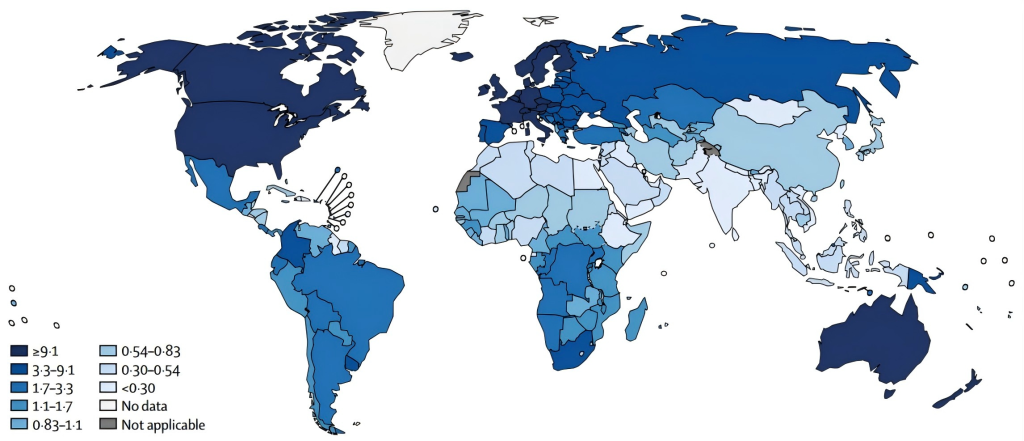
风险因素包括:
(1)遗传易感性:存在易患黑色素瘤的种系突变或多态性(如CDKN2a、CDK4、MC1R、TERT、MITF、PTEN)以及其他增加黑色素瘤风险的癌症易感基因(如CHEK2、BRCA1/2、BLM、ATM);有2个或以上侵袭性皮肤黑色素瘤或非皮肤癌(尤其是胰腺癌、肾癌、膀胱癌、消化道癌和/或乳腺癌)家族史或个人史。
(2)表型易感性:非典型痣/发育不良痣、痣的数量增多(尤其是大的痣)、日光性表型/易晒伤倾向。
(3)个人病史:多次和/或导致水疱的晒伤、癌前病变/癌症、免疫抑制与器官移植、罕见基因突变(着色性干皮症)。
(4)环境因素:长期或频繁暴露于强烈紫外线(如户外工作、日光浴、晒黑床使用),增加黑色素细胞突变风险。
一、皮肤黑色素瘤的诊断
1
病理诊断
病理活检是黑色素瘤诊断的“金标准”,若初始活检不足以明确诊断或进行微分期,需进行重复活检。病理评估中,关注以下指标:Breslow厚度、是否伴有溃疡、真皮有丝分裂率、评估深部和外周缘状态、神经浸润情况、微卫星灶。
1
临床分期与辅助检查
(1)基线检查:对于IB期及以上或有高危因素的患者,需进行基线影像学检查(胸部/腹部/盆腔CT或FDG-PET/CT)和实验室检查。
(2)前哨淋巴结活检(SLNB):根据是否存在亚临床淋巴结转移,对临床I-II期黑色素瘤患者进行进一步的风险分层。
二、皮肤黑色素瘤的治疗
1
手术治疗
手术是黑色素瘤治疗的基础,核心目标是彻底切除肿瘤,降低复发风险。主要包括:原发肿瘤广泛切除、前哨淋巴结活检(SLNB)、完全淋巴结清扫(CLND)。
2
放疗
放疗在黑色素瘤治疗中主要用于辅助治疗和姑息治疗:
辅助放疗:对于局部复发风险高的患者,如肿瘤厚度较大(如T4b,后续手术切除难度大)、促结缔组织增生性组织学特征、多灶性/广泛神经浸润、切缘阳性、存在微卫星灶等,可考虑对原发肿瘤切除部位进行放疗。
姑息放疗:用于缓解晚期黑色素瘤患者的症状,如骨转移引起的疼痛、脑转移引起的神经症状等,以提高患者生活质量。
3
全身治疗
全身治疗主要用于晚期(不可切除或转移性)黑色素瘤,以及高危可切除患者的辅助治疗,包括免疫治疗、靶向治疗、细胞毒性治疗等。
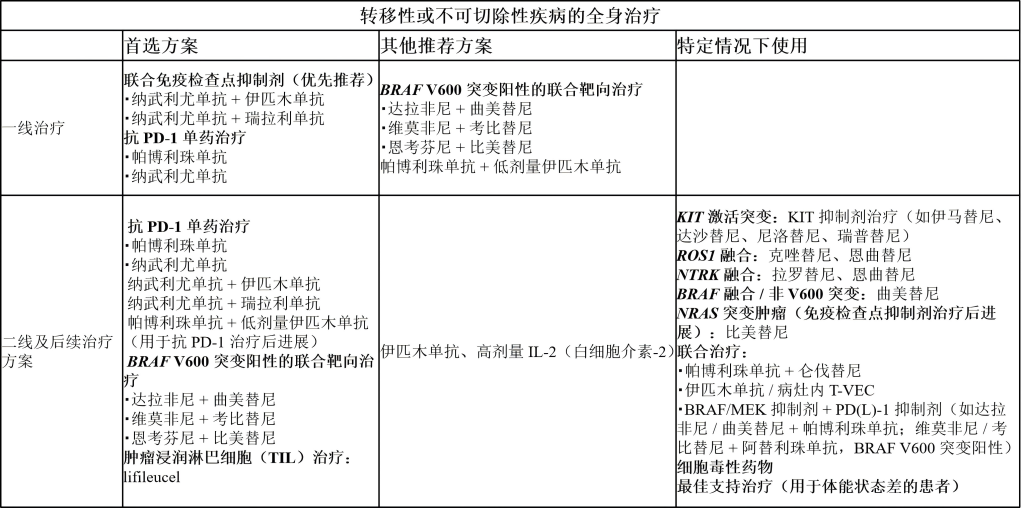
三、皮肤黑色素瘤的分子检测
皮肤黑色素瘤的分子检测,是诊断、预后评估、前哨淋巴结活检(SLNB)风险预测及靶向/免疫治疗决策的核心工具。目前已发现多种体细胞基因改变,其中少数为可靶向驱动突变,已被证实可用于指导治疗决策和/或临床试验入组。
1
核心驱动基因突变
(1)BRAF 突变
检测方式:IHC(初筛)、PCR、NGS
检测意义:BRAF突变最常见于V600,其中V600E最为常见(80%),此外还有V600K(15%)及V600R/M/D/G(5%)。BRAF V600突变与对BRAF抑制剂和MEK抑制剂的敏感性相关;在携带BRAF V600突变的患者中,BRAF与MEK抑制剂联合治疗优于单药治疗。
(2)KIT 突变
检测方式:NGS
检测意义:KIT 突变可出现在基因的多个“热点”区域,其对KIT抑制剂(如伊马替尼、舒尼替尼、尼洛替尼)的敏感性不同。KIT第11号外显子和第13号外显子突变(如W557R、V559D、L576P、K642E)似乎对KIT抑制剂高度敏感;KIT第17号外显子突变(如D816H)和KIT基因扩增患者对KIT抑制剂几乎不敏感或完全不敏感。
(3)NRAS 突变
检测方式:PCR、NGS
检测意义:NRAS突变存在于约15%的慢性日晒和间歇性日晒皮肤、肢端及黏膜来源的黑色素瘤中。NRAS 突变似乎与局限期和晚期黑色素瘤的较差生存率相关;MEK抑制剂可能在少数携带NRAS突变的患者中产生反应。
2
其他不常见遗传驱动因素
(1)NTRK1、NTRK2、NTRK3基因融合
检测方式:NGS
检测意义:在各亚型黑色素瘤中发生率<1%,可使用拉罗替尼或恩曲替尼治疗。
(2)ALK、ROS1基因融合
检测方式:NGS
检测意义:在黑色素瘤各亚型中发生率<1%,ROS1融合可使用克唑替尼或恩曲替尼,ALK融合可使用克唑替尼。
(3)BRAF融合
检测方式:NGS
检测意义:可使用曲美替尼治疗
3
免疫治疗相关标志物
(1)PD-L1(程序性死亡配体 1)
检测方式:IHC
检测意义:PD-L1的IHC检测可辅助预测患者对免疫检查点抑制剂的应答。
(2)肿瘤突变负荷(TMB)
检测方式:WES(金标准)
检测意义:与黑色素瘤及其他肿瘤患者对免疫检查点抑制剂应答相关,突变负荷越高,产生的新抗原越多,越易激活抗肿瘤免疫反应。

皮肤黑色素瘤
葡萄膜黑色素瘤是成人中最常见的原发性眼内恶性肿瘤,可发生于葡萄膜的任何部位,其中90%发生于脉络膜,其余发生于虹膜或睫状体[4]。
风险因素包括:
(1)遗传因素:家庭成员患有葡萄膜黑色素瘤被认为是黑色素瘤的危险因素;某些BAP1胚系突变已被证明与葡萄膜黑色素瘤的易感性相关。
(2)眼部因素:约8%的葡萄膜黑色素瘤患者源于已记录的脉络膜痣,痣的增大或形态变化可能提示恶性转化风险;眼/眼皮肤黑变病(导致巩膜外层、葡萄膜和皮肤色素沉着过度)在葡萄膜黑色素瘤患者中的发生率远高于一般人群。
(3)其他因素:较浅的肤色和眼睛颜色以及易晒伤体质、焊接等职业暴露被证明与葡萄膜黑色素瘤风险增加相关。
一、葡萄膜黑色素瘤的诊断
1
全面眼部检查
包括病史采集(个人及家族癌症史)、视力检测、散瞳眼底检查、裂隙灯生物显微镜检查等。
2
辅助成像检查
在某些情况下,可能需要额外的影像学检查来确认诊断或更好地表征肿瘤以进行治疗计划(或监测),包括彩色眼底照相、眼部超声、眼眼底自发荧光、光学相干断层扫描、眼底视网膜荧光血管造影、透照法以及根据临床指征选择使用或不使用静脉对比剂的MRI。
3
活检与病理检查
多数情况下,通过上述检查即可确诊,无需活检。但对于诊断不确定的病例,或需要进行预后分层、参与临床试验时,可考虑活检。
二、葡萄膜黑色素瘤的治疗
1
局部治疗:针对局限性肿瘤
对于未发生转移的局限性葡萄膜黑色素瘤,局部治疗是首选,目的是彻底清除肿瘤,尽可能保留患眼视力。治疗方式包括放射治疗(近距离治疗、粒子束放疗)与手术治疗(眼球摘除术),瞳孔温热疗法、冷冻治疗等消融技术常作为放疗或手术的辅助手段。
2
全身治疗:针对转移性或不可切除肿瘤
葡萄膜黑色素瘤最常见的转移部位是肝脏,其次是肺、皮肤/软组织、骨骼等。一旦发生转移,全身治疗成为主要手段,目的是控制肿瘤进展、缓解症状、延长生存期。

三、葡萄膜黑色素瘤的分子检测
皮肤、葡萄膜和结膜黑色素瘤的分子特征也不同。BRAF、NRAS、KIT 和TERT 启动子突变在葡萄膜黑色素瘤中极为罕见,但在结膜和皮肤黑色素瘤中更常见。在葡萄膜黑色素瘤中常见且具有预后意义的分子标志物(如染色体异常,特别是3号和8号染色体,以及GNAQ或GNA11突变(>80%的葡萄膜黑色素瘤)、BAP1、SF3B1和EIF1AX)在结膜或皮肤黑色素瘤中通常不常见[2][5][6]。
(1)GNAQ/GNA11突变
检测方式:Sanger测序、NGS
检测意义:约85%的葡萄膜黑色素瘤存在GNAQ或GNA11基因突变,是肿瘤发生的关键驱动因素,有助于确诊和分子分型。
(2)BAP1突变
检测方式:HC、NGS、PCR
检测意义:BAP1突变或缺失与肿瘤侵袭性、转移风险及预后不良密切相关,是重要的预后标志物。
(3)SF3B1突变
检测方式:NGS、PCR
检测意义:SF3B1突变与迟发转移相关,有助于评估肿瘤的远期风险。
(4)EIF1AX基因检测
检测方式:NGS、PCR
检测意义:EIF1AX突变通常提示较好预后,与肿瘤的生物学行为和治疗反应相关。
(5)染色体3和8q拷贝数检测
检测方式:荧光原位杂交(FISH)、NGS或微卫星分析(MSA)
意义:染色体3缺失和8q扩增是葡萄膜黑色素瘤的常见遗传特征,与肿瘤的侵袭性和预后密切相关。
(6)DNA甲基化检测
检测方式:甲基化特异性PCR(MSP)、甲基化免疫共沉淀(MeDIP)、全基因组甲基化测序
意义:DNA甲基化谱可辅助肿瘤分类和预后评估,帮助区分不同分子亚型。
黑色素瘤的治疗已进入精准医疗时代,早期识别病变特征、规范手术及分子分型指导下的系统性治疗是改善其预后的核心。分子检测在黑色素瘤的诊疗中不仅能帮助了解其发病机制及生物学特点,还能有效地指导治疗方案选择,预测患者预后和复发风险,从而提高精准诊疗的成功率。基于目前的研究结果,由多学科专家针对黑色素瘤的分子检测及其诊疗应用进行讨论后制定下述支持证据强度高的10条共识[6]。
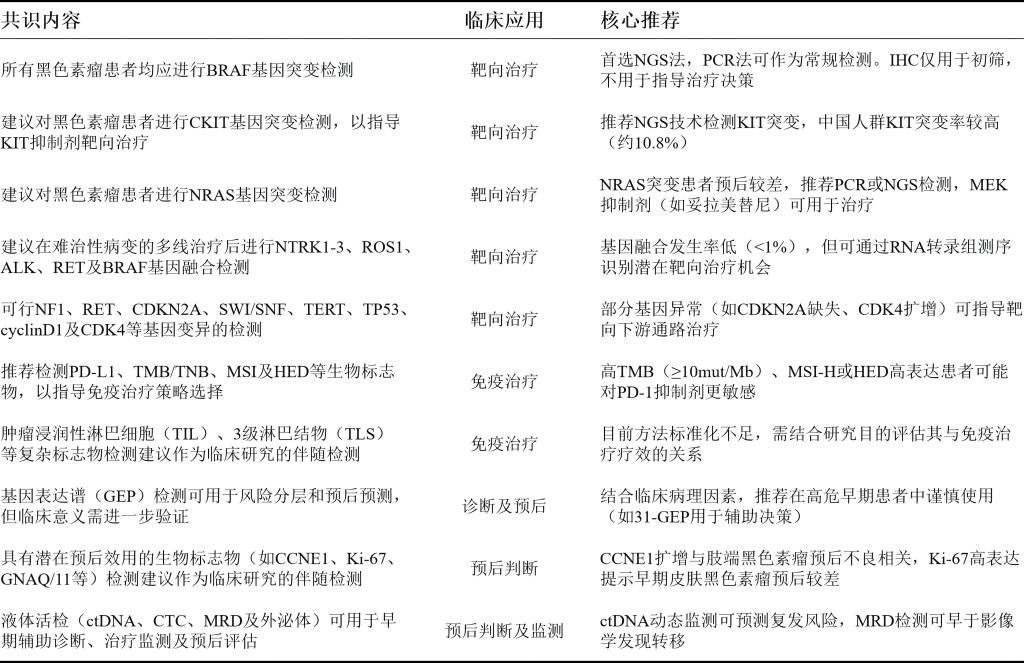
伯科生物在国内已经建设了全流程国产化的高通量核酸合成与应用技术转化中心,建立了GMP厂房和ISO9001、ISO13485质量体系。已经为国内外数百家知名医院、科学研究机构、临床检验所开发了上千款Gene Panel(液相基因芯片),并配套完整的检测试剂,各项性能参数均与国际竞品相当或优于(详见附表1),在基因组、转录组、甲基化组及病原体的检测应用方向均有成熟的产品管线。
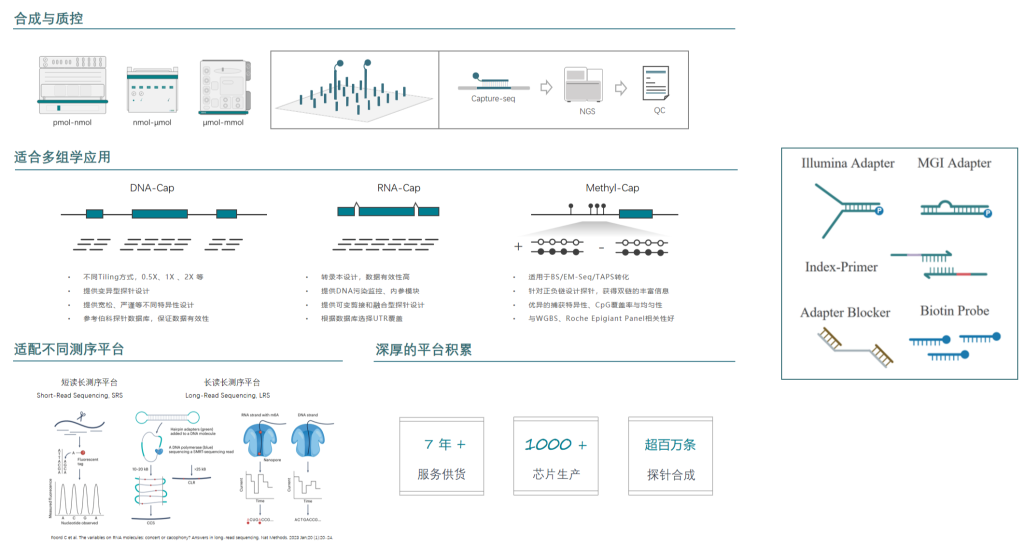
附表1: 产品简介
TargetCap® WES Onco Panel
在肿瘤临床研究与转化的检测应用中,WES(全外显子组测序)通过捕获和测序基因组中所有蛋白质编码区域(约占总基因组的1-2%),高效识别肿瘤样本中的体细胞突变、拷贝数变异及关键驱动基因。它与正常对照样本比较,能够精准筛选出与肿瘤发生、进展及耐药性相关的功能性变异,为揭示不同癌种的基因突变谱、发现潜在治疗靶点以及评估遗传易感性提供核心数据支撑。因此,WES是肿瘤基因组学研究和临床转化应用中的基础工具。
伯科设计的TargetCap® WES Onco Panel目标区域和捕获区域大小分别约为40 Mb和50M+,覆盖基因数量超20000个,其中数百个肿瘤重要相关基因编码区进一步得到覆盖增强,还包含34个融合基因的非编码区(融合基因),能够准确检出SNV、InDel等多种突变类型,实现肿瘤基因组变异的全面解析。
性能表现
采用肿瘤gDNA和血液gDNA样本,使用伯科TargetCap® WES Onco Panel进行杂交捕获,在捕获性能方面,伯科TargetCap® WES Onco Panel表现优异,整体Panel测序深度为500x时,肿瘤相关基因测序深度达到778x,0.2 × Mean占比均在99%左右,Fold 80为1.5-1.6之间。
整体区域QC
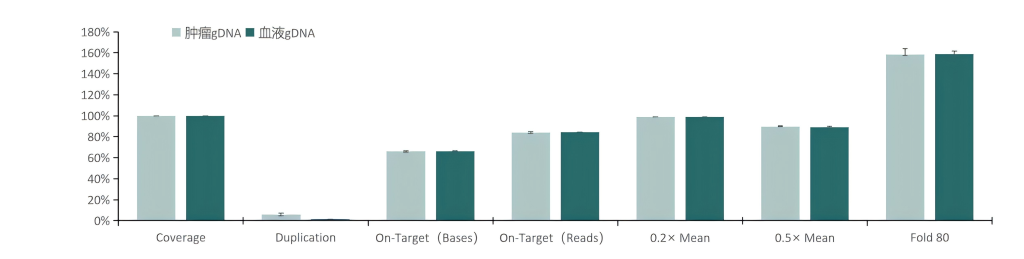
Onco区域QC
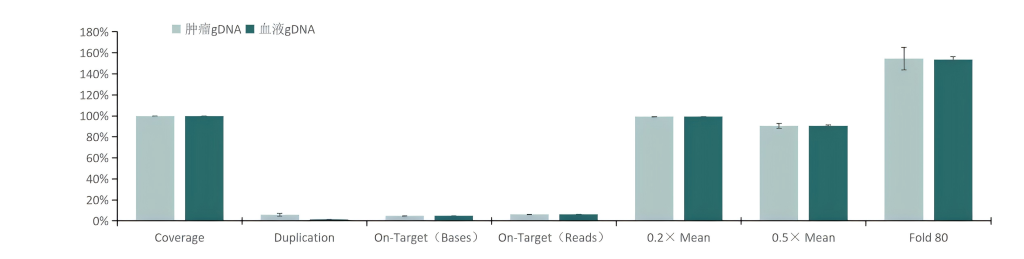
肿瘤液相基因芯片
伯科设计的TargetCap® OncoGene Plus Research Panel基于美国食品药品监督管理局(FDA)批准的用于肿瘤基因检测的FoundationOne CDxTM与MSK-IMPACTTM,其覆盖702个肿瘤相关基因编码区和34个基因的非编码区(融合基因),含有6个MSI和53个化药相关位点,探针覆盖2.32Mb区间。这些区域涵盖更多基因,检测范围更泛,涉及肿瘤高频突变、肿瘤易感、药物靶向、药物耐受等多种类型基因。
性能表现
竞品评测
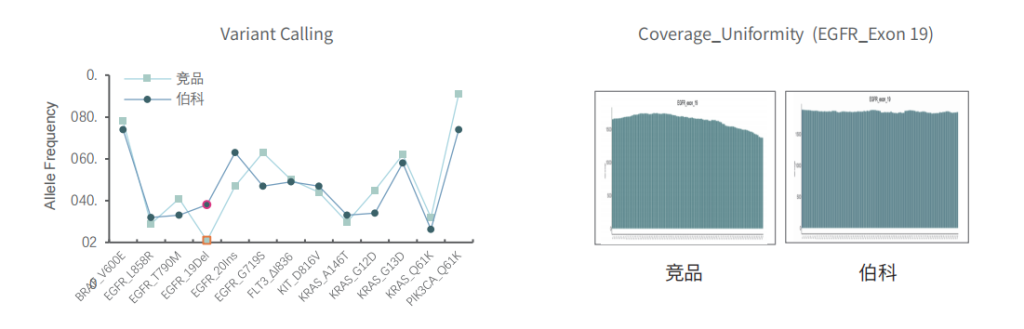
采用gDNA/cfDNA/FFPE/泛肿瘤800gDNA标准品文库,分别使用伯科商品化肿瘤大Panel-OncoGene Plus Research Panel与竞品肿瘤大Panel进行性能比较(二者大小相近),在捕获特异性上(On-Target)和覆盖均一性(0.2XMean)上,伯科均优于竞品。
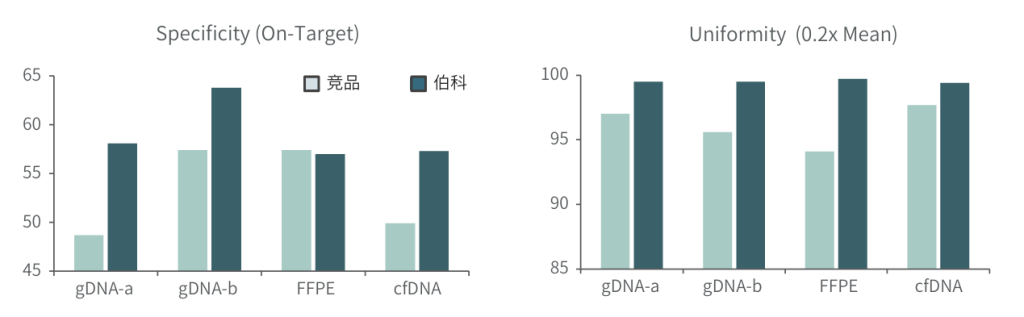
对于gDNA标准品,竞品测序35.9Gb,伯科测序19.6Gb,虽然伯科测序数据少,深度低,但二者的突变频率检出无明显差异,伯科对EGFR的19号外显子缺失变异的检出优于竞品。
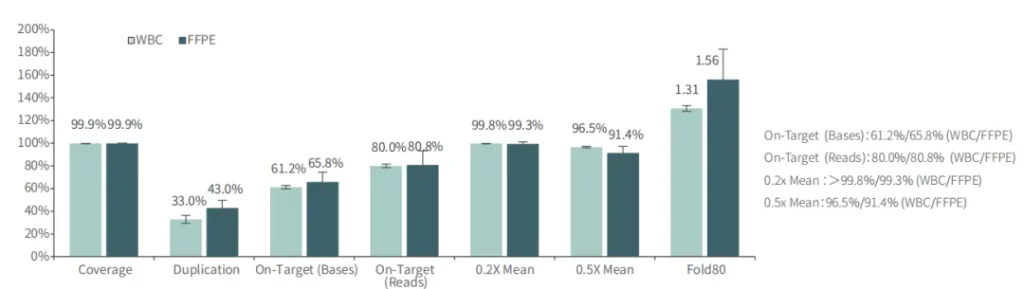
不同样本类型表现
对不同质量的gDNA样本 (WBC/FFPE, >150例),TargetCap® OncoGene Plus Research Panel表现稳定。
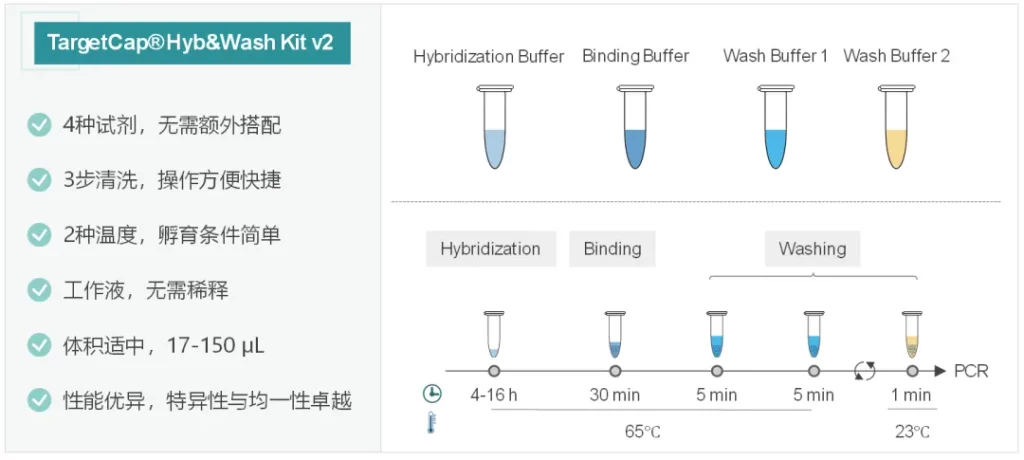
杂交与清洗试剂盒v2 简介
试剂盒概述
伯科杂交与清洗试剂盒v2 (TargetCap® Hybridization and Wash Kit v2,下文简称Hyb&Wash Kit v2)简化了试剂组分和操作流程,同时仍保持优异的捕获性能。Hyb&Wash Kit v2包含4种缓冲液组分,仅需3步清洗,操作流程更加便捷。
性能表现介绍
Ⅰ. 基本QC表现
使用NA12878和NA24694 gDNA标准品,采用三款不同大小的Gene Panel (650Kb、2.3Mb和42Mb) 对Hyb&Wash Kit v2 和 v1 进行比较测试。
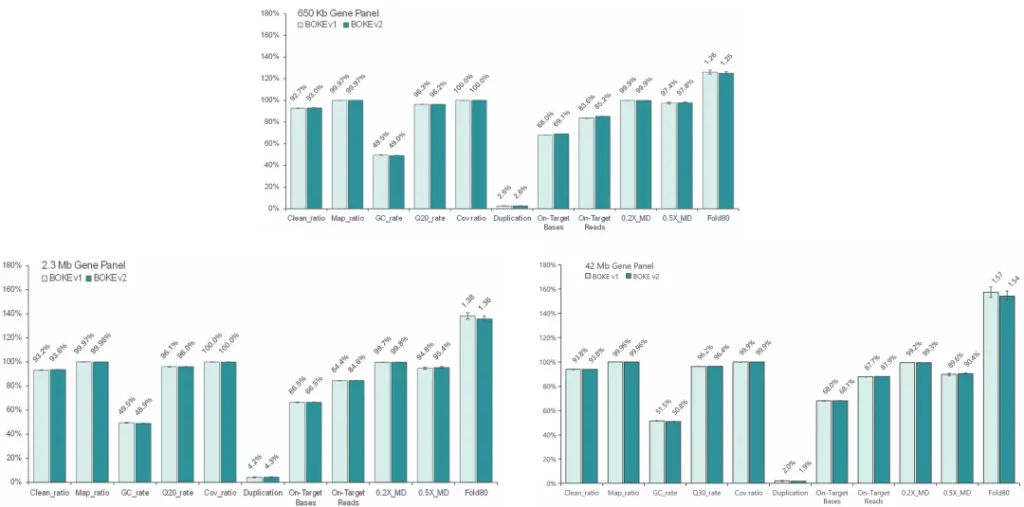
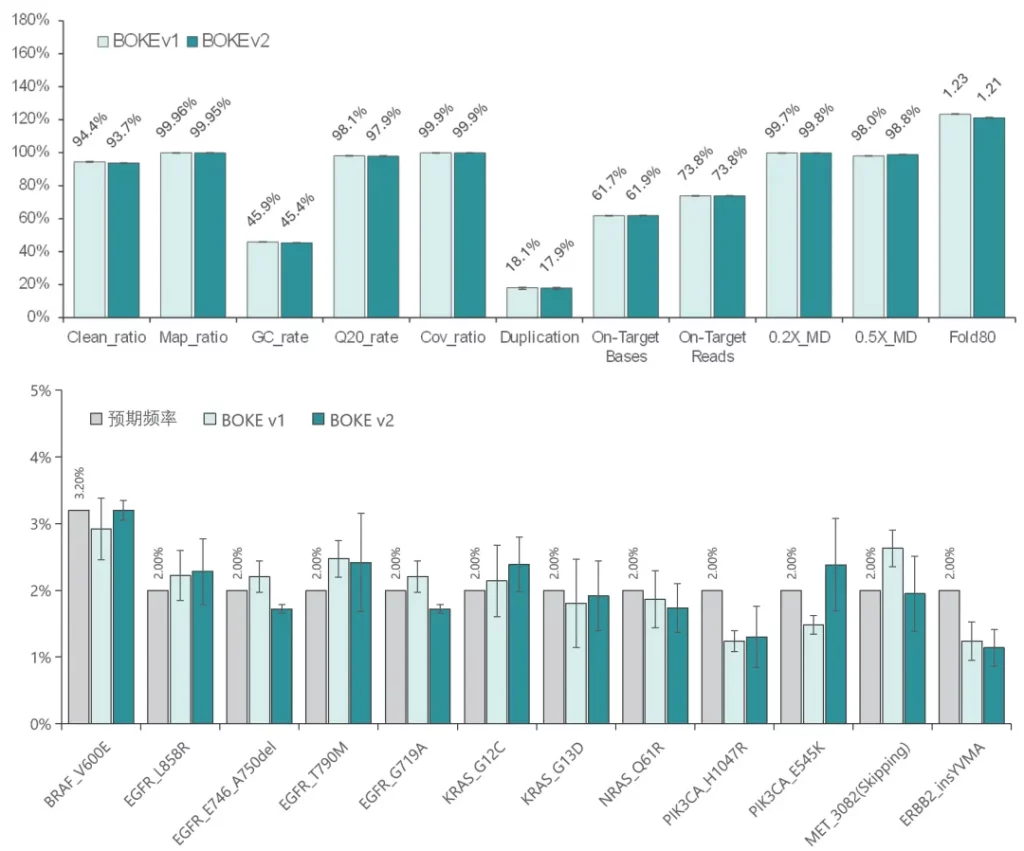
结果显示,在不同大小的Gene Panel中,对于杂交与清洗试剂盒的关键参数-中靶率和均一性,v2与v1试剂盒表现相当,v2试剂盒表现更好的均一性(0.2X_MD、0.5X_MD和Fold80)。
Clean_ratio、Map_ratio等基本参数两款试剂盒表现一致,由于v2试剂盒对低GC目标区域覆盖更佳,其GC_rate率略低于v1。
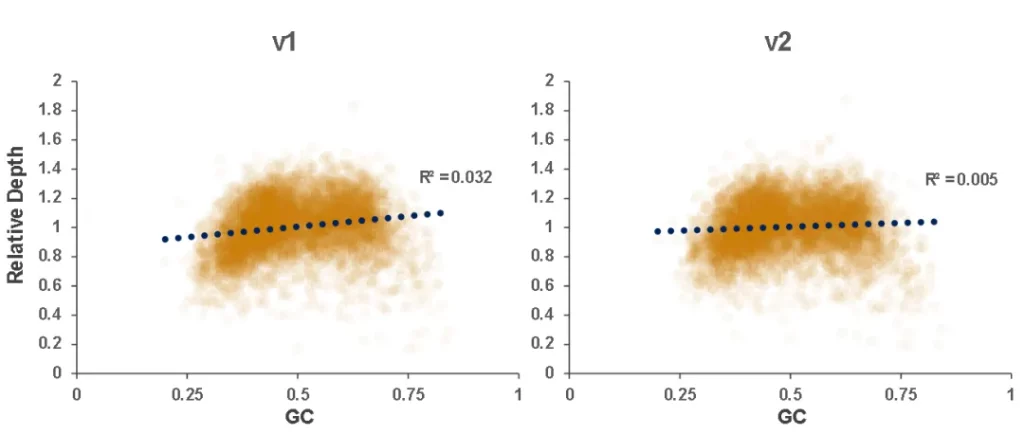
Ⅱ. 低频变异检测
使用肿瘤 SNV gDNA 标准品Ⅱ (GW-OGTM006) 对Hyb&Wash Kit v2的低频变异检测性能进行验证。GW-OGTM006 DNA标准品包含 EGFR、KRAS、NRAS、BRAF、PIK3CA、FGFR3、Her2、MET 等多个常见伴随诊断基因及位点,包含点突变、插入和缺失等多种变异类型。
采用300 Kb Gene Panel对该标准品进行捕获,捕获数据显示,v1与v2试剂盒的基本捕获性能表现相当,v2的中靶率与均一性略优于v1。同时,v1与v2试剂盒均能对12个已知变异准确检出。
参考文献:
1.NCCN Clinical Practice Guidelines in Melanoma: Cutaneous. (2025 Version 2).
2.NCCN Clinical Practice Guidelines in Melanoma: Uveal. (2025 Version 2).
3.Schadendorf D, Van Akkooi A C J, Berking C, et al. Melanoma[J]. The Lancet, 2018, 392(10151): 971-984.
4.中国葡萄膜黑色素瘤诊疗专家共识(2021年)[J].中华眼科杂志,2021,57(12):886-897.
5.Gentien D, Saberi-Ansari E, Servant N, et al. Multi-omics comparison of malignant and normal uveal melanocytes reveals molecular features of uveal melanoma[J]. Cell reports, 2023, 42(9).
6.黑色素瘤分子检测及其诊疗应用的专家共识(2025版)[J].中国肿瘤临床,2025,52(20):1027-1034.


