伯科CHIP Gene Panel助力冠心病经皮冠状动脉介入治疗(PCI)预后风险分层研究
- boke
- 2026-04-17
- 2:11 下午
研究背景
冠状动脉疾病(CAD)全球每年约900万人死亡,经皮冠状动脉介入治疗(PCI)后患者即使接受最佳药物治疗仍有显著的残余风险。潜能不明克隆性造血(CHIP)是白血病相关基因(主要是DNMT3A和TET2)体细胞突变驱动的造血干细胞克隆扩增,与动脉粥样硬化发生相关。CHIP通过IL-6、IL-1β、NLRP3等炎症通路相关因子增加心血管风险,但这些机制性的生物标志物在临床上不常规检测,限制了它们的转化应用。而超敏C反应蛋白(hsCRP)、血常规衍生炎症指数在临床中广泛用于评估全身性和慢性低度炎症[1]。
临床常规可获得的炎症指标(hsCRP、血常规衍生指数)能否改变CHIP对PCI患者的预后风险?
研究设计
研究队列:阜外医院2013年1-12月PCI患者,3642人入组,最终3640人。所有患者接受至少1年双联抗血小板治疗(阿司匹林+替格瑞洛或氯吡格雷)。
验证队列:UK Biobank中3715例PCI患者。
随访:5年,中位随访5.06年。
研究方法
CHIP检测:利用伯科生物设计合成的液相基因芯片(Gene Panel)进行靶向高深度测序,检测37个白血病相关基因驱动的CHIP突变,平均测序深度985×可检测VAF>0.5%的体细胞变异。使用变异等位基因分数(VAF)>0.5%作为CHIP检测的阈值,VAF<2%的突变被定义为小克隆。对于每个参与者,使用VAF最高的突变进行分析。
炎症指标(12个):hsCRP、细胞(WBC)、中性粒细胞(NEU)、单核细胞(MONO)、淋巴细胞(LY)、血小板(PLT)、中性粒细胞-淋巴细胞比率(NLR)、单核细胞-淋巴细胞比率(MLR)、血小板-淋巴细胞比率(PLR)、全身免疫炎症指数(SII)、全身炎症反应指数(SIRI)、全身性炎症总指数(AISI)。
统计方法:Cox比例风险模型、多变量校正模型、交互作用检验(乘积项)、多重插补处理缺失值(mice包)、FDR校正多重比较、C-index、NRI、IDI评估增量预测价值、年龄匹配亚组做敏感性分析。
主要结果
1
CHIP发生率与特征
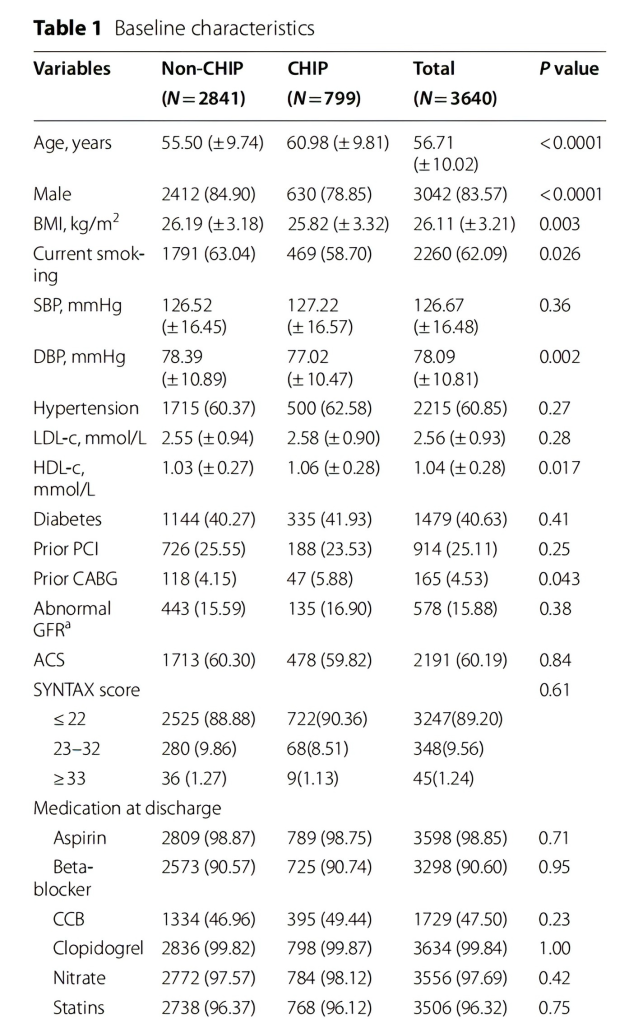
研究发现,799名(22.95%)个体中识别出1271个CHIP驱动基因突变,其中617名(77.22%)仅携带一个突变。最常发生突变的基因为DNMT3A和TET2(共560人,15.4%)。在不同亚型中观察到CHIP患病率随年龄增长而上升(图1)。与非CHIP携带者相比,CHIP患者年龄更大,男性比例更低(表1)。
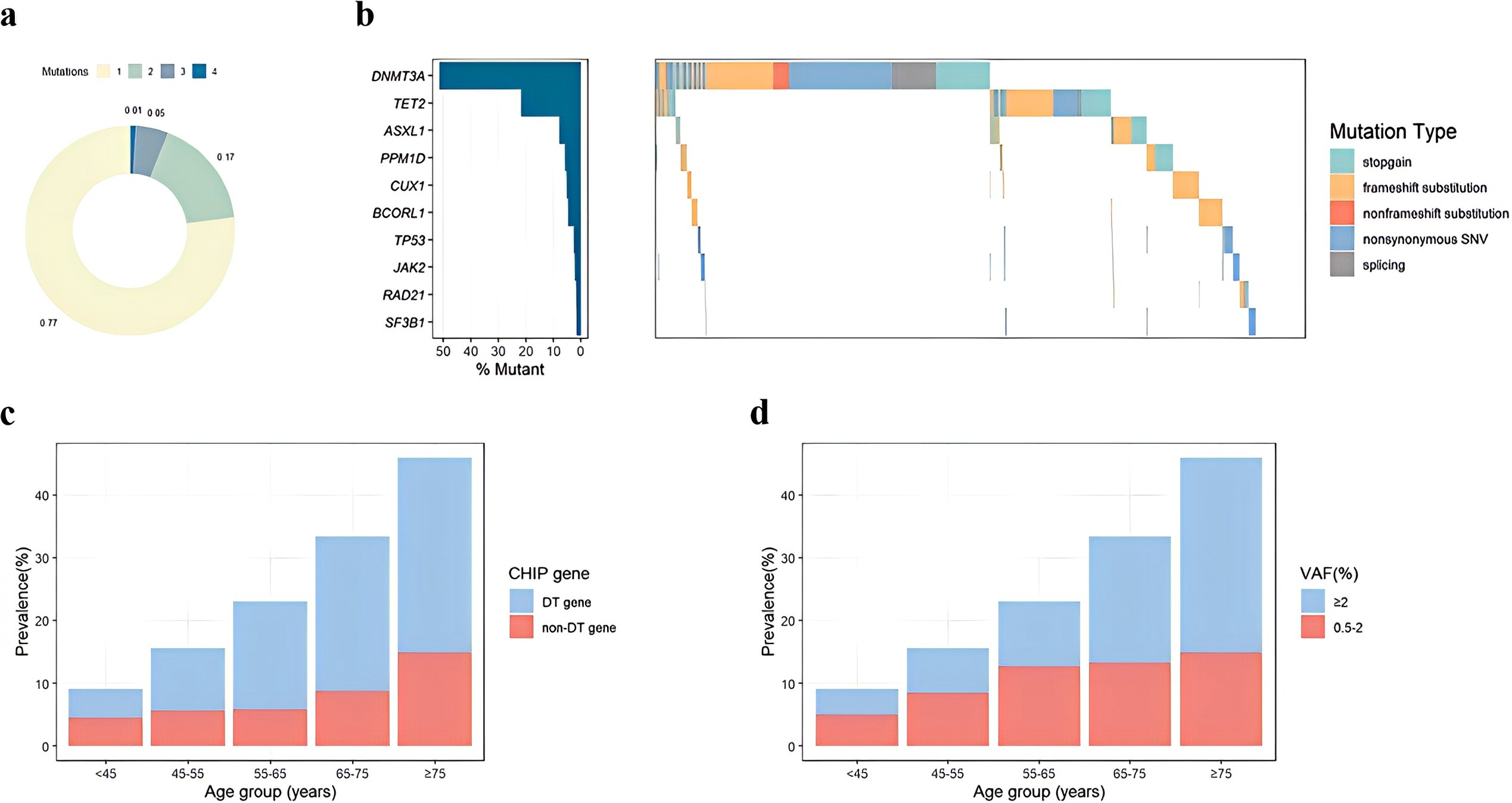
图1 PCI患者的CHIP谱。a每例患者的突变数。b驱动基因和突变类型的分布。c不同年龄组中DT(DNMT3A/TET2)和其他非DT基因的突变分布。d VAF组中突变基因的分布(0.5-2.0%和≥2.0%)。
2
CHIP与血液学和炎症参数的关联
在校正年龄、性别和BMI后,CHIP与血小板相关参数(包括血小板体积分布宽度、血小板体积和血小板比率)水平升高显著相关。炎症标志物水平在CHIP携带者中总体偏高但多数未达到统计学显著(图S4)。
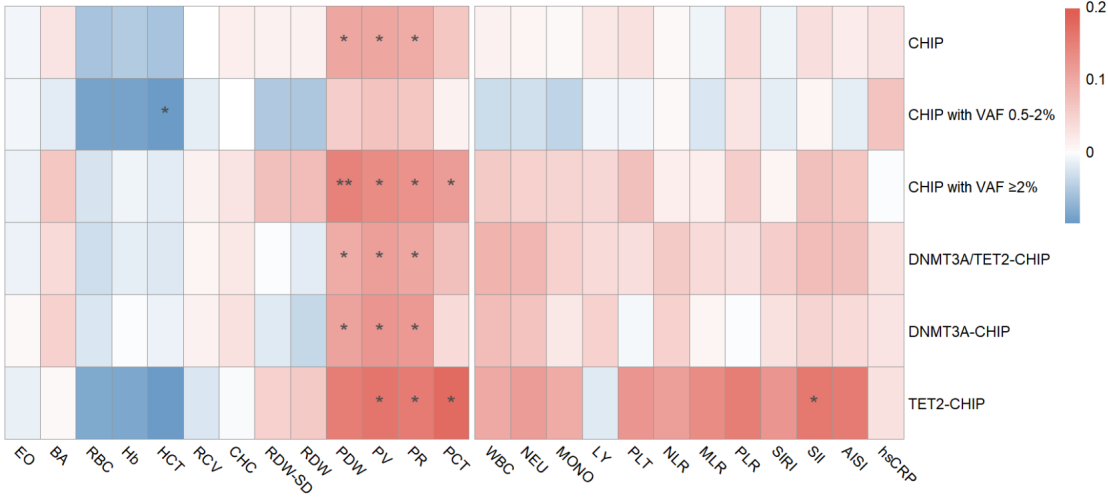
图 S4. CHIP 与血液细胞及炎症参数之间关联的贝塔系数热图。
3
CHIP与预后之间的关联
在校正多个协变量后,CHIP携带者表现出更高的5年全因死亡率(HR, 1.76; 95% CI, 1.20–2.57; P=0.004)和心源性死亡率(HR, 2.19; 95% CI, 1.31–3.65; P=0.003)风险。
携带VAF ≥ 2%的CHIP突变的个体显示出2至3倍的5年全因死亡率(HR, 2.13; 95% CI, 1.37–3.31; P<0.001)和心源性死亡率(HR, 2.99; 95% CI, 1.67–5.33; P<0.001)风险。
在基因特异性分析中发现,与非DT(DNMT3A / TET2突变) CHIP患者相比,DT CHIP患者的死亡率风险更高(图2)。
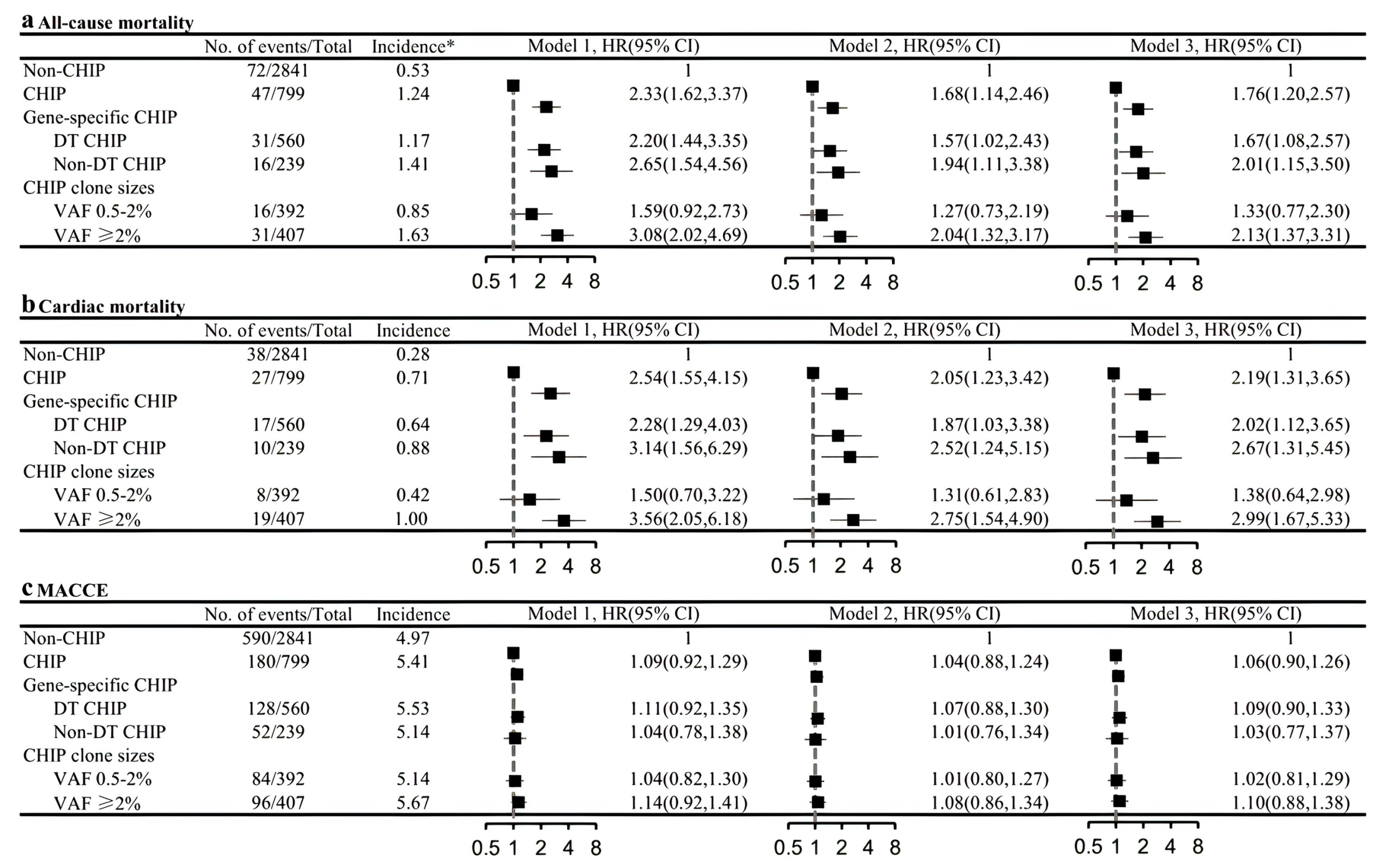
图2 CHIP及其亚型与5年预后的相关性。三个图显示了CHIP及其亚型与5年预后的相关性,包括全因死亡率(a)、心源性死亡率(b)和MACCE(c)。模型1未校正;模型2校正了年龄、性别和体重指数;模型3进一步校正了吸烟、高血压、糖尿病、低密度脂蛋白胆固醇、异常肾小球滤过率、既往经皮冠状动脉介入治疗或冠状动脉旁路移植术、急性冠状动脉综合征和SYNTAX评分。
4
炎症的修饰效应
在校正协变量和多重比较后,对于5年全因死亡率,观察到AISI、MLR、SII和SIRI存在显著的CHIP-炎症交互作用(图3)。
文章进一步研究了在不同全身性炎症水平下CHIP的影响,发现在炎症水平升高的情况下,尤其是在高水平SII下,CHIP相关的5年全因死亡风险显著增加(HR, 3.36; 95% CI, 1.94–5.82; P<0.001),而在低水平SII的患者中未观察到显著关联(HR, 0.92; 95% CI, 0.52–1.66; P=0.793;图4)。此外,小克隆CHIP与5年全因死亡率之间无显著关联,但在高水平全身性炎症的情况下(特别是在高水平SII),携带小克隆的个体也表现出死亡风险增加。
研究还发现CHIP与两种全身性炎症指标(SII和SIRI)对5年MACCE存在显著的交互作用,CHIP与高水平SII或SIRI的组合与5年MACCE的显著风险相关。
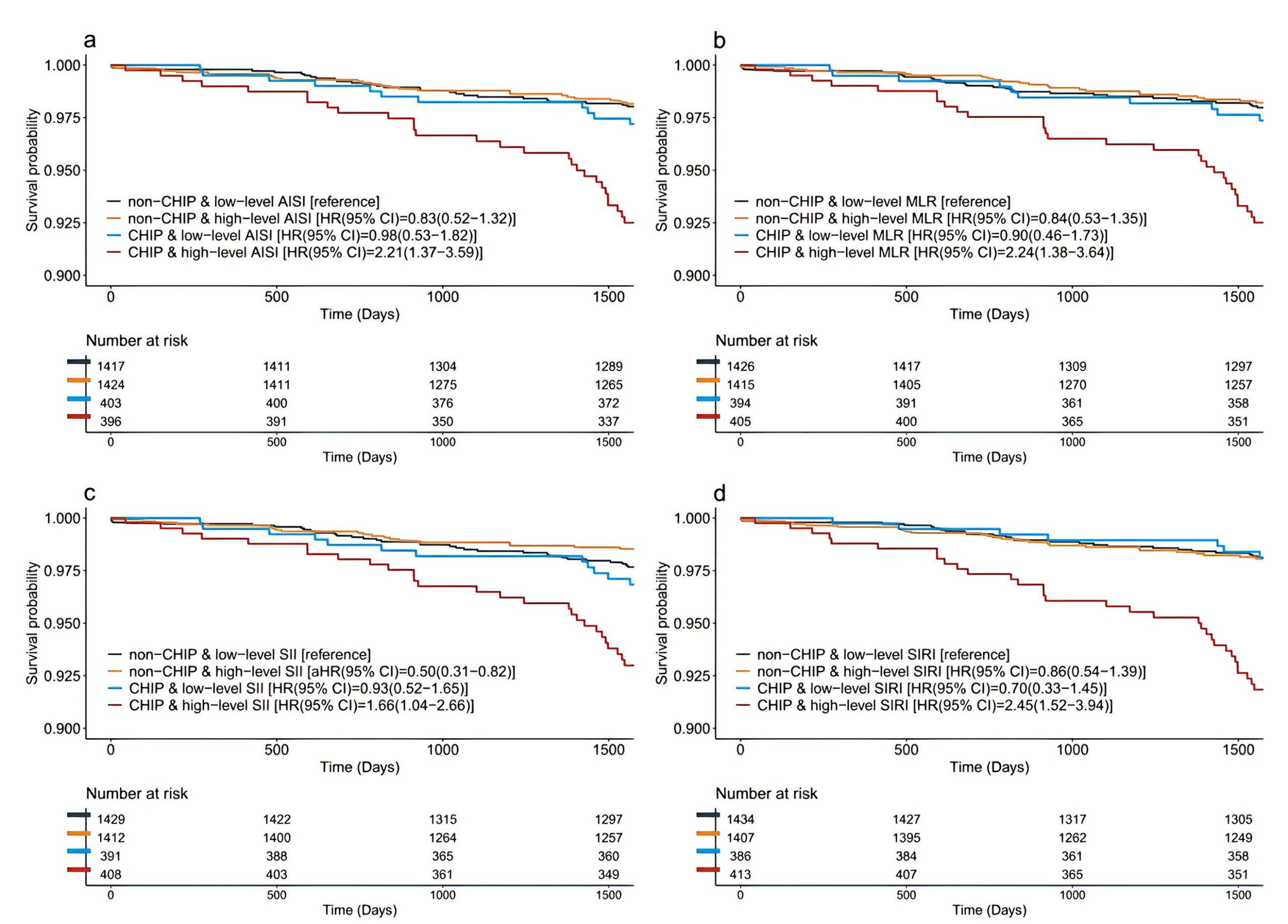
图3按CHIP和常规炎症指数联合分层的全因死亡率的Kaplan-Meier生存曲线。结果根据年龄、性别、体重指数、吸烟、高血压、糖尿病、低密度脂蛋白胆固醇、异常肾小球滤过率、既往经皮冠状动脉介入治疗或冠状动脉旁路移植术、急性冠状动脉综合征、使用四种常规炎症指数(AISI(a)、MLR(B)、SII(c)和SIRI(d))评价全身性炎症,所述四种常规炎症指数在调整多次测试后与CHIP显著相互作用。
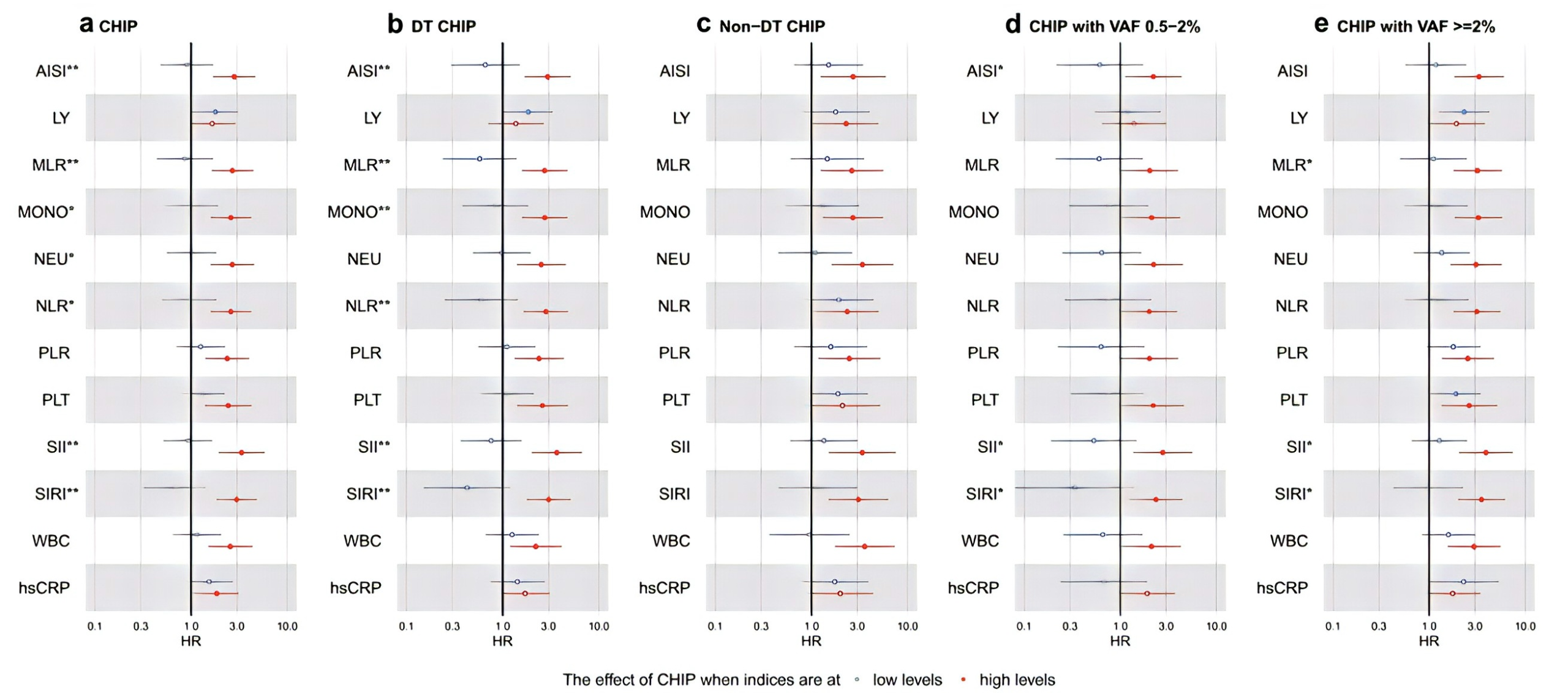
图4 CHIP与按常规炎症指数分层的5年全因死亡率之间的相关性。所用多变量校正模型的详细信息见图2图例。CHIP及其亚型的影响在常规炎症指数水平低(蓝色)或高(红色)的亚组中进行估计。实心圆表示P<0.05时的显著相关性。
5
预测模型改进
在GRACE评分基础上加入CHIP后,C-index从0.614提升到0.644,说明CHIP在传统临床评分之上有独立的增量预测价值。将CHIP和SII同时纳入GRACE评分产生了最高的预测能力,C-index从0.614提升到0.662。
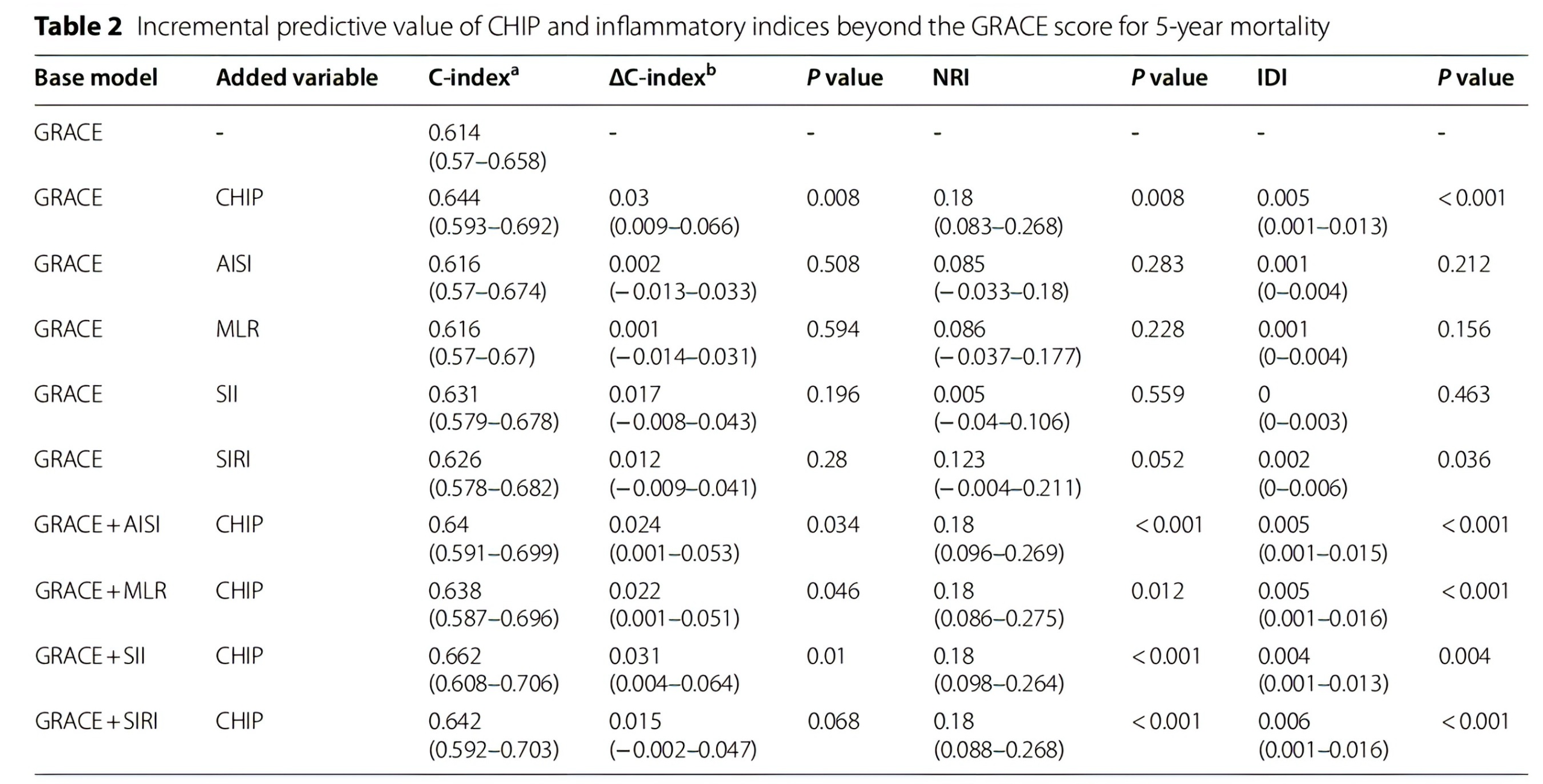
C-index代表包含基础模型加上所加变量的模型的值;ΔC-index表示当所加变量纳入基础模型时C-index的绝对变化
外部验证
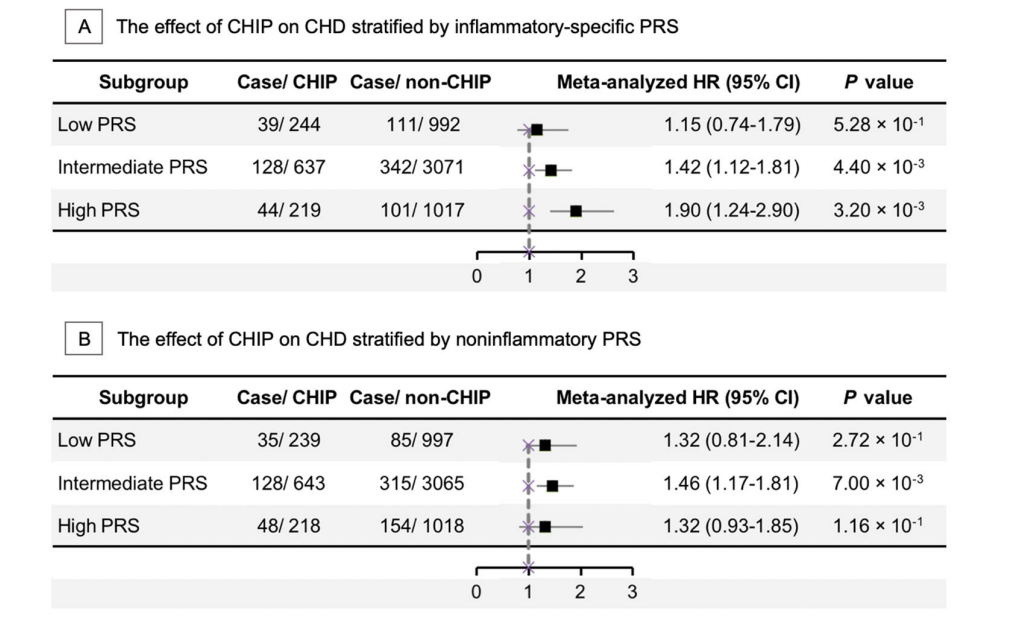
UK Biobank 3715例 PCI 患者中验证了主要发现。在UKB队列中观察到与CHIP携带者表现出更高的5年全因死亡率,与研究队列一致。尽管交互作用未达到统计学显著性,但观察到CHIP与炎症负荷之间存在明显的协同趋势。此外,在该验证分析中也出现了不同炎症水平之间CHIP相关风险的类似差异。例如,在低SIRI个体中CHIP未带来额外风险(HR, 0.91; 95% CI, 0.28–2.92; P=0.874),而SIRI升高则显著加剧了死亡风险(图S11)。
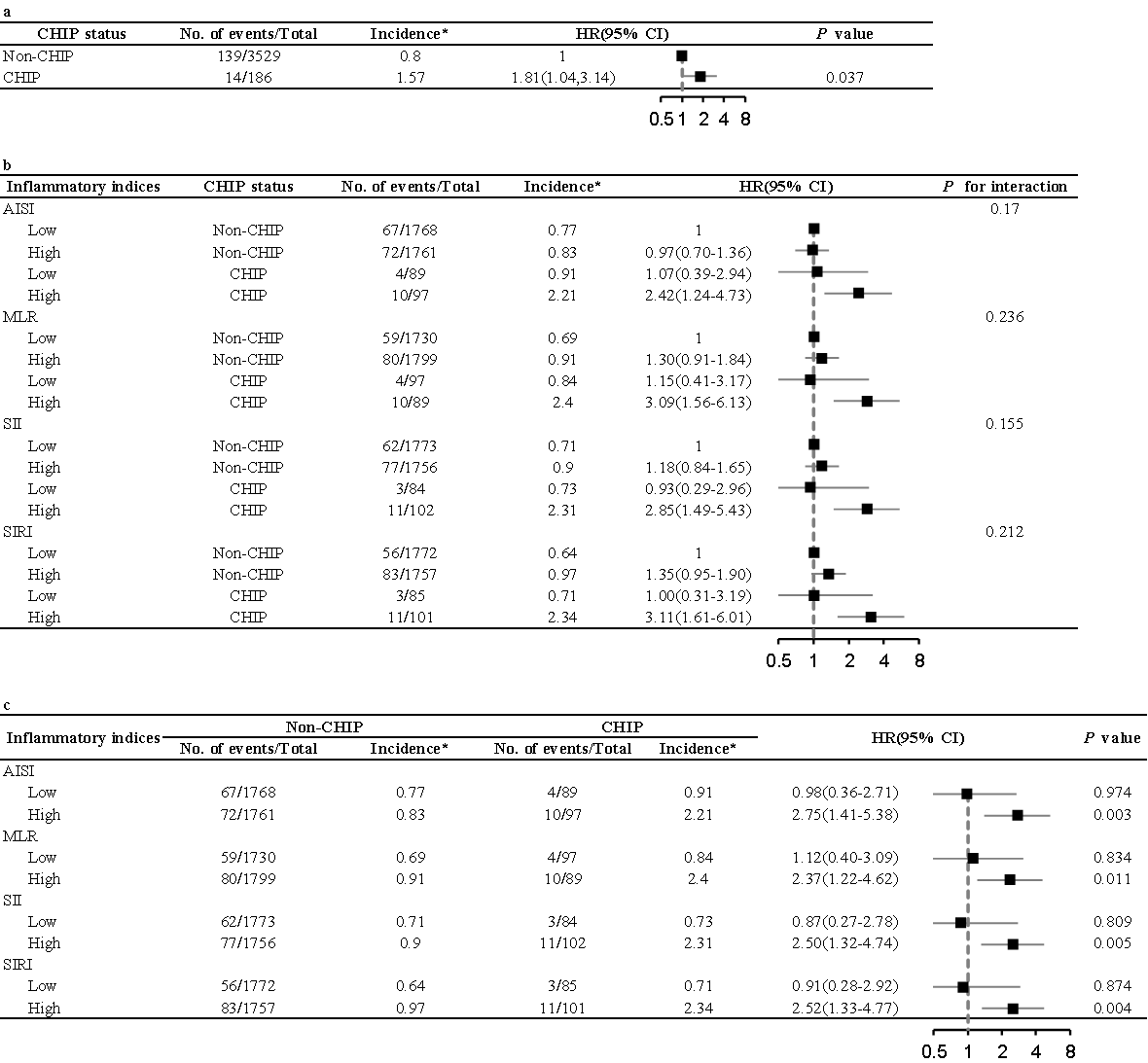
图 S11. UK Biobank外部验证分析总结。(a)CHIP与5年全因死亡率之间的关联。(b)炎症与 CHIP 共同对5年全因死亡率的影响。(c)CHIP对5年全因死亡率的影响(按炎症水平划分)。
核心结论
CHIP独立增加PCI患者全因或心源性死亡风险,这一风险被全身性炎症显著修饰。在高炎症状态下,CHIP相关的死亡风险被显著放大,即使携带小克隆的个体也表现出死亡风险增加。
常规血常规衍生炎症指数(如SII、SIRI、MLR等)可以作为CHIP风险分层的实用临床工具,提示CHIP携带者可能从抗炎治疗中获益。
亮点与临床意义
创新性:首次在 PCI 队列中系统评估 CHIP 与常规炎症指标的交互作用。
转化价值:不依赖昂贵机制性标志物,用临床常规检测就能识别高危 CHIP 携带者。
治疗启示:为CHIP携带者的抗炎干预(如 IL-1β 抑制剂、秋水仙碱等)提供了循证依据。
实用性:SII、SIRI 等指标计算简单,可纳入临床决策流程。
参考文献:
1.Shen X, Song Y, Zhao H, et al. Routine inflammatory indices modify clonal hematopoiesis-related prognostic risk in patients undergoing percutaneous coronary intervention: a real-world cohort study[J]. BMC medicine, 2026.
2.Zhao K, Shen X, Liu H, et al. Somatic and germline variants and coronary heart disease in a Chinese population[J]. JAMA cardiology, 2024, 9(3): 233-242.


