NCCN 2025.V2.0 | 中枢神经系统癌症的诊断与精准治疗
- boke
- 2026-04-21
- 10:27 上午
中枢神经系统(CNS)癌症,是一组高度异质性的肿瘤,起源于脑、脊髓或颅底神经,具有侵袭性、易复发、预后差的特点。成人以胶质母细胞瘤最常见,儿童以髓母细胞瘤、弥漫性中线胶质瘤高发。NCCN CNS癌症指南重点关注成人CNS癌症的诊断与治疗:胶质瘤(WHO 1级,少突胶质细胞瘤[1p与19q共缺失,IDH突变],IDH突变型星形细胞瘤,胶质母细胞瘤),颅内和脊髓室管膜瘤等类型[1]。
一、CNS癌症的诊断:精准定位“病灶”,明确病情
1
影像学检查
MRI(磁共振成像):首选方法,能清晰显示肿瘤的大小、位置、形态,以及是否侵犯周围脑组织、脊髓组织。术后也需要定期通过MRI复查,动态评估手术切除效果,及时发现是否有肿瘤残留或复发。
CT(计算机断层扫描):适用于快速筛查,在显示钙化、骨质改变、出血等方面有优势,但对软组织分辨率较低。
PET-CT:可评估肿瘤代谢活性,辅助判断肿瘤良恶性。
2
病理活检
通过立体定向穿刺或手术切除获取肿瘤组织,进行显微镜下观察、免疫组化分析、分子检测等,是确诊肿瘤类型、分级和制定治疗方案的金标准。
二、CNS癌症的治疗:多手段协同
中枢神经系统癌症是一组复杂、难治的恶性肿瘤,早期诊断、最大安全切除、个体化放化疗 +靶向 / 免疫治疗是核心策略。
1
手术(首选)
切除肿瘤、缓解颅内压、获取病理诊断,为后续治疗提供依据。手术包括近全切(GTR)、次全切(STR)、立体定向活检、开放活检。
2
放射治疗
利用高能射线破坏肿瘤细胞DNA,抑制肿瘤生长,适用于无法手术或术后残留肿瘤。治疗方式包括外照射放射治疗(EBRT)、大分割放疗(HFRT)、全脑放射治疗(WBRT)、体定向放疗(SRS)。
3
全身治疗
全身治疗,有多种选择可用于治疗脑肿瘤,如化疗、靶向治疗、免疫治疗等。烷化剂仍然是治疗原发性脑肿瘤最有效的化疗药物。对于脑转移瘤,全身治疗的选择应基于药物对原发肿瘤的活性以及药物穿过血脑屏障(BBB)的能力。
NCCN指南不同类型中枢神经系统肿瘤的全身治疗方案
(1)成人胶质瘤:局限性胶质瘤
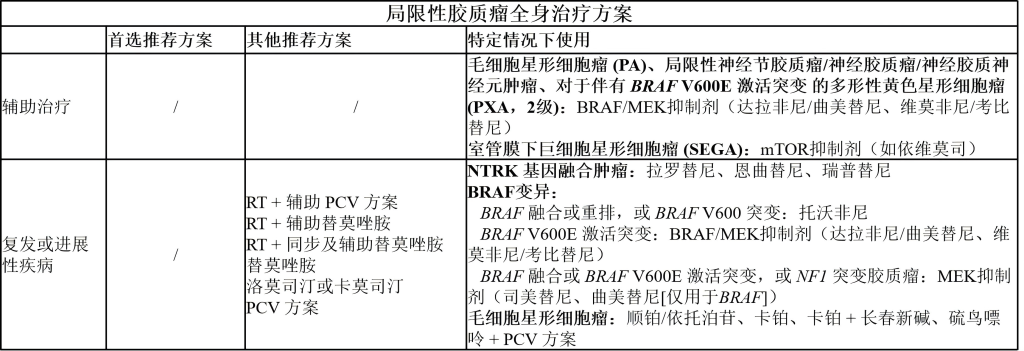
(2)成人胶质瘤:少突胶质细胞瘤(IDH突变,1p19q共缺失)
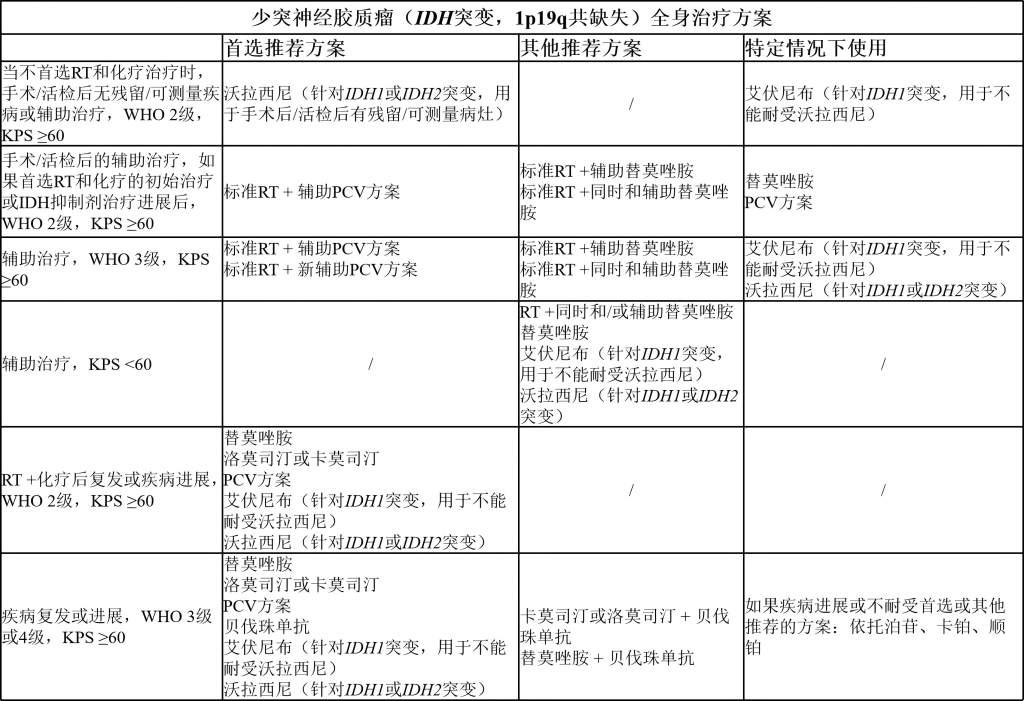
(3)成人胶质瘤:IDH突变型星形细胞瘤
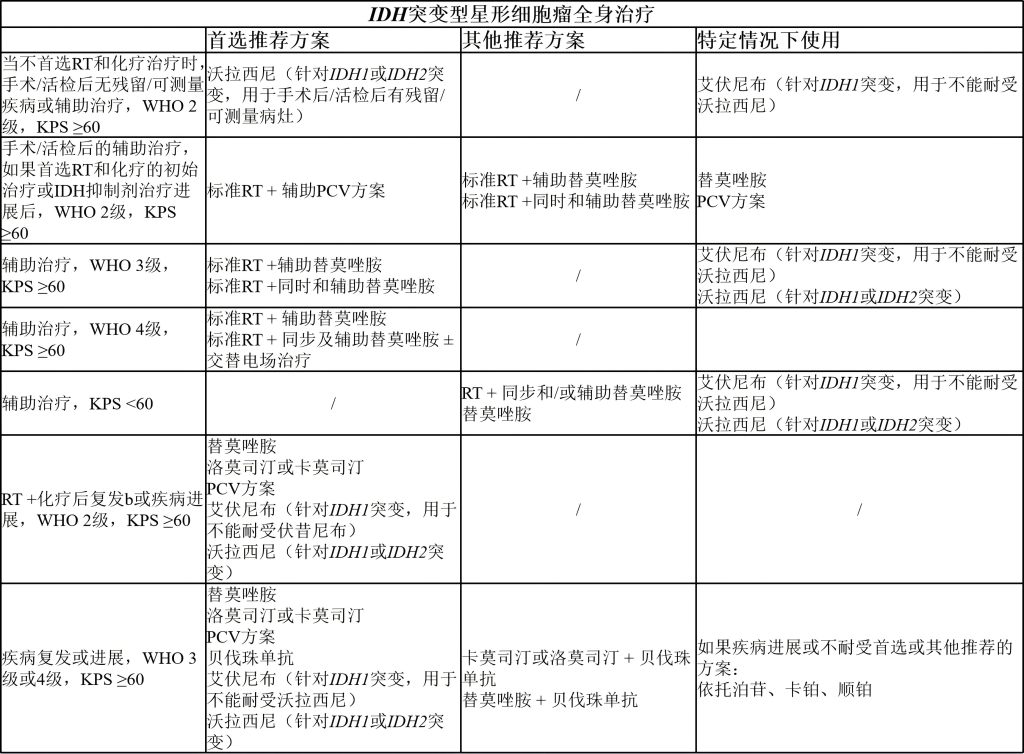
(4)成人胶质瘤:胶质母细胞瘤
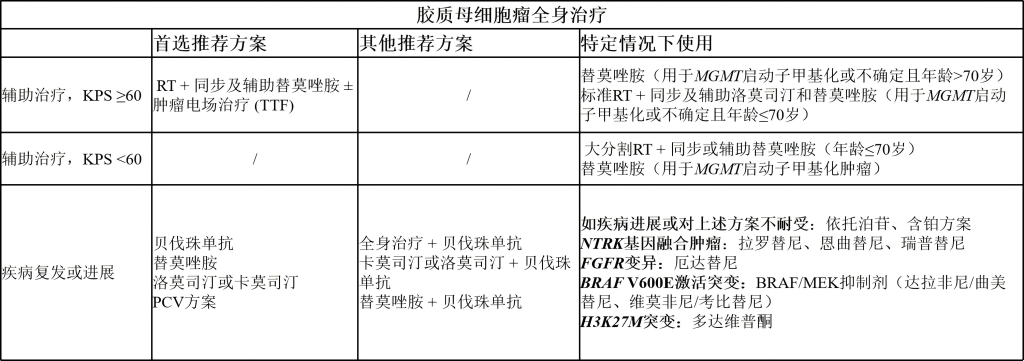
(5)成人颅内和脊髓室管膜瘤(不包括室管膜下瘤)

(6)成人髓母细胞瘤
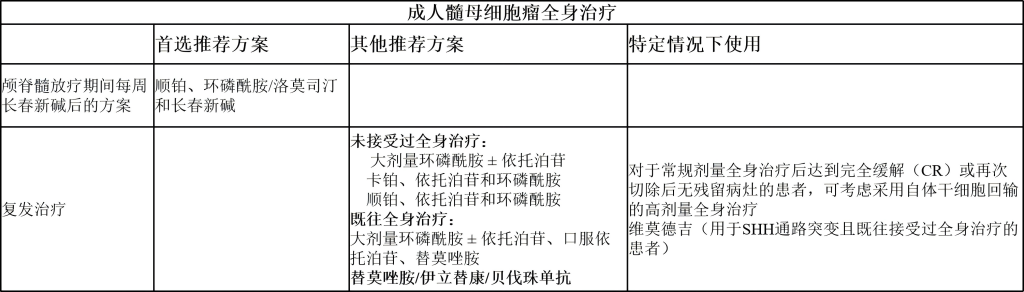
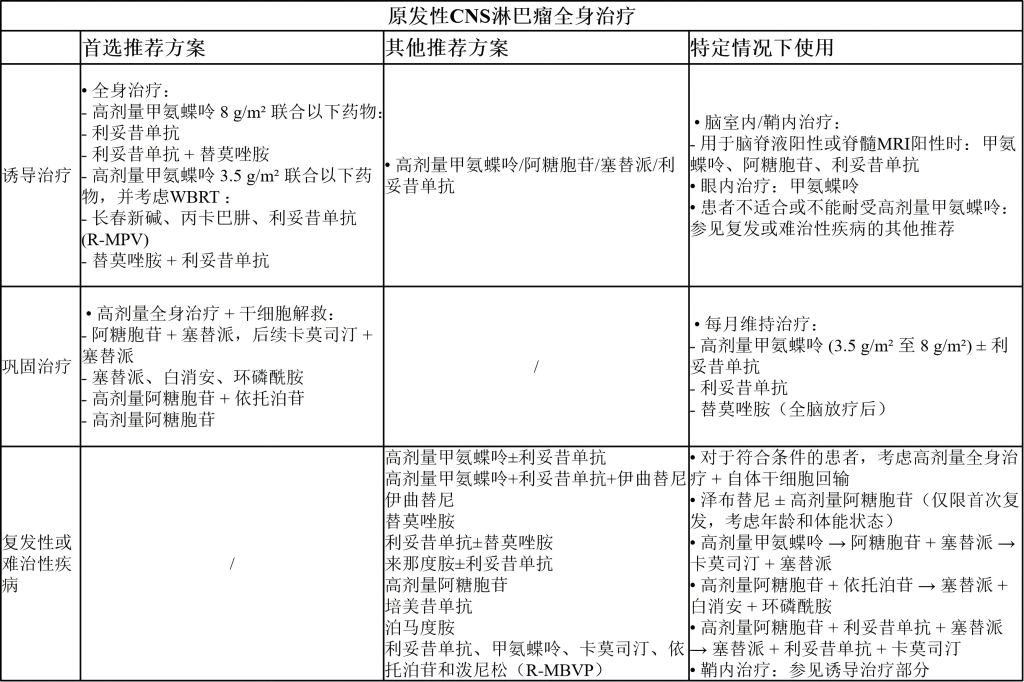
(7)原发性中枢神经系统淋巴瘤
原发性中枢神经系统淋巴瘤(Primary Central Nervous System Lymphoma,PCNSL)是一种侵袭性非霍奇金淋巴瘤,发生在脑、脊髓、眼或软脑膜内。男性发病率高于女性,且发病率随年龄增长而增加。
(8)原发性脊髓肿瘤
原发性脊髓肿瘤是一组组织学多样化的疾病,占所有原发性中枢神经系统肿瘤的2%至4%。MRI成像是诊断脊髓病变的金标准。对于MRI有禁忌的患者,CT脊髓造影可用于诊断。当肿瘤有症状且适合手术切除时,全切除术是首选的初始治疗。

(9)脑膜瘤
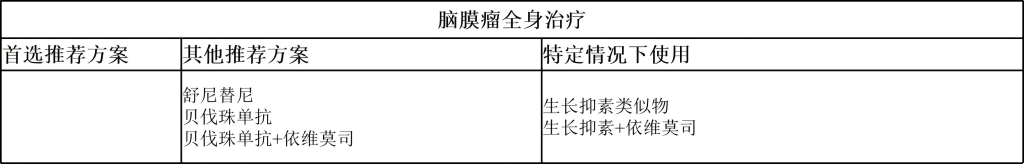
(10)脑转移瘤
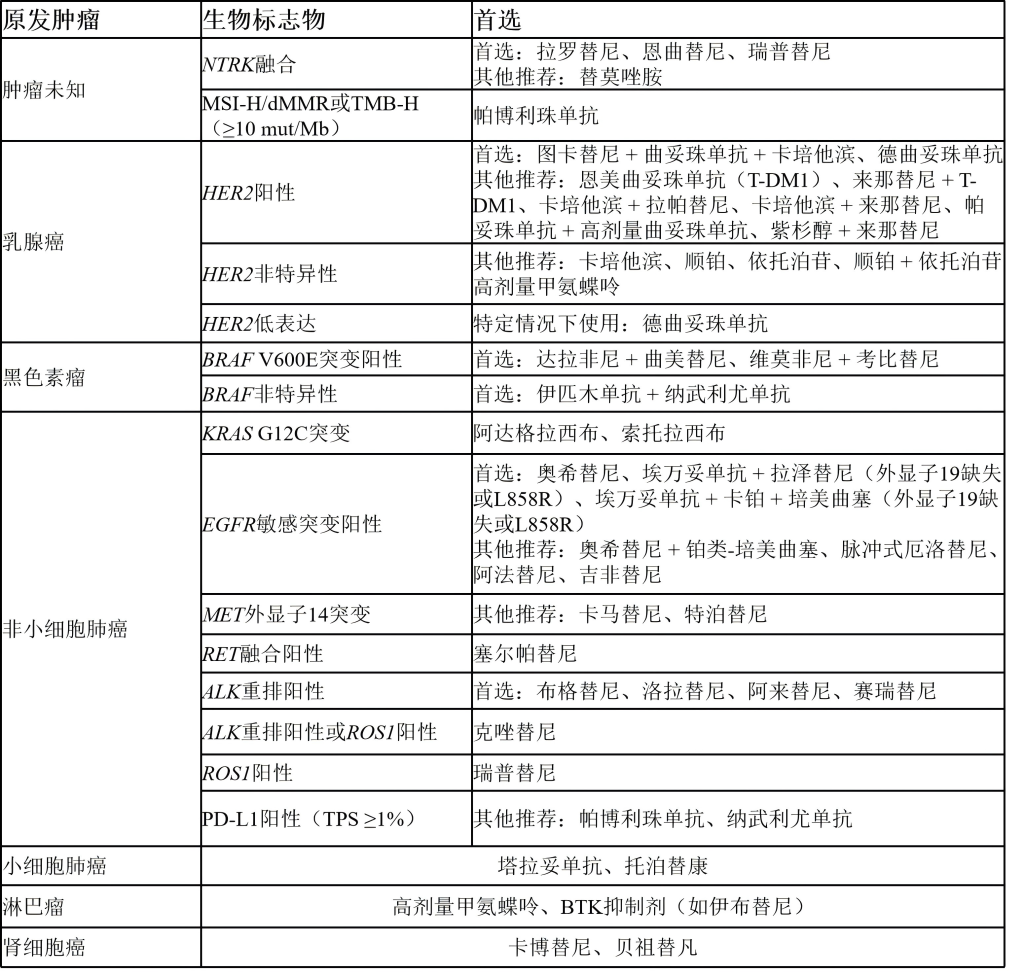
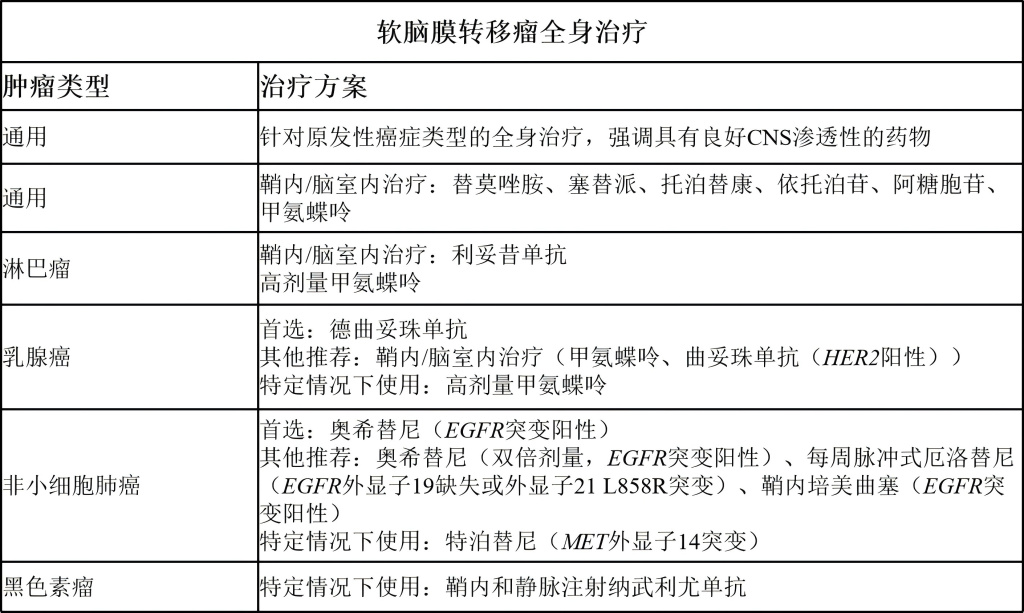
(11)软脑膜转移
三、脑肿瘤分子标志物
分子/遗传学特征检测是标准组织学分析的补充,提供额外的诊断和预后信息,可提高诊断准确性,影响治疗选择,并改善管理决策。
1
胶质瘤相关分子标志物检测:
以下是NCCN指南根据2021年WHO分类系统总结的重点突变[2],但并未涵盖所有胶质瘤中所有临床相关的变异。
(1)IDH1和IDH2突变
推荐意见:所有胶质瘤的检查都需要IDH突变检测。
检测方式:IHC(主要检测IDH1 R132H)、Sanger测序、焦磷酸测序、NGS
(2)1p和19q共缺失
推荐意见:1p/19q 检测是少突胶质细胞瘤分子诊断的重要组成部分。
检测方法:微阵列分析(优先推荐)、FISH
(3)MGMT 启动子甲基化
推荐意见:MGMT启动子甲基化是所有高级别胶质瘤(3级和4级)分子诊断的重要组成部分。
检测方法:甲基化特异性PCR(MSP)、高分辨率熔解曲线分析、焦磷酸测序、液滴数字PCR(ddPCR)
(4)ATRX 突变
推荐意见:胶质瘤病理检查需包含ATRX突变检测。
检测方法:IHC、NGS
(5)TERT 启动子突变
推荐意见:推荐对胶质瘤进行TERT启动子突变检测。
检测方法:Sanger测序,NGS
(6)H3-3A 突变
推荐意见:在适当临床背景下,推荐进行H3-3A和HIST1H3B突变检测。
检测方法:NGS、IHC
(7)BRAF 突变/融合
推荐意见:在适当临床背景下,推荐进行BRA 融合和/或突变检测。
检测方法:测序(BRAF V600E)、RNA-NGS(融合)
(8)ZFTA 与YAP1 融合
推荐意见:建议在适当的临床背景下进行ZFTA和YAP1融合检测,主要用于室管膜瘤的诊断与分型。
检测方法:RNA-NGS、FISH
(9)颅内和脊髓室管膜瘤
推荐意见:建议在适当的临床背景下进行MYCN扩增检测。部分脊髓室管膜瘤显示MYCN扩增。此类肿瘤往往行为更具侵袭性,被定义为SP-EPN-MYCN。
检测方法:FISH
除NCCN提到了分子标志物外,《胶质瘤分子病理诊断中国专家共识》还提出其他的胶质瘤相关分子标志物[3]:CDKN2A/B基因纯合缺失;EGFR变异(包括扩增、突变、重排或剪接改变);第7号染色体获得/第10号染色体丢失(+7/-10);MYB或MYBL1基因变异;FGFR1/2/3基因变异;受体酪氨酸激酶(RTK)家族基因融合;PRKCA基因变异;MN1基因变异;TP53基因突变。
2
髓母细胞瘤相关分子标志物
NCCN指南中提及的髓母细胞瘤分子标志物主要与分子分型相关。WHO建议将髓母细胞瘤进一步分为四个不同的组[4]:(1)WNT激活型;(2)SHH激活和TP53突变型;(3)SHH激活和TP53野生型;(4)非WNT/非SHH激活型。
(1)WNT激活型
分子标志物:β-Catenin表达(核阳性)、6号染色体单体、CTNNB1突变、APC突变
检测方法:IHC、FISH、NGS
(2)SHH激活和TP53野生型
分子标志物:YAP1表达/GAB 表达(SHH通路激活标志)、MYCN扩增 / GLI2扩增 / 14q染色体缺失(TP53野生型预后不良标志物)(TP53野生型特征)
检测方法:IHC、NGS、Sanger测序
(3)SHH激活和TP53突变型
分子标志物:YAP1表达/GAB 表达(SHH通路激活标志)、TP53突变、17p缺失 / TP53区域杂合性缺失(特征性存在)
检测方法:IHC、NGS、Sanger测序
(4)非WNT/非SHH型
非WNT/非SHH激活型根据DNA甲基化谱,可以分为G3型和G4型,并可进一步详细划分为8个分子亚组。
分子标志物:MYC扩增 / 17q等臂染色体(与G3肿瘤预后不良相关)、11号染色体缺失/17号染色体增加(与G4肿瘤预后良好相关)
检测方法:FISH、NGS
3
脑膜瘤相关分子标志物
分子标志物:22q联合1p染色体缺失;CDKN2 A/B纯合缺失、;TERT启动子突变;6、10、14或18号染色体缺失
预后价值:22 q和1 p的同时缺失足以将CNS WHO 2级归为脑膜瘤。累及6、10、14或18号染色体的两个或更多个全臂缺失提示肿瘤风险较高。CDKN 2A/B 的纯合缺失或TERT 启动子突变证明CNS WHO 3级髓母细胞瘤分子亚型。
检测方法:任何经过验证、能够测量全基因组拷贝数变异的检测方法(不推荐FISH)。
除NCCN提到了分子标志物外,《脑膜瘤分子诊疗专家共识》还提出其他的脑膜瘤相关分子标志物[5][6]:
基因突变:NF2突变;PI3K通路相关驱动基因AKTI、PIK3CA异常;Hedgehog通路相关驱动基因SMO、SUFU突变;TRAF7突变;SMARCE1突变;BAP1突变;DMD突变;POLR2A突变。
表观遗传学改变:H3 K27me3;TIMP3甲基化;TP73启动子甲基化
伯科生物在国内已经建设了全流程国产化的高通量核酸合成与应用技术转化中心,建立了GMP厂房和ISO9001、ISO13485质量体系。已经为国内外数百家知名医院、科学研究机构、临床检验所开发了上千款Gene Panel(液相基因芯片),并配套完整的检测试剂,各项性能参数均与国际竞品相当或优于(详见附表1),在基因组、转录组、甲基化组及病原体的检测应用方向均有成熟的产品管线。
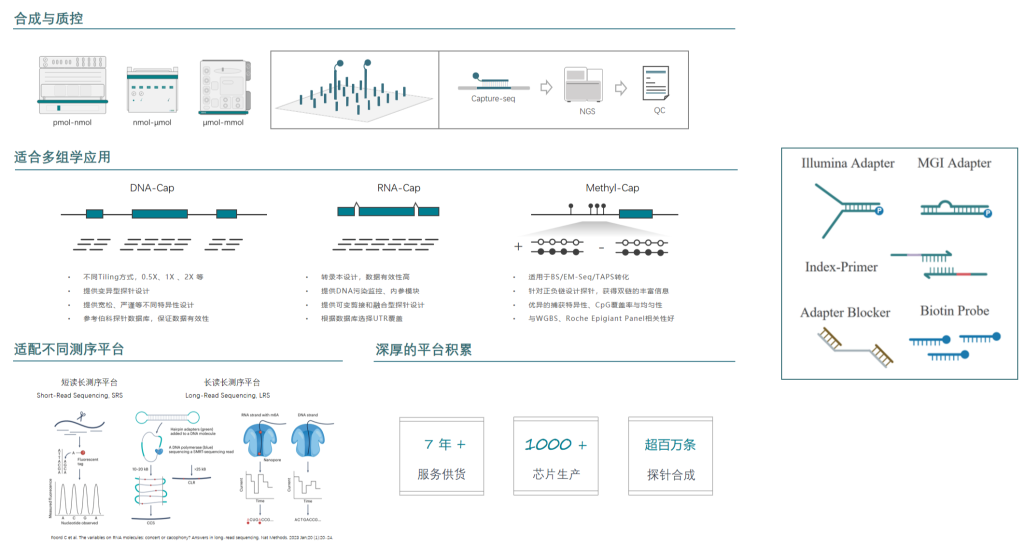
附表1: 产品简介
TargetCap® WES Onco Panel
在肿瘤临床研究与转化的检测应用中,WES(全外显子组测序)通过捕获和测序基因组中所有蛋白质编码区域(约占总基因组的1-2%),高效识别肿瘤样本中的体细胞突变、拷贝数变异及关键驱动基因。它与正常对照样本比较,能够精准筛选出与肿瘤发生、进展及耐药性相关的功能性变异,为揭示不同癌种的基因突变谱、发现潜在治疗靶点以及评估遗传易感性提供核心数据支撑。因此,WES是肿瘤基因组学研究和临床转化应用中的基础工具。
伯科设计的TargetCap® WES Onco Panel目标区域和捕获区域大小分别约为40 Mb和50M+,覆盖基因数量超20000个,其中数百个肿瘤重要相关基因编码区进一步得到覆盖增强,还包含34个融合基因的非编码区(融合基因),能够准确检出SNV、InDel等多种突变类型,实现肿瘤基因组变异的全面解析。
性能表现
采用肿瘤gDNA和血液gDNA样本,使用伯科TargetCap® WES Onco Panel进行杂交捕获,在捕获性能方面,伯科TargetCap® WES Onco Panel表现优异,整体Panel测序深度为500x时,肿瘤相关基因测序深度达到778x,0.2 × Mean占比均在99%左右,Fold 80为1.5-1.6之间。
整体区域QC
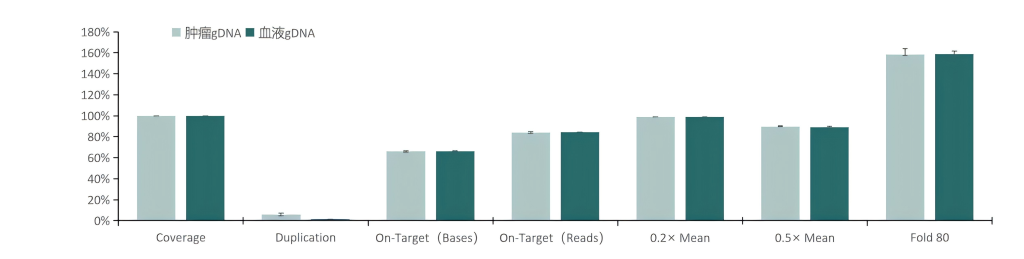
Onco区域QC
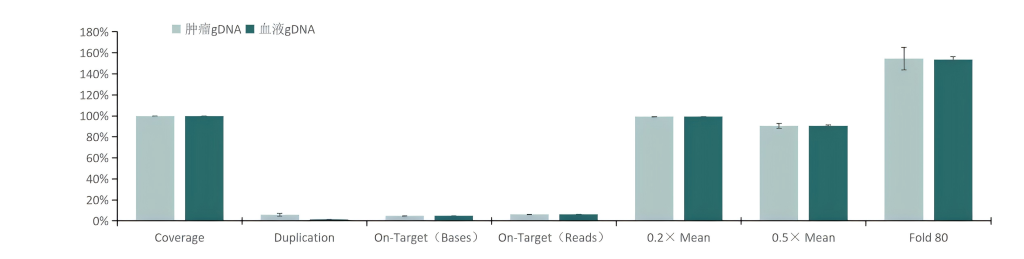
肿瘤液相基因芯片
伯科设计的TargetCap® OncoGene Plus Research Panel基于美国食品药品监督管理局(FDA)批准的用于肿瘤基因检测的FoundationOne CDxTM与MSK-IMPACTTM,其覆盖702个肿瘤相关基因编码区和34个基因的非编码区(融合基因),含有6个MSI和53个化药相关位点,探针覆盖2.32Mb区间。这些区域涵盖更多基因,检测范围更泛,涉及肿瘤高频突变、肿瘤易感、药物靶向、药物耐受等多种类型基因。
性能表现
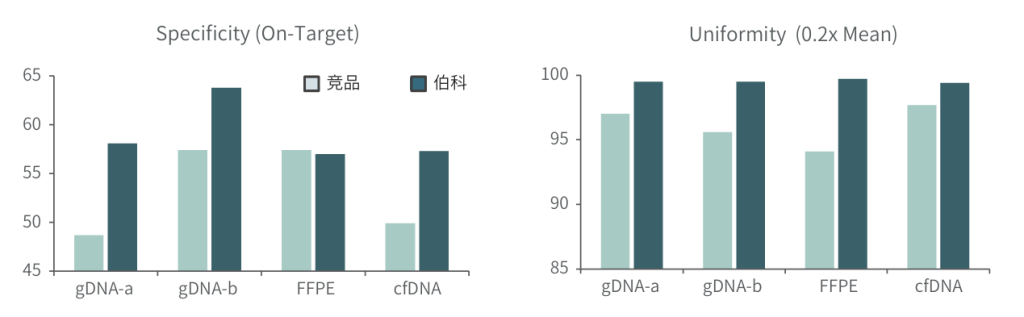
竞品评测
采用gDNA/cfDNA/FFPE/泛肿瘤800gDNA标准品文库,分别使用伯科商品化肿瘤大Panel-OncoGene Plus Research Panel与竞品肿瘤大Panel进行性能比较(二者大小相近),在捕获特异性上(On-Target)和覆盖均一性(0.2XMean)上,伯科均优于竞品。
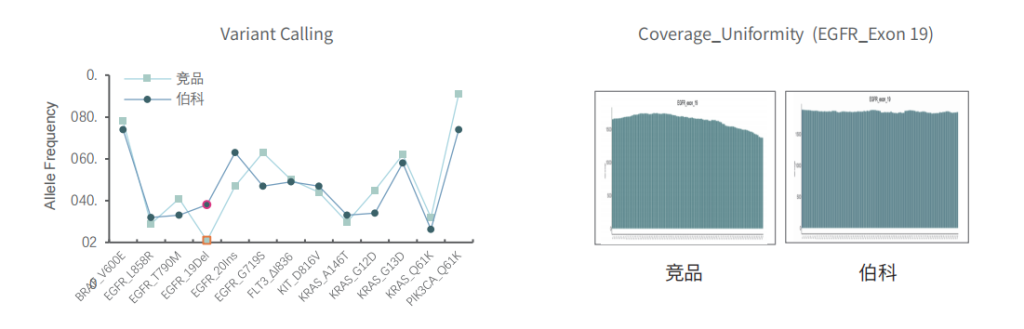
对于gDNA标准品,竞品测序35.9Gb,伯科测序19.6Gb,虽然伯科测序数据少,深度低,但二者的突变频率检出无明显差异,伯科对EGFR的19号外显子缺失变异的检出优于竞品。
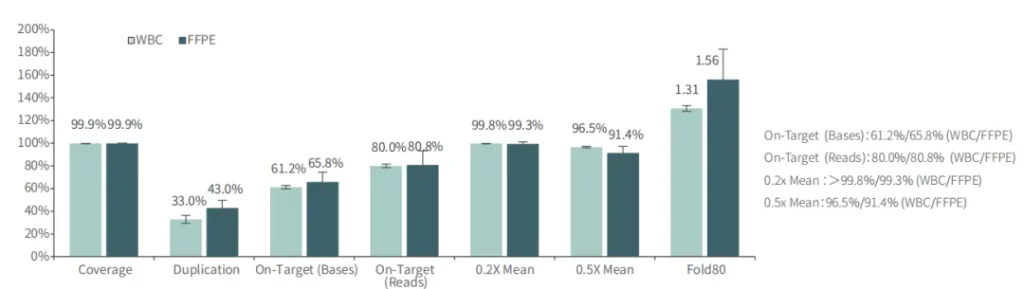
不同样本类型表现
对不同质量的gDNA样本 (WBC/FFPE, >150例),TargetCap® OncoGene Plus Research Panel表现稳定。
杂交与清洗试剂盒v2 简介
试剂盒概述
伯科杂交与清洗试剂盒v2 (TargetCap® Hybridization and Wash Kit v2,下文简称Hyb&Wash Kit v2)简化了试剂组分和操作流程,同时仍保持优异的捕获性能。Hyb&Wash Kit v2包含4种缓冲液组分,仅需3步清洗,操作流程更加便捷。
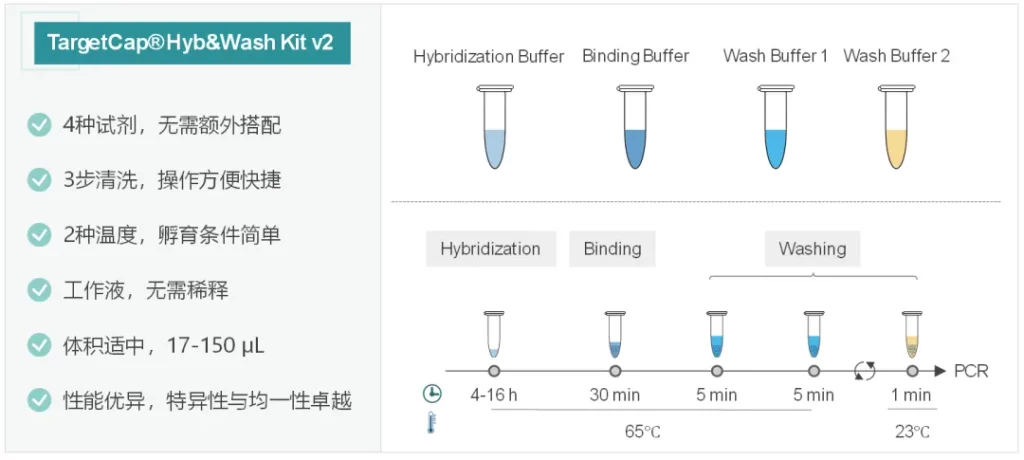
性能表现介绍
Ⅰ. 基本QC表现
使用NA12878和NA24694 gDNA标准品,采用三款不同大小的Gene Panel (650Kb、2.3Mb和42Mb) 对Hyb&Wash Kit v2 和 v1 进行比较测试。
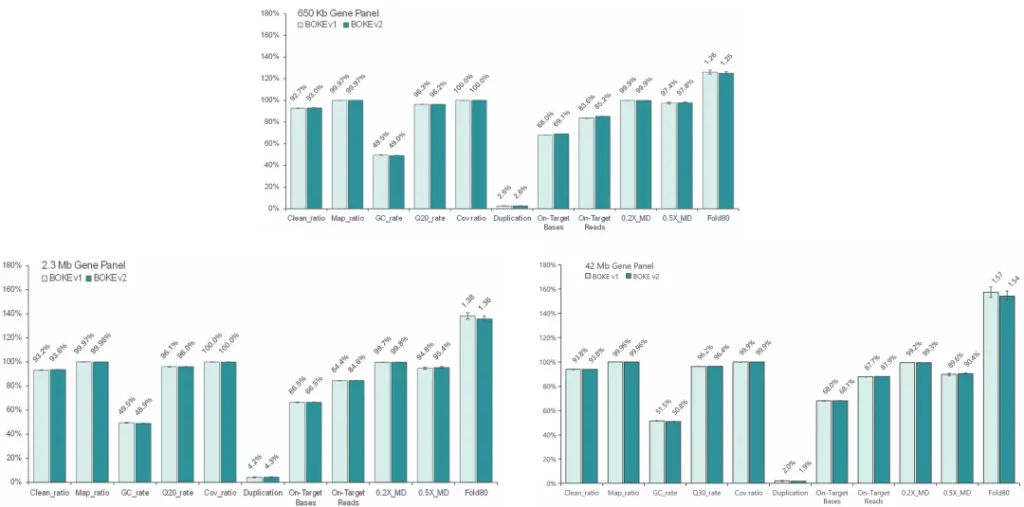
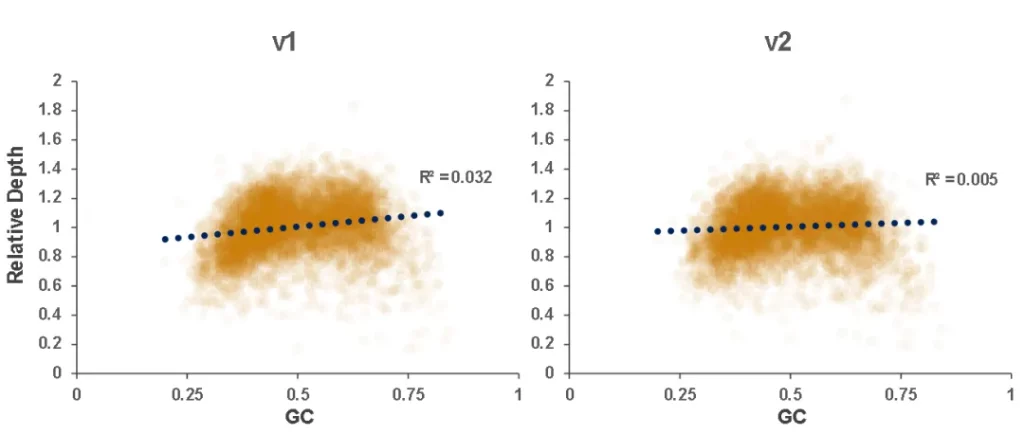
结果显示,在不同大小的Gene Panel中,对于杂交与清洗试剂盒的关键参数-中靶率和均一性,v2与v1试剂盒表现相当,v2试剂盒表现更好的均一性(0.2X_MD、0.5X_MD和Fold80)。
Clean_ratio、Map_ratio等基本参数两款试剂盒表现一致,由于v2试剂盒对低GC目标区域覆盖更佳,其GC_rate率略低于v1。
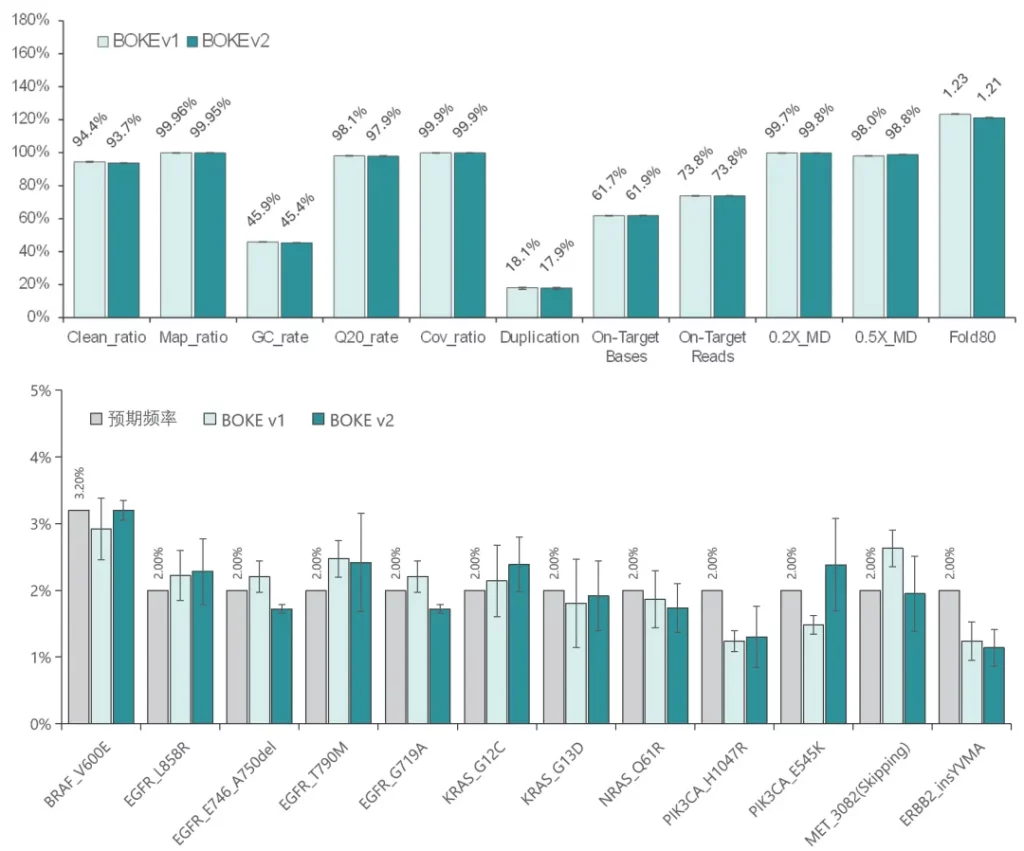
Ⅱ. 低频变异检测
使用肿瘤 SNV gDNA 标准品Ⅱ (GW-OGTM006) 对Hyb&Wash Kit v2的低频变异检测性能进行验证。GW-OGTM006 DNA标准品包含 EGFR、KRAS、NRAS、BRAF、PIK3CA、FGFR3、Her2、MET 等多个常见伴随诊断基因及位点,包含点突变、插入和缺失等多种变异类型。
采用300 Kb Gene Panel对该标准品进行捕获,捕获数据显示,v1与v2试剂盒的基本捕获性能表现相当,v2的中靶率与均一性略优于v1。同时,v1与v2试剂盒均能对12个已知变异准确检出。
参考文献:
1.NCCN Clinical Practice Guidelines in Central Nervous System Cancers. (2025 Version 2).
2.2021年世界卫生组织中枢神经系统肿瘤分(第五版)分子诊断指标解读
3.胶质瘤分子病理诊断中国专家共识(2025版)
4.Cotter J A, Hawkins C. Medulloblastoma: WHO 2021 and beyond[J]. Pediatric and Developmental Pathology, 2022, 25(1): 23-33.
5.脑膜瘤分子诊疗专家共识(2022版)
6.Sahm F, Bertero L, Brandner S, et al. European Association of Neuro-Oncology guideline on molecular testing of meningiomas for targeted therapy selection[J]. Neuro-oncology, 2025, 27(4): 869-883.


