2026 V2.0 NCCN指南|急性髓系白血病(AML)的诊断分层与精准治疗
- boke
- 2025-12-30
- 5:06 下午
一
疾病概述
急性髓系白血病(AML)是一种异质性的血液系统恶性肿瘤,是成人中最常见的急性白血病形式,其特征是外周血、骨髓(BM)和/或其他组织中髓系原始细胞的克隆性扩增。AML以及骨髓增生异常综合征(MDS)的发病率随着年龄的增加而上升。目前研究表明确定会增加AML风险的环境因素包括长期接触石油化工产品、溶剂(如苯)、杀虫剂、以及电离辐射等。
二
诊断与预后分层
1
AML诊断
血常规:白细胞计数可高、可低或正常,分类可见原始和幼稚髓细胞;血红蛋白和血小板常降低。
骨髓穿刺涂片:骨髓增生明显活跃或极度活跃,原始细胞≥20%,伴有不同程度的病态造血。
细胞化学染色:常用的有过氧化物酶(POX)染色、苏丹黑B(SB)染色、非特异性酯酶(NSE)染色等,有助于白血病细胞类型的鉴别。
免疫表型分析:通过流式细胞术检测白血病细胞表面抗原,有助于确定白血病细胞的来源和分化阶段,对诊断、分型和预后评估有重要意义。常见的髓系抗原包括CD13、CD33、CD117等。
细胞遗传学和分子遗传学检查:染色体核型分析、荧光原位杂交(FISH)、NGS测序分析染色体结构变异和FL3T-ITD等基因突变,有利于AML预后分层和治疗[2]。
2
AML预后分层
染色体核型和分子标志物是预测AML缓解率、复发风险和总生存期(OS)的最重要因素,NCCN指南采用欧洲白血病网(ELN)的风险分层建议,基于细胞遗传学、分子遗传学以等检测,将急性髓系白血病(AML)的预后分层分为三类:
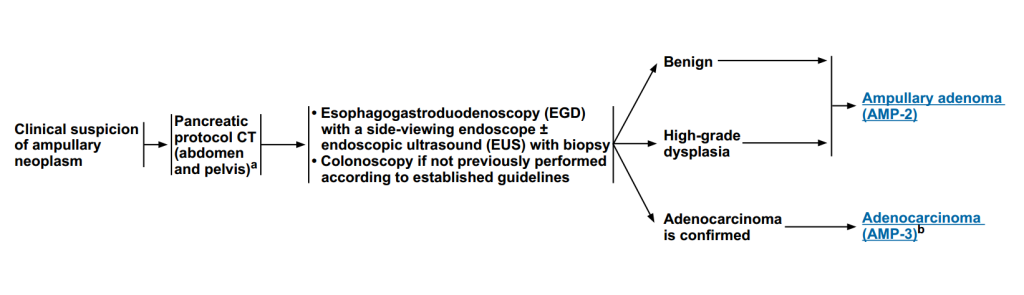
图1 壶腹肿瘤患者临床表现与检查流程
三、治疗方案
1
壶腹腺瘤治疗方案:
首选治疗是进行内镜切除术(直径≤20 mm的壶腹腺瘤),根据切除结果进行下一步治疗。
若切缘为阴性(肿瘤被完整切除),直接进入内镜监测;
若切缘为阳性(肿瘤未切净),则再次进行内镜切除术或进行外科壶腹切除术、胰十二指肠切除术。
无法进行内镜切除术,则进行胰十二指肠切除术。
内镜切除或外科壶腹切除术后切缘阴性的患者应进行内镜监测,而胰十二指肠切除术后患者无需监测。
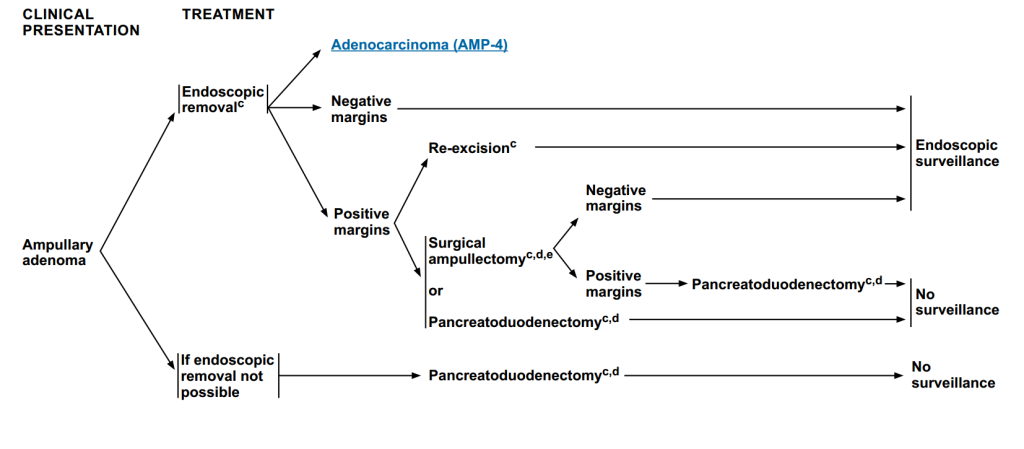
图2 壶腹腺瘤治疗方案
2
壶腹腺癌治疗方案
(1)壶腹腺癌患者检查评估
对于确诊为腺癌患者,治疗时先进行CT胸部和胰腺CT(腹部和骨盆)、肝功能检查,基线CA 19-9、癌胚抗原(CEA)。根据临床指征考虑内窥镜逆行胰胆管造影(ERCP)/经皮肝穿刺胆管造影(PTC)、遗传突变的基因检测和多学科评估。
完成上述检查后,若无转移性疾病按照局部疾病治疗方案进行治疗;若有转移型疾病,按照转移型疾病治疗方案进行治疗。
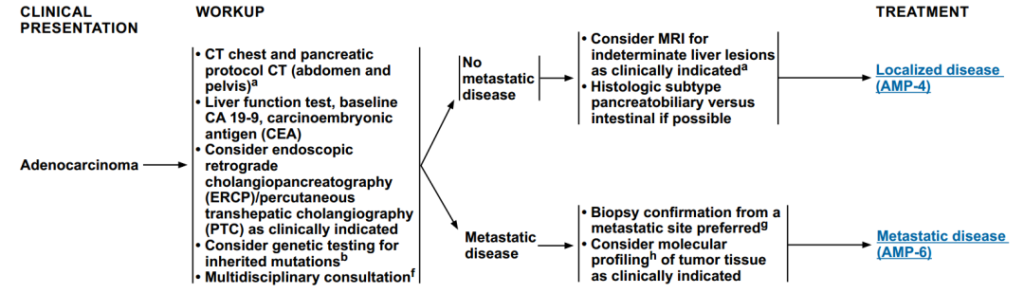
图3 壶腹腺癌患者进一步检查评估
(2)壶腹腺癌的治疗:局部疾病治疗
优先考虑直接进行手术(胰十二指肠切除术)。
对于具有高风险特征(包括影像学表现、CA 19-9 显著升高、癌胚抗原CEA显著升高、原发肿瘤较大、区域淋巴结较大、体重过度下降和剧烈疼痛)的患者,考虑新辅助全身治疗±后续放化疗;如果有临床指征,考虑胆道支架植入术。在治疗完成后进行重复胰腺CT或MRI评估,根据评估结果进行下一步治疗方案:若评估为“可切除”,则进行胰十二指肠切除术;若评估为“局部晚期”,则按照转移型疾病治疗方案进行治疗。
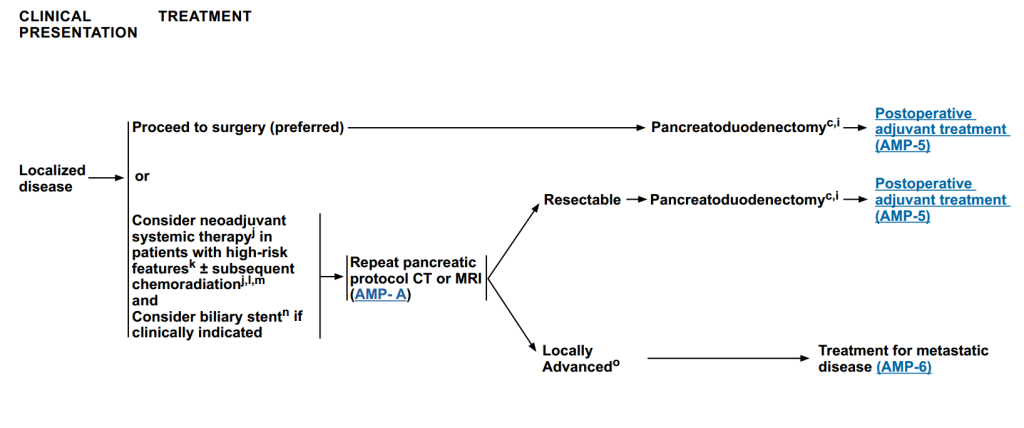
图4 壶腹腺癌局部疾病治疗方案
术后辅助治疗:
根据切除手术后不同的病理分期,决定后续的辅助治疗。
Ⅰ期:进行系统治疗(化疗)或考虑观察。
Ⅱ期:全身治疗±后续放化疗或考虑观察。
Ⅲ期:全身治疗±后续放化疗。
治疗之后,需进行术后监测。在监测中发现“疾病进展”,则患者进入后续治疗。
监测频率:术后前2年:每3-6个月一次;第3至5年:每6-12个月一次。
监测内容:病史与体格检查、胸部CT、腹部和盆腔增强CT或MRI、肿瘤标志物(CEA和CA 19-9)。
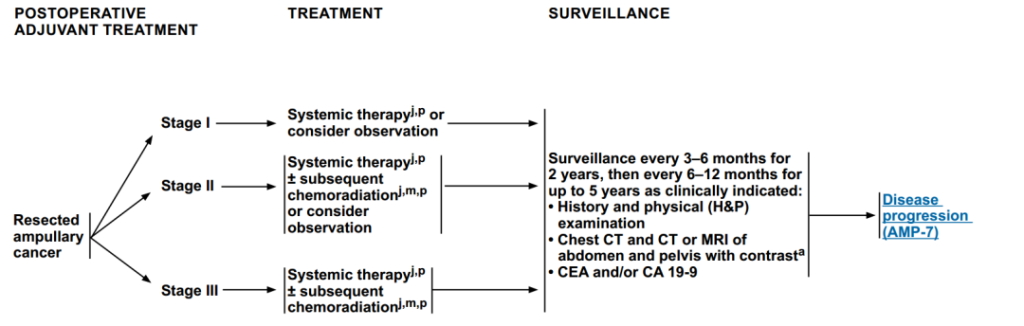
图5 术后辅助治疗方案
(3)壶腹腺癌的治疗:转移型疾病治疗
在治疗方案开始前,需进行遗传突变基因检测和肿瘤组织分子谱分析(如果之前未做)。然后根据患者的体能状态(PS)进行分层,从而进行不同的治疗:
体能状态良好(Good PS,定义为胆道引流良好,营养摄入充足):
全身治疗 靶向治疗(基于肿瘤组织分子谱) 全身治疗,随后进行姑息性放射治疗(RT) 全身治疗,随后针对肝或肺转移瘤进行手术或其他局部定向治疗(适用于对全身治疗有反应/病情稳定的特定转移性疾病患者)
后续若出现疾病进展,则进入后续治疗。
体能状态差(Poor PS):
姑息性放疗与最佳支持治疗 考虑系统治疗 考虑靶向治疗 考虑姑息性放疗
注:姑息性放疗是指在恶性肿瘤已处于晚期、发生转移或无法通过放疗根治的情况下,为了缓解症状、减轻痛苦、改善患者生活质量而进行的放射治疗,其核心目标不是治愈肿瘤。
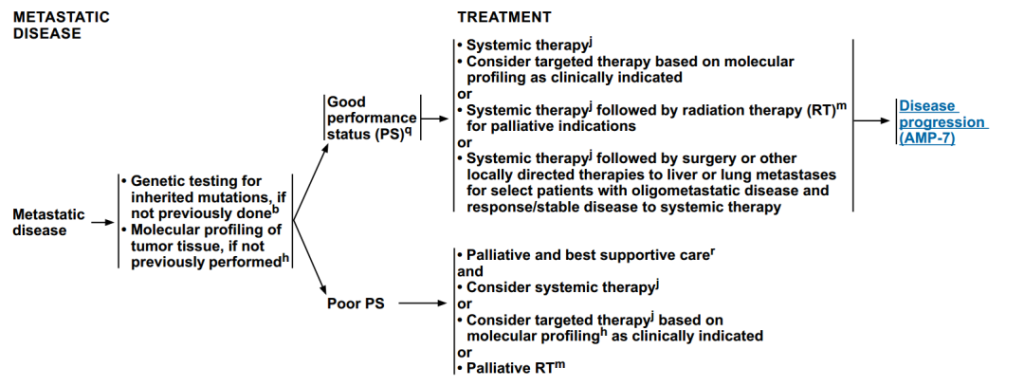
图6 转移性壶腹部癌治疗方案
(4)后续治疗方案
根据患者的体能状态(PS)分为不同的治疗方案:
体能状态良好
一线治疗优先进行临床试验,其他选择包括全身化疗、基于分子谱分析的靶向治疗、针对镇痛治疗无效的严重疼痛进行姑息性放疗。
二线治疗包括姑息治疗和最佳支持治疗或纳入临床试验。
临体能状态差
应接受姑息治疗和最佳支持治疗,并根据临床指征考虑全身治疗、基于分子谱分析的靶向治疗,或姑息性放疗。

图 7 壶腹部癌疾病进展后的后续治疗方案
具体治疗方案
a.辅助治疗:
壶腹癌根治性切除后常使用辅助治疗,最常见的形式是化疗。放疗也可用于辅助治疗场景,通常与化疗联合使用。

b.转移性疾病治疗—一线全身治疗

c.疾病进展治疗

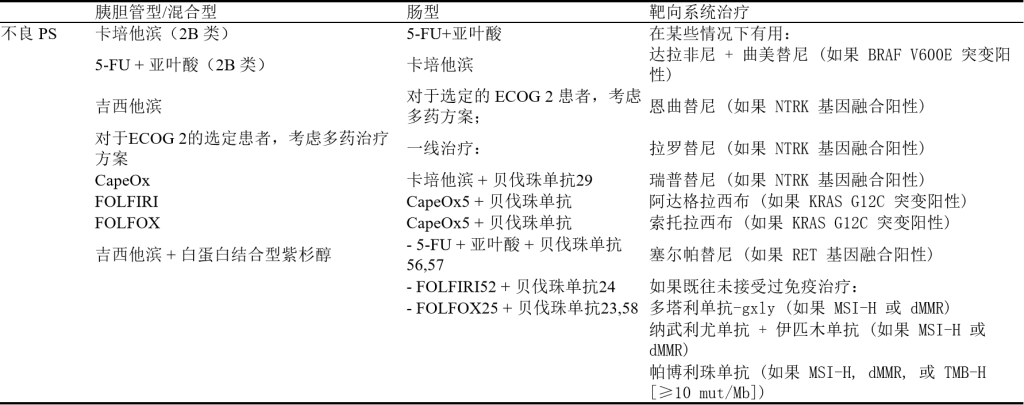
四、壶腹癌的遗传学
壶腹癌中已报道的其他体细胞改变包括APC、TP53、CDKN2A、DPC4、ELF3、PIK3CA和SMAD4突变、HER2扩增和微卫星不稳定性(MSI)。已报道的致病性突变包括BRCA1/2、ATM、RAD 50和MUTYH。
NCCN指南建议所有确诊壶腹癌的患者使用遗传性综合性的Gene Panel进行遗传性突变检测;对于致病性突变(ATM、BRCA1、BRCA2、CDKN2A、MLH1、MSH2、MSH6、PALB2、PMS2、STK11和TP53)检测呈阳性的患者或具有阳性癌症家族史(尤其是胰腺癌/壶腹癌)的患者,建议进行遗传咨询。
对于局部晚期/转移性疾病患者,建议进行肿瘤/体细胞分子谱分析用以识别罕见变异。建议通过FDA批准或验证的下一代测序(NGS)检测,筛查潜在可靶向的体细胞改变,包括但不限于:融合基因(如ALK、NRG1、NTRK、ROS1、FGFR2、RET)、突变(如BRAF、BRCA1/2、KRAS、PALB2)、扩增(HER2)、MSI、TMB。优选肿瘤组织检测,若无法进行肿瘤组织检测,可考虑循环肿瘤DNA检测。
基因靶向技术结合高通量测序在壶腹癌的精准诊疗中发挥关键作用,它能够检测出许多体细胞变异和胚系变异,这对肿瘤的精准诊断与分型以及家族性遗传风险评估有重要作用[2]。在治疗方面,基因靶向技术结合高通量测序能检测出特定基因突变或融合,可针对性选择靶向药物;同时通过检测MSI、TMB等免疫治疗相关标志物,指导免疫治疗药物的使用[3]。
伯科生物在国内已经建设了全流程国产化的高通量核酸合成与应用技术转化中心,建立了GMP厂房和ISO9001、ISO13485质量体系。已经为国内外数百家知名医院、科学研究机构、临床检验所开发了上千款Gene Panel(液相基因芯片),并配套完整的检测试剂,各项性能参数均与国际竞品相当或优于(详见附表1),在基因组、转录组、甲基化组及病原体的检测应用方向均有成熟的产品管线。
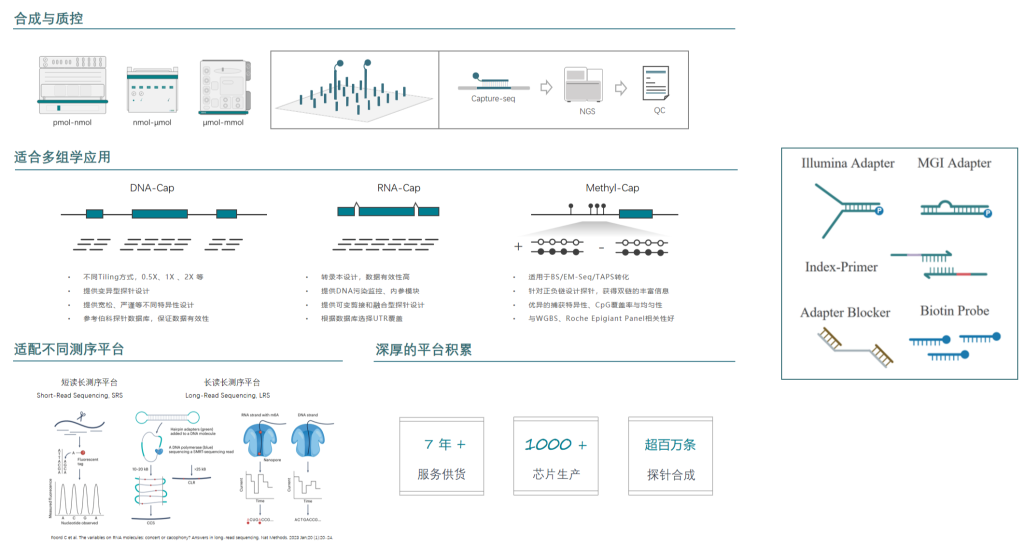
附表1: 产品简介
血液肿瘤液相基因芯片
TargetCap® Haematological Disease Research Panel是一款用于血液肿瘤研究分析的基础型panel,覆盖407个血液病相关基因,探针覆盖约2Mb区间。探针浓度已知,可独立或进一步掺入其他探针使用。
性能表现
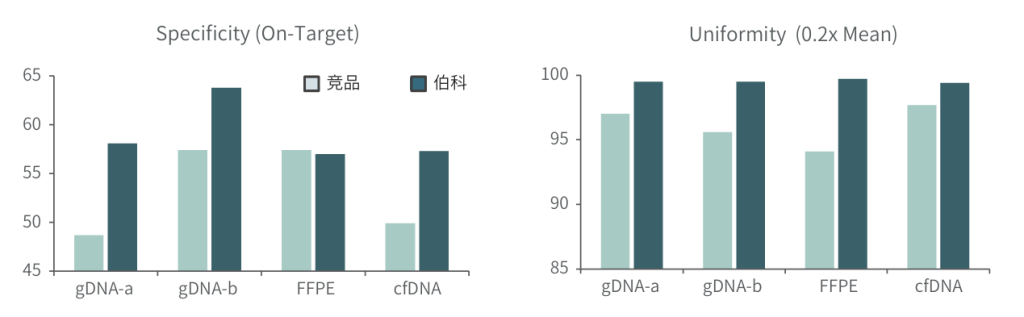
竞品评测
采用gDNA/cfDNA/FFPE/泛肿瘤800gDNA标准品文库,分别使用伯科商品化肿瘤大Panel-OncoGene Plus Research Panel与竞品肿瘤大Panel进行性能比较(二者大小相近),在捕获特异性上(On-Target)和覆盖均一性(0.2XMean)上,伯科均优于竞品。
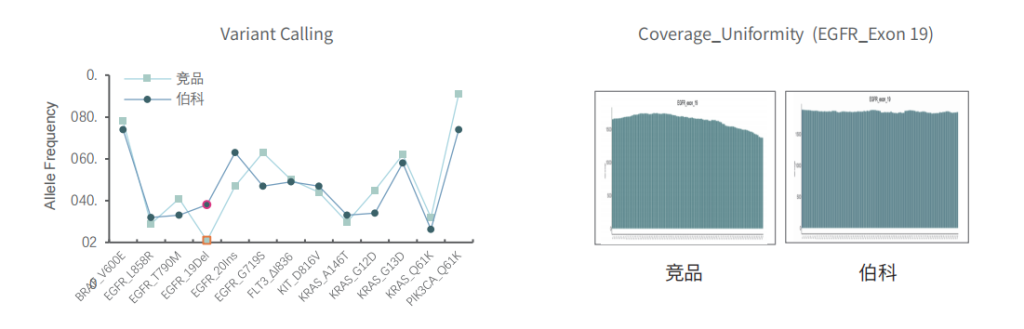
对于gDNA标准品,竞品测序35.9Gb,伯科测序19.6Gb,虽然伯科测序数据少,深度低,但二者的突变频率检出无明显差异,伯科对EGFR的19号外显子缺失变异的检出优于竞品。
不同样本类型表现
对不同质量的gDNA样本 (WBC/FFPE, >150例),TargetCap® OncoGene Plus Research Panel表现稳定。
杂交与清洗试剂盒v2 简介
产品概述
伯科杂交与清洗试剂盒v2 (TargetCap® Hybridization and Wash Kit v2)简化了试剂组分和操作流程,同时仍保持优异的捕获性能。该试剂盒由4种缓冲液组成,分别为Hyb Buffer、Bingding Buffer、Wash Buffer 1和Wash Buffer 2,所有试剂均为1x缓冲液,可以直接使用,同时清洗步骤仅需3步,整个操作流程更加便捷。

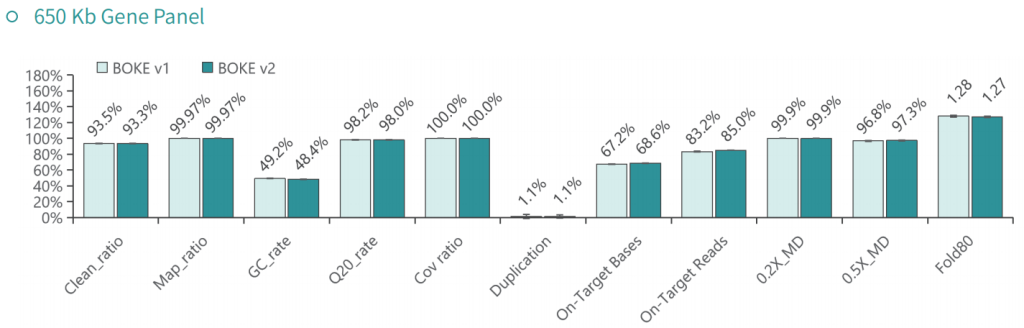
基本捕获性能
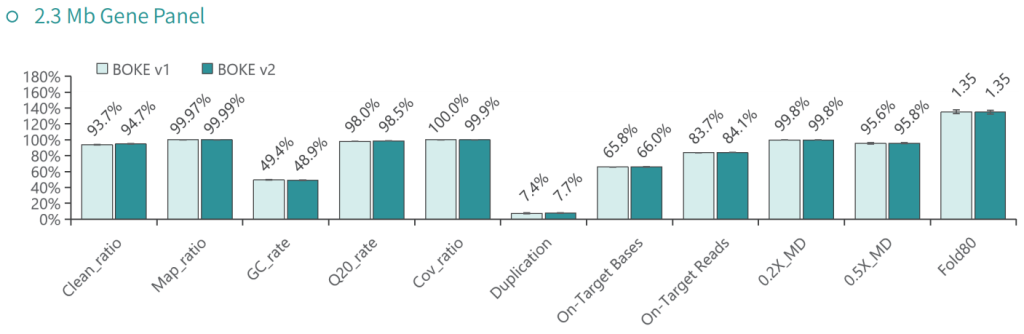
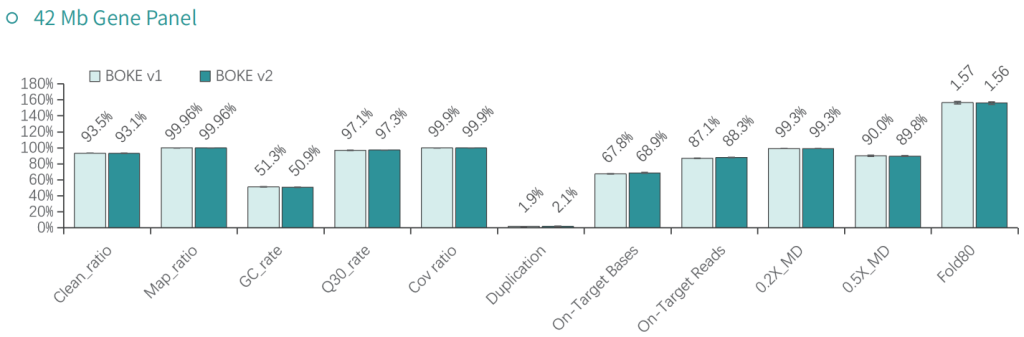
使用NA12878和NA24694 DNA标准品,分别采用不同大小的Gene Panel对TargetCap® Hybridization and Wash Kit v1和v2进行比较。结果显示,在不同大小的 Gene Panel 中, v2试剂盒的中靶率和均一性与v1试剂盒表现基本一致,v2试剂盒表现略好。
低频变异检测
使用肿瘤 SNV gDNA 标准品Ⅱ (GW-OGTM006) 对TargetCap® Hybridization and Wash Kit v1和 v2 进行验证。GW-OGTM006 DNA标准品包含 EGFR、KRAS、NRAS、BRAF、PIK3CA、FGFR3、Her2、MET 等多个常见伴随诊断基因及位点,包含点突变、插入和缺失等多种变异类型。
a. 基本QC
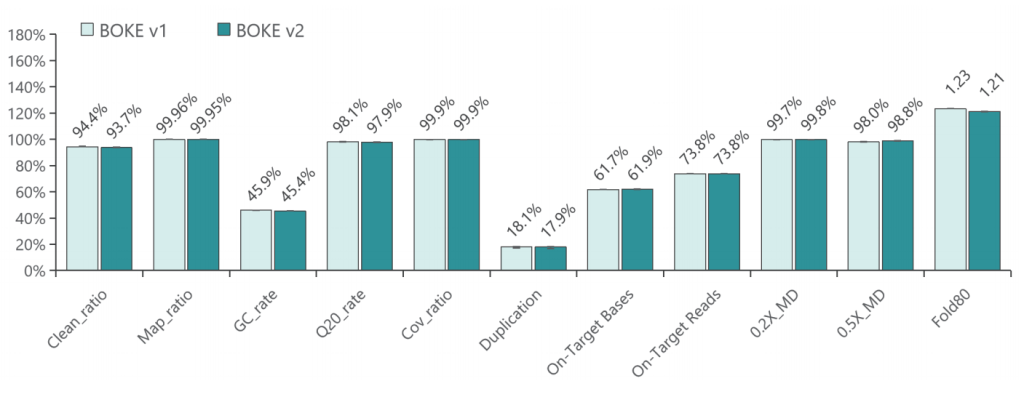
采用300Kb Gene Panel对该标准品进行捕获,捕获数据显示,v1与v2试剂盒的基本捕获性能表现相当,v2略优于v1。
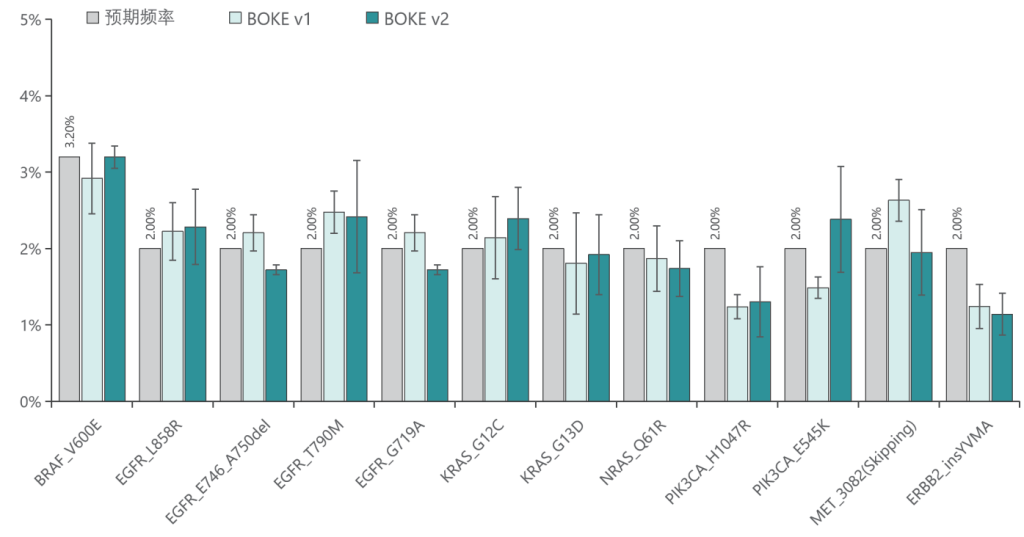
b. 变异检测
v1与v2试剂盒均能对12个已知变异准确检出。
参考文献:
1. 中国成人急性淋巴细胞白血病诊断与治疗指南(2024年版)
2. NCCN Clinical Practice Guidelines in Oncology-Acute Lymphoblastic Leukemia(2025 Version 2).
3. Kantarjian H, Pui CH, Jabbour E. Acute lymphocytic leukaemia. Lancet. 2025 Aug 30;406(10506):950-962. doi: 10.1016/S0140-6736(25)00864-5.
4. Muffly L, Liang EC, Dolan JG, Pulsipher MA. How I use next-generation sequencing-MRD to plan approach and prevent relapse after HCT for children and adults with ALL. Blood. 2024 Jul 18;144(3):253-261. doi: 10.1182/blood.2023023699.
5. Gocho Y, Yang JJ. Genetic defects in hematopoietic transcription factors and predisposition to acute lymphoblastic leukemia. Blood. 2019 Sep 5;134(10):793-797. doi: 10.1182/blood.2018852400.


