助力DMD/BMD的诊断与治疗,中国研究团队建立“一步式”DMD基因全谱检测方法
- boke
- 2023-12-29
- 5:58 下午
分子遗传学的研究表明,杜氏肌肉营养不良(OMIM:310200)和贝克肌营养不良(OMIM:300376)都是由肌营养不良蛋白基因(dystrophin gene,DMD基因)的突变引起的。在患有DMD或BMD的患者中,有68-70%的突变是DMD基因的单个或多个外显子缺失,8-11%是DMD基因的重复。另外,18-20%的突变是小的突变,包括外显子和内含子的插入、缺失和单核苷酸替换。
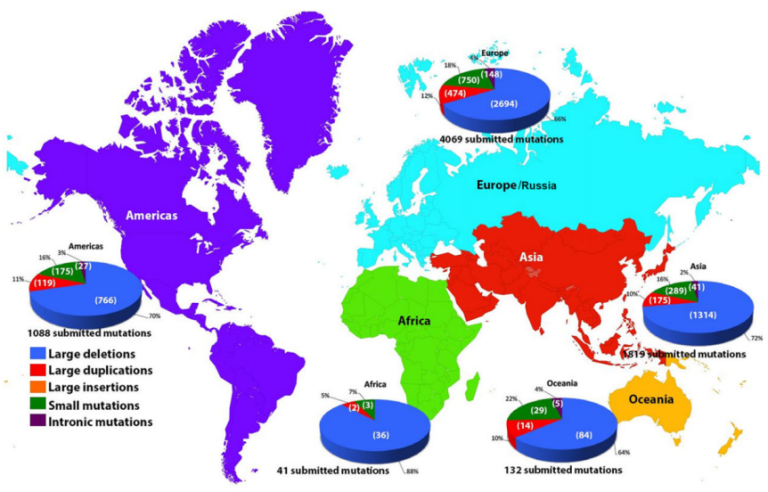
图1. DMD基因不同变异类型占比
对于患有DMD或BMD的患者,已经采用了多种方法进行致病突变检测,但这些方法都有一定的局限性。
MLPA(multiplex ligation-dependent probe amplification)通常用于同时筛查DMD的79个外显子的缺失/重复。然而,因为可能存在探针结合问题,单个外显子缺失仍需要额外验证。另外,MLPA不适用于检测单核苷酸变异(SNV)和小插入缺失。
短读长高通量测序(NGS)技术被广泛应用于检测SNV、微缺失和微重复。根据读数,多数缺失的断点可以被确定;不过,由于读长受限(100-300bp),对于重复或复杂结构变异的准确检测是有一定挑战的。基于纳米通道的下一代mapping技术能够敏感地检测致病结构变异(SV),这些变异可能被PCR技术或染色体微阵列漏检;然而,断点的分辨率受限于内切酶切位点密度。
大约有2-7%的DMD/BMD患者无法通过MLPA或NGS/mapping方法进行诊断。这可能是因为存在深部内含子变异,这些变异包括微插入/缺失、替换,以及大规模的缺失和重复。
研究表明,RNA深度内含子突变可能导致新的剪接位点的产生,从而形成伪外显子。因此,通过对肌肉组织进行RNA分析,利用RT-PCR或短读长测序可作为这些罕见突变的遗传诊断工具。然而,该方法是有创的肌肉活检手术。此外,临床医生通常还需要进一步调查DNA突变情况,以进行基因治疗和产前诊断。
因此,基于基因组DNA,建立一种能够准确获取DMD基因突变类型的全谱检测方法,将有助于DMD/BMD患者的分子诊断和治疗。
长读长测序技术是一种单分子实时测序技术,以Oxford Nanopore Technologies(ONT)和Paci c Biosciences(PB)为代表,并正在不断提高通量并降低成本。与传统方法相比,长读长测序技术在检测结构变异和复杂重排方面提供了更多可能性。此外,通过提高测序深度(超过30x)和HiFi测序技术,也可以准确鉴定SNV和较小的插入缺失。
靶向长读长测序(Gene Panel)被认为是一种高效且成本效益的方法,可用于检测复杂变异。因此,长读序列技术可以作为一种统一的方法来检测DMD基因中所有异质致病突变。近日,中国研究团队开发了一种针对DMD基因的靶向长读长测序技术,可以一次性获取DMD基因不同变异类型,做到全谱分析– Uncovering the true features of dystrophin gene rearrangement and improving the molecular diagnosis of Duchenne and Becker muscular dystrophies,iScience。
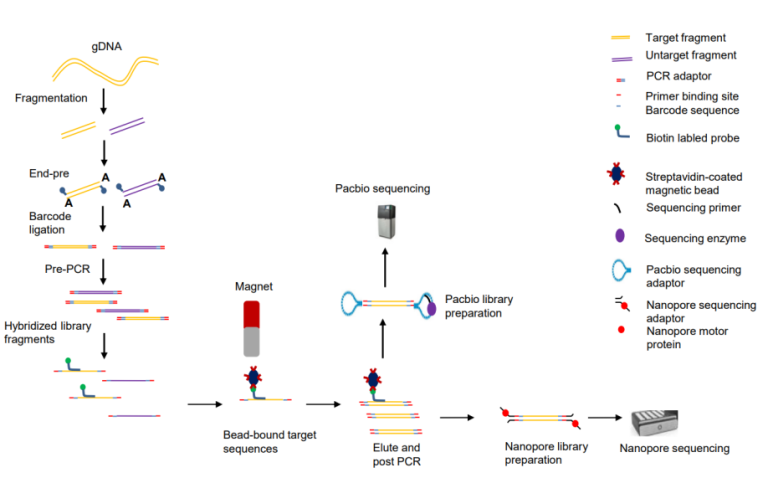
图2. 基于液相基因芯片靶向捕获与长读长测序建立的DMD基因全谱检测方法
研究人员设计了一个DMD基因的全基因Panel,纳入了该基因的所有外显子与内含子,并包括了上下游20Kb的区域(GRCh37/hg19 chrX: 31115345–33377726),该基因的重复序列区域被排除。随后,参照伯科生物靶向捕获实验手册,利用该DMD全基因Panel对129例患有DMD/BMD的受试者进行了遗传测序,并使用ONT和PB平台进行了长读长分析。
129位受试者中,76位为男性DMD,16位为男性BMD,7位男性患有中度型肌营养不良(IMD),2位女性携带者出现症状。另外,还有24位无症状的女性携带者以及4位正常受试者(1位男性、3位女性)。在这个队列中,70名受试者使用ONT平台进行测序,51名使用PB平台,8名采用ONT和PB平台进行平行验证(表S1)。
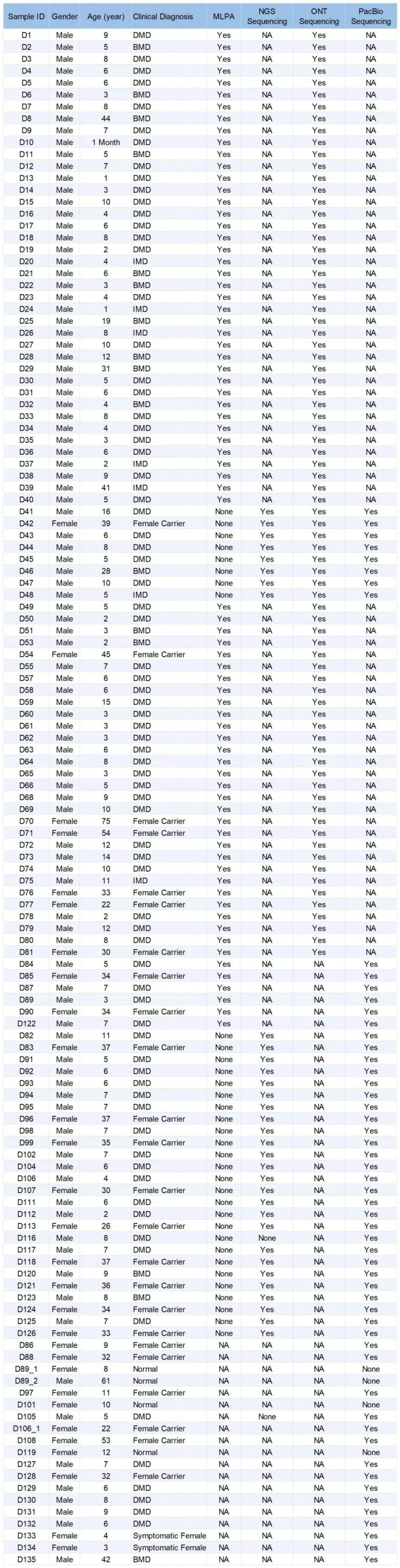
表S1. 129名受试者检测情况(NA:未检测;None:检测但未发现致病变异)
测序数据概述
PB和ONT平均测序数据118,433 和1,261,799 Reads;PB平台的平均读取长度为2,502bp,覆盖96.92%的目标区域,平均测序深度168x。ONT平台的平均读取长度为1,945 bp,覆盖99.99%的目标区域,平均测序深度382x。
靶向长读长测序DMD基因突变更为有效
在这项研究中,通过使用设计良好的DMD全基因Panel,成功准确鉴定并纠正了DMD基因的变异检测,包括之前未能检测到的突变。靶向捕获长读取测序在大规模倒位和易位检测方面具有优势,涵盖的结构变异片段大小范围从11 kb到40 Mb。研究结果显示,与 DMD基因的缺失相比,易位、重复和倒位具有更广泛的改变范围(详见表1和表2)。
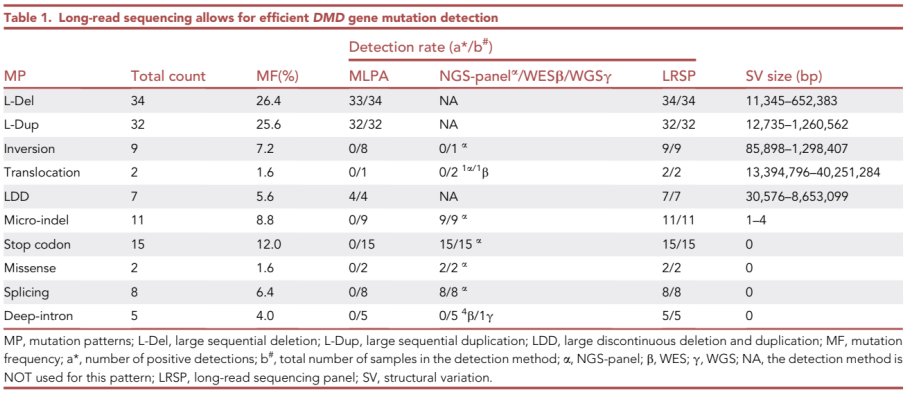
表2. 不同检测方法在DMD不同类型变异检测中的差异
此外,靶向长读长测序还能够检测微小插入缺失和单核苷酸变异,包括深层内含子变异,其准确性在相同的30x测序深度下甚至比短读长测序更高。
在这项研究中,41位患者在DMD基因内出现了单核苷酸变异和小插入缺失。其中,有5位是深层内含子突变,预计会通过影响转录产生剪接位点和伪外显子。肌肉活检RNA-Seq的确认显示,患者 D116 的内含子48(chrX: 31881062–31892406)有一个约11 kb的缺失,会导致产生一个161bp的伪外显子转录(图3)。所有单核苷酸变异均能够通过长读取测序平台被正确鉴定。此外,无义突变和剪接位点突变在单核苷酸变异中更频繁地被检测到(表1)。
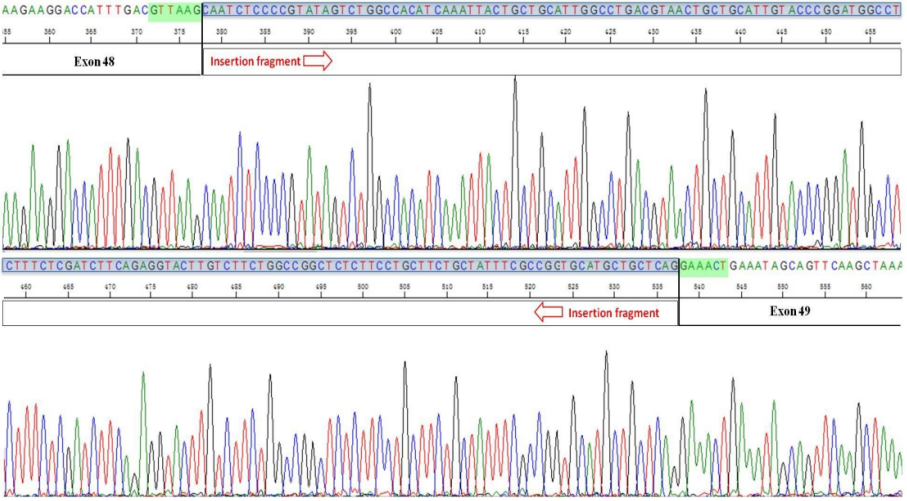
靶向长读长测序提供了更为精确的结构变异细节
使用靶向长读长测序方法对DMD基因进行了研究,发现了84名患者存在重复和/或缺失情况。其中32名具有重复、34名具有缺失、9名发生倒位、2名发生易位,7名出现大片段不连续缺失和重复。根据长读测序结果,确认所有结构变异的断点位于内含子区域,并且大多数含有微插入。少数受试者在断点之间出现大片段(600-1000bp)插入,但顺序连接未受到影响。
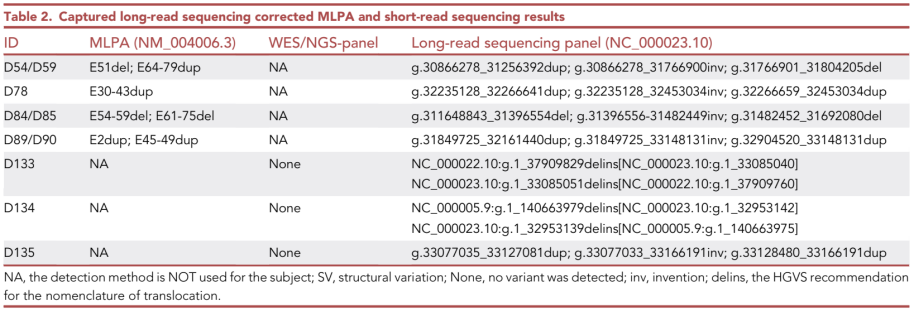
表2. 靶向长读长测序精确揭示结构变异细节
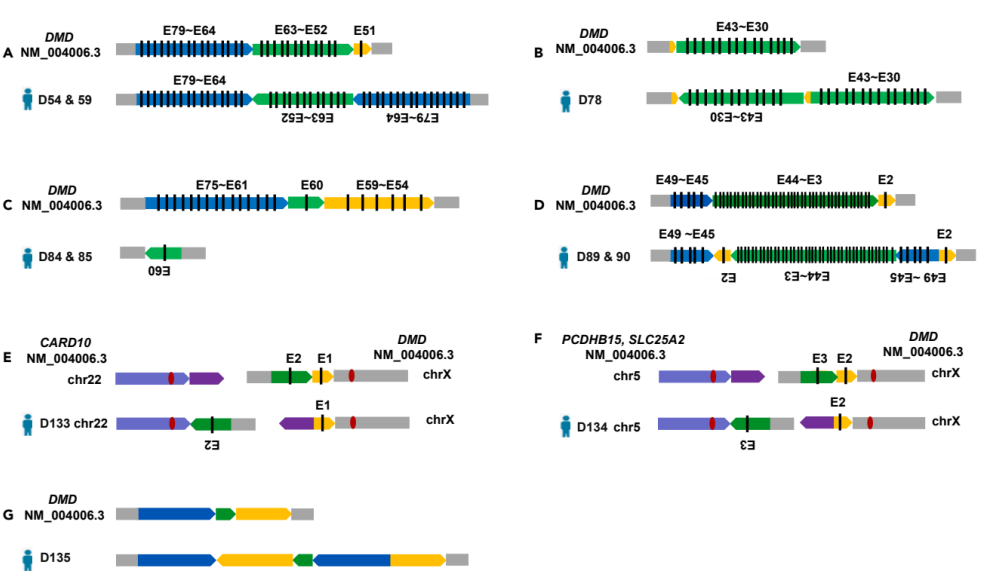
图4. 靶向长读长测序技术准确揭示了DMD基因的结构变异。靶向长读长测序分析揭示,MLPA方法检测到的非连续变异和少量的重复序列,明确是由倒位(A–D)引起的;在涉及DMD基因的常染色体和X染色体之间发现了易位现象(E和F);发生在内含子区域的倒位(G)。
讨论
在这项研究中,研究人员测试了一种DMD基因靶向长读长测序技术的性能,并对129名个体进行了验证。靶向长读长测序展现出了在解码整个DMD重排区域方面的强大能力,超越了传统的方法。特别是发现并非所有的重复都是串联重复,这也直接揭示了DMD中外显子重复的本质。
在30x测序深度下,这种长读长测序Panel能够精确检测微小插入缺失变异和深层内含子单核苷酸变异。研究结果还显示,该方法能够更精确地识别 DMD 基因结构变异的断点位置。
综上所述,本研究开发的DMD全基因靶向“一步式”突变检测平台将加速DMD基因检测过程,从而使诊断更加高效。此外,在治疗DMD/BMD患者时,采用ASO寡核苷酸介导的外显子跳跃以及基因编辑治疗策略也需要准确详细的DMD基因的变异信息,以选择合适的候选靶点。因此,DMD/BMD的寡核苷酸治疗新时代需要更准确的突变检测。本研究采用的靶向长读长测序技术提供了一种高效准确的分子诊断手段,这些发现扩展了我们对DMD基因重排的理解,并为DMD/BMD的诊疗提供了新的思路。
参考资料
1. Ling C, Dai Y, Geng C, Pan S, Quan W, Ding Q, Yang X, Shen D, Tao Q, Li J, Li J, Wang Y, Jiang S, Wang Y, Chen L, Cui L, Wang D. Uncovering the true features of dystrophin gene rearrangement and improving the molecular diagnosis of Duchenne and Becker muscular dystrophies. iScience. 2023 Oct 30;26(12):108365.
2. The TREAT-NMD DMD Global Database: Analysis of More than 7,000 Duchenne Muscular Dystrophy Mutations[J].Human Mutation, 2015, 36(4):395-402.
推荐阅读