个性化定制Panel-RNA
应用背景
基因组DNA层面的检测可以发现基因序列变异,但是只有少数变异与疾病有关,导致肿瘤发生和进展。转录组测序通过检测特定时空状态下的转录本表达量和转录组的变化,对肿瘤的临床检测和预后有重要意义。
伯科定制化RNA捕获芯片TargetCap® RNA-Cap Panel ,是以参考基因组的转录本为模板,采用跨Exon-Exon和Exon边缘覆盖相结合的方式进行探针设计,合成的RNA捕获芯片可以应用于可变剪切、融合基因等的变异检测,也可检测目标转录本的表达量,与肿瘤相关lncRNA的研究。通过目标区域捕获,可以有效检测低表达的转录本,提高转录本覆盖度。
方案推荐
1. 融合基因检测
融合基因检测对临床诊疗和预后均有着重要意义,常作为肿瘤的分子标志物。然而融合位点常发生在具有大量重复区域的内含子上,而重复区域内的探针设计是捕获的难题。
为了增加覆盖密度,CNV Panel (DNA-Cap)加入重复区域探针后,中靶率从70降低至50%;而ROS1的Intron31添加至CDx Panel (DNA-Cap)后,中靶率从60降低至40%,均导致Panel测序成本增加明显。因此,对于DNA-Cap Panel的融合热点的覆盖大多以牺牲融合检出为代价,减少或者直接去掉相应的覆盖区域,再或者是通过反义DNA封闭off-Target区域,但是这些方法均有不足。
相比于在DNA水平检出融合位点,利用RNA-Cap对两个基因外显子连接的融合位点进行基因融合检测是更优的选择。随着RNA测序(RNA-seq)技术的出现,基于RNA生物分子在诊断、预后和治疗各种疾病(包括癌症和传染病)方面的应用前景也越来越广阔。
为更好实现在RNA水平上检测融合基因,伯科依托高通量核酸合成以及自主知识产权的生物素修饰技术,开发商用融合基因检测Panel-Target Cap® Solid Tumor Fusion RNA-Cap Panel。为更精确定位融合位点,伯科专门针对探针进行跨Exon-Exon方式设计,对目标转录本设计多重叠瓦排布探针(图1),显著提高融合检出能力,还可用于检测可变剪切变异以及转录本的表达量等。

RNA捕获对可变剪切、融合基因探针设计示意图
Target Cap® Solid Tumor Fusion RNA-Cap Panel优势
1)较内含子区域更小,成本更低
2)较mRNA-seq对FFPE样本耐受度更高
3)捕获过程进一步去除rRNA污染,有效数据率更高
4)高灵敏度,避免内含子重复区干扰,并应对低表达的融合基因或正常细胞转录本的稀释
5)多基因检测,具有发现新的融合亚型的能力
6)同时检测多基因的“宽度”可以有效节约诊断时间
7)良好的技术拓展性,快速更新迭代,适应临床需求
2. FFPE样品RNA捕获
临床样本通常尺寸有限,在进行病理检测后,往往只留下了FFPE样品。FFPE的RNA质量也通常较低,片段化程度较高,mRNA抽提效率低,影响测序结果准确性,而去核糖体方法又会残留较多含有内含子的未成熟mRNA中间体,导致有效测序数据有限,基于杂交捕获的RNA-Cap技术可以克服上述问题。
|
预文库构建方法
|
样本类型
|
RNA建库投入量
|
杂交方式
|
每个样本预文库投入量
|
杂交时间
|
测序平台
|
测序模式
|
|---|---|---|---|---|---|---|---|
|
总RNA建库,离子打断
|
FFPE RNA
|
500ng
|
3-Plex
|
167ng
|
16h
|
MGI-2000
|
PE100
|
FFPE RNA样本融合基因检测实验参数
对于检测结果能够达到与DNA检测或qPCR一样的效果,且在转录本的均一性、不同区域捕获占比达到相对较高的一致性,具有可靠的稳定性。
|
捕获芯片
|
样本
|
测序数据(Gb)
|
On Target Ratio
|
平均深度
|
平均深度
|
平均深度
|
|---|---|---|---|---|---|---|
|
PET PC 1#
|
CCDC6
|
RET
|
+
|
+
|
+
|
✔
|
|
PET PC 2#
|
KIF5B
|
RET
|
+
|
+
|
+
|
✔
|
|
PET PC 3#
|
KIF5B
|
RET
|
+
|
+
|
+
|
✔
|
融合基因样本检测的捕获效果
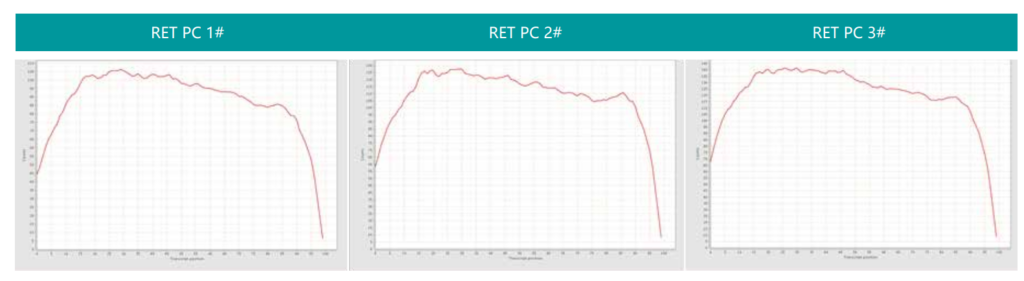
转录本的覆盖均一性
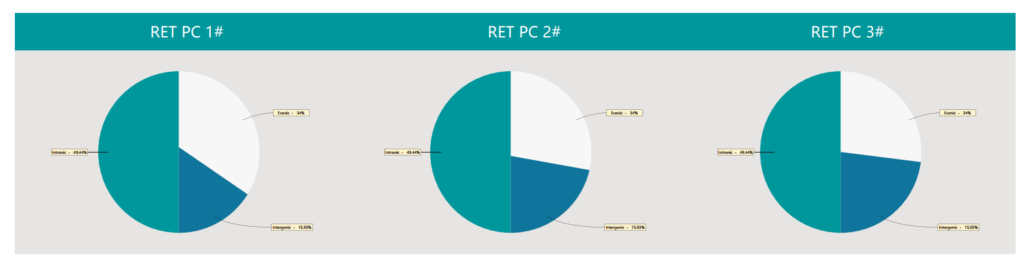
Exon、Intron、Introgenic 占比


