NEJM 孕前或孕早期遗传病基因携带者筛查,不应只关注少数常见病 ACMG第三级筛查或将漏检近50%
- boke
- 2025-03-05
- 2:05 下午

述评:基因携带者筛查—号召全球行动[1]
父母往往要等到孩子被意外诊断出严重的常染色体隐性遗传病,才能意识到自己有生育患病孩子的风险。瑞秋和乔纳森·卡塞拉夫妇就是这样;他们的女儿-麦肯齐被诊断出脊髓性肌萎缩症,并在7个月大时去世。
针对隐性遗传病基因携带者的检测越来越普遍,即使在怀孕之前,也能告知父母生育患有遗传病孩子的风险。
麦肯齐的父母为提高公众意识,并让所有准父母都能进行携带者检测,从而做出明智的生育决定,他们发起了“麦肯齐使命”,呼吁为澳大利亚所有当前怀孕或计划怀孕的父母免费提供遗传病基因携带者筛查,随后,澳大利亚政府拨款2000万澳元用于全国基因携带者筛查项目“麦肯齐使命”。
尽管基因测序技术取得了进步,但全球对建立携带者筛查项目重视程度仍然不足。将携带者筛查纳入产前或孕前保健很困难,因为资源有限,而且非遗传学专业的医护人员缺乏相关知识。此外,与许多国家广泛使用的无创产前检测相比,携带者检测的需求却很低。
尽管如此,全球范围内已启动了一些筛查个人或夫妇生殖风险的倡议,这些倡议超越了针对高危人群的特定基于血统的筛查项目。这些扩展检测大多由商业机构提供,技术进步是驱动力,但筛查范围、项目和疾病种类差异很大,包括一些相对轻微的疾病。然而,这些通常价格不菲的服务,很少有准父母负担得起,这既反映了也加剧了健康差距。
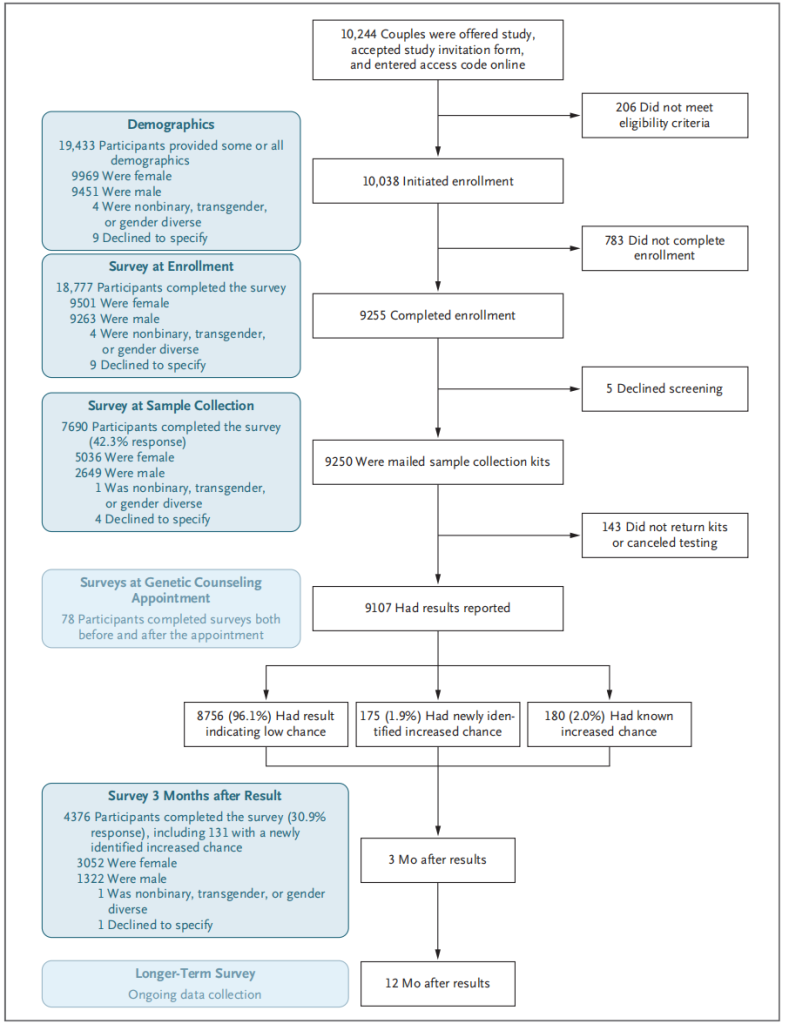
在本期期刊中,Kirk等人的研究报告了“麦肯齐使命”项目的成果,该项目为准父母提供免费携带者筛查,并结合了研究设计。所有关键利益相关者的合作使得建立像这样的大型项目成为可能。尽管经历了新冠疫情,超过9000对夫妇(预计接受率为45.9%)选择接受针对约750种常染色体隐性或X连锁儿童期疾病相关基因变异的筛查。
在接受筛查的夫妇中,1.9%的新发现有增加的生育风险(每次怀孕25%),这比普通人群高。其中一些夫妇在研究前已知家族史或近亲结婚,风险高于常人;若排除这些夫妇,新发现有增加风险的比例为1.5%。在所有发现有增加生育风险的夫妇中,76.6%选择改变生育计划,以避免生育患病孩子,这体现了携带者筛查的临床价值。在筛查时女性未怀孕的夫妇中,比例更高;而对于轻中度疾病和重症疾病风险的夫妇,比例则较低。

澳大利亚全国范围内基于夫妻的遗传病基因携带者筛查[2]
背景
方法
作为“麦肯齐使命”项目的一部分,我们调查了澳大利亚全国性的基于夫妻的遗传病基因携带者筛查项目的可行性、可接受性和结果。医护人员在孕前或孕早期为个人提供筛查。检测结果涵盖了至少1281个基因,并告知了孕育夫妇。我们旨在确定参与者的身心影响、所有参与者的筛查可接受性以及被识别为有较高几率生育患有我们筛查疾病的子女的个人,他们的生育选择。
结果
结论
候选基因选择
生殖遗传携带者筛查旨在让准父母了解他们生育某些常染色体隐性遗传和X连锁遗传病患儿的可能性。我们开发了一个基因列表[3],用于“麦肯齐使命”研究项目,该项目计划将对1万对夫妇进行筛查。
选择基因的标准是: 病情应是致命或致残,在儿童期发病,以便夫妻可能采取措施避免生育受影响的子女;和/或早期诊断和干预将显著改变结果的病情。需要强有力的基因表型关系证据。
候选基因从OMIM和23个商业和已发表的基因列表的审查中确定。基因由16名临床遗传学家使用标准操作程序进行审查,这一过程由一个多学科委员会监督,该委员会包括临床遗传学者、遗传顾问、一名伦理学家、一名患有遗传病儿童的家长以及来自诊断和研究背景的科学家。
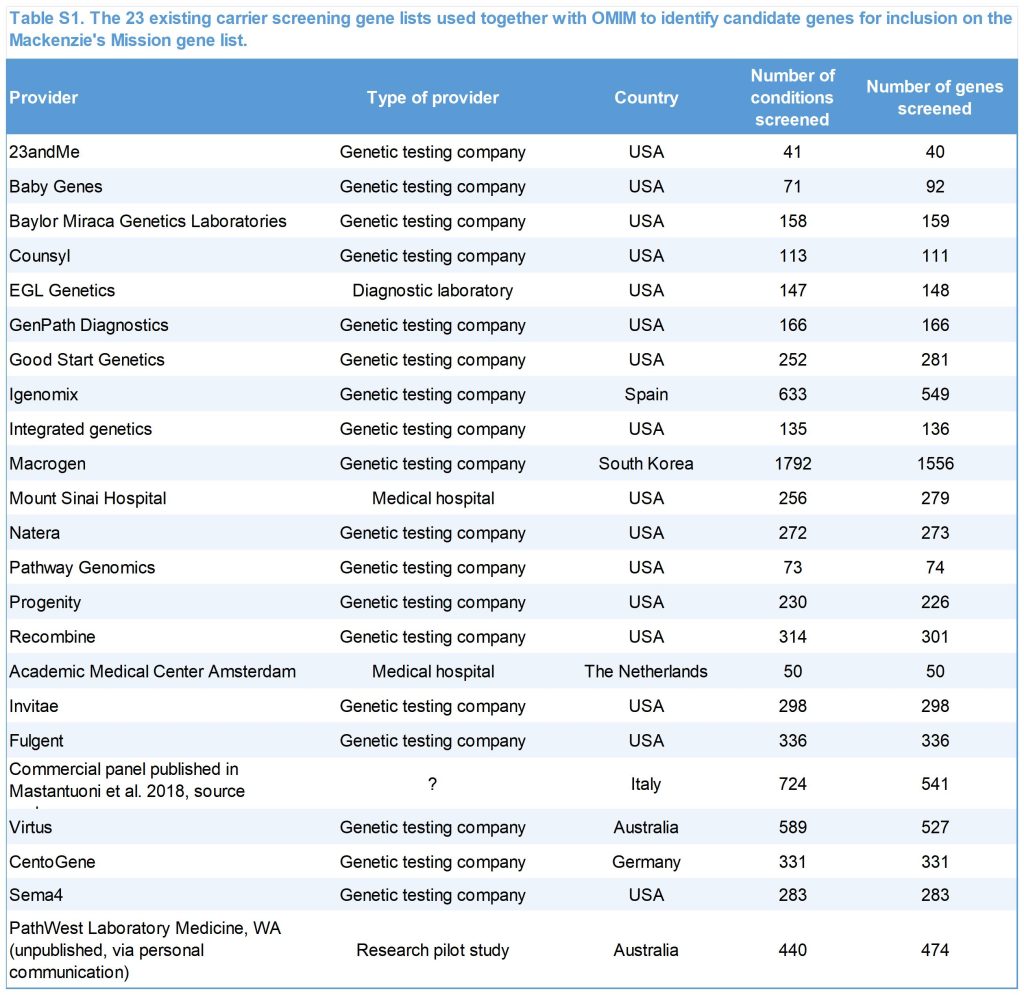
1300个基因符合标准。与非综合征性耳聋和非综合征性的性发育差异相关的基因未被包括在内。我们的经验强调,携带者筛选小组的基因选择需要是一个动态的过程,需要不断的审查和确认。。

美国医学遗传学与基因组学学会 (AmericanCollege of Medical Genetics and Genomics, ACMG) 2021年发布的指南,对携带者筛查的疾病种类进行了分层推荐。一级携带者筛查包括囊性纤维化和脊髓性肌萎缩等2种疾病,以及在风险评估后确定额外的携带者筛查;二级携带者筛查在一级的基础上包括具有严重或中度表型且携带率至少为1/100的疾病,共38种;三级携带者筛查在二级基础上包括了携带率至少为1/200的疾病和X连锁隐性遗传病,共113种;四级携带者筛查在三级的基础上包括了部分携带率小于1/200的疾病。ACMG指南建议所有孕妇和备孕者适合进行三级携带者筛查(113基因)。
在Kirk等人的研究中[1],大约42%的可能生出有缺陷孩子的夫妻,如果只用ACMG 第三级Panel,就检测不出来。该研究数据表明,生殖遗传携带者筛查,不应该只关注少数常见病。

根据我国《孕前及孕早期常见隐性单基因遗传病 携带者筛查临床应用专家共识》[4],推荐适合携带者筛查的疾病应为人群携带率相对较高、青少年期及以前发病、表型严重和/或可提供有效干预措施的常染色体隐性遗传疾病和X连锁遗传疾病。
同时,为了携带者筛查的获益最大化,降低潜在危害,提高临床实用性,提供携带者筛查服务的各机构或实验室应基于实际情况,个性化地确定筛查疾病的数量。

检测方案
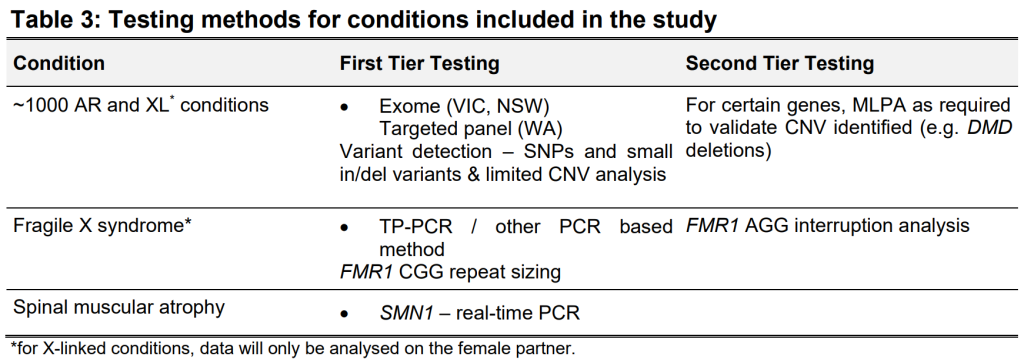
如表3所示,本研究中的基因检测将采用三种方法进行检测。
常染色体隐性和X连锁遗传病(AR and XL conditions):使用NGS技术对~1000个基因进行测序,根据实验室不同,分别采用全外显子Panel和靶向Gene Panel检测。预期检测的变异类型为SNP、小的缺失/插入以及一小部分基因的拷贝数变异,例如DMD和MTM1基因,拷贝数变异是一种常见的变异类型;MLPA用于验证拷贝数变异。
脆性X综合征 (Fragile X syndrome,FXS):FXS是由FMR1基因上游CGG重复单元扩增引起的,55-200个CGG重复的前突变不会导致FXS,但前突变等位基因的女性携带者有可能生育一个完全突变(>200个CGG重复单元)的孩子,从而导致FXS。对于突变结果,可能需要进行第二层分析,以识别CGG重复中的AGG中断。FMR1基因CGG重复中的一个或多个AGG中断与扩展到完全突变的几率较低相关。
脊髓性肌萎缩症(Spinal Muscular Atrophy,SMA):首先使用qPCR方法检测一个伴侣;如果他们有两份或更多的SMN1副本,另一个伴侣将不会被检测。如果被检测的伴侣被发现是携带者(即只携带一份SMN1),则将对第二个伴侣进行检测,以确定这对夫妇生育SMA儿童的可能性是否增加。
伯科全外芯片 – Core Exome Panel v3.0
TargetCap@ Core Exome Panel v3.0基于伯科高品质DNA探针合成技术开发,全流程国产制造,由~40万条探针组成,以GRCh38/hg38人类参考基因组设计,参考Refseq、CCDS、ClinVar等数据库,覆盖19,524个基因,目标区域为33.9Mb。
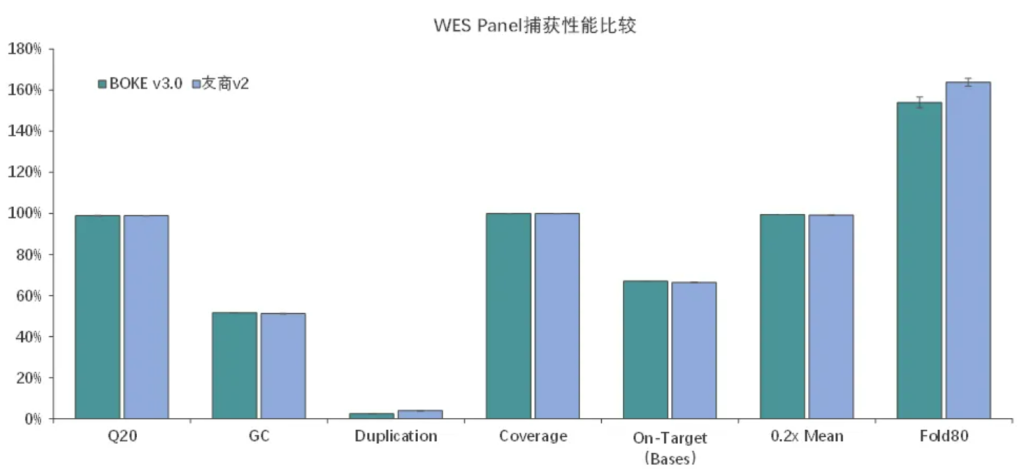
捕获性能比较
伯科全外芯片v3.0性能优异与国外友商同类型产品v2相当,中靶率、覆盖率、覆盖均一性等参数均达到国际领先水平。
适配高通量流程平台

批次稳定
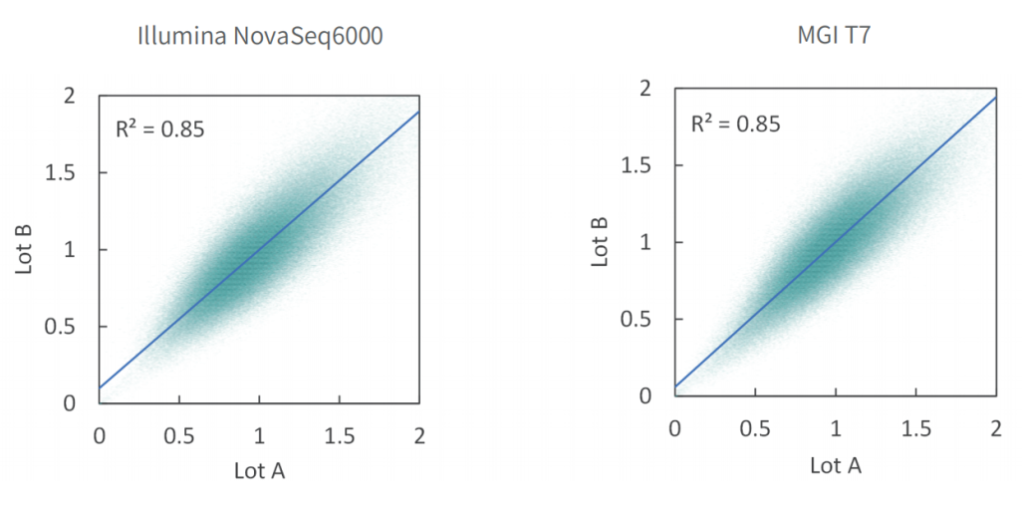
使用不同批次TargetCap® Core Exome Panel v3.0芯片对NA12878 gDNA进行捕获测序,结果显示,不同批次芯片在不同测序平台上均显示出优异的稳定性,不同位点的相对深度相关性高,批次稳定。
变异检测准确
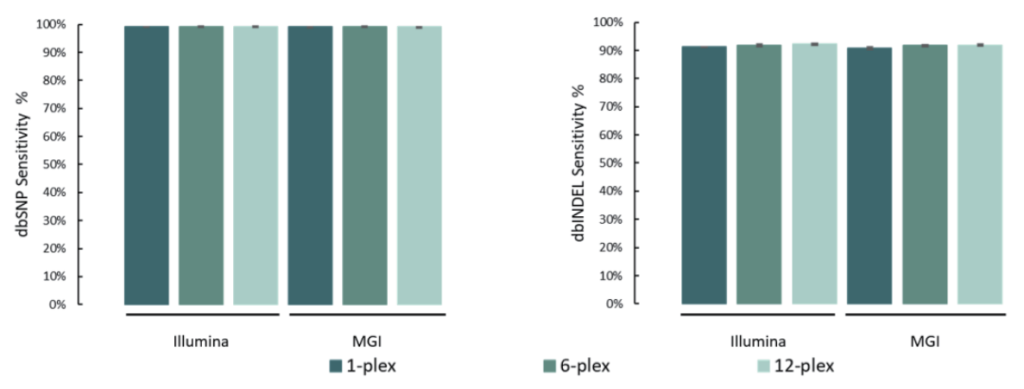
单核苷酸变异(SNV)和插入缺失 (INDEL)是基因组变异的常见形式,也是引起人类疾病的重要原因。
选取NA12878标准品,与预期SNV和INDEL变异进行比较。结果表明,在MGI与Illumina测序平台,SNP灵敏度为99.1%,INDEL灵敏度为91.6%。
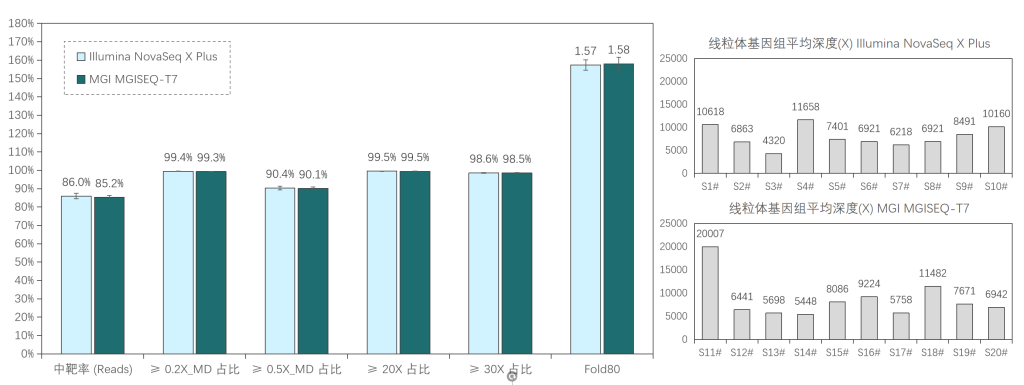
添加线粒体模块临床样本表现
20例全血样本(S1#-S20#),采用1-4 Plex方式使用伯科Core Exome Panel v3.0添加线粒体模块进行过夜杂交捕获;其中,S1#-S10#在Illumina NovaSeq X Plus平台测序, S11#-S20#在MGI MGISEQ-T7平台测序,均采用150PE模式测序。得到测序数据后,抽取8Gb数据进行生信分析。
两种测序平台的数据表现相近,平均深度分别为111x/115x (Illumina/MGI),中靶率优异均> 85%,覆盖均一性极佳(0.2X_MD≥99.3%);仅使用8Gb数据,高达98.5%的捕获区域达到了30X以上,99.5%的捕获区域达到20X以上,为临床样本检测提供了可靠的捕获数据。
参考资料
[1] Henneman L. Genetic Carrier Screening — Call for a Global Mission. N Engl J Med 2024;391:1947-1948
[2] Kirk EP, Delatycki MB, Archibald AD, et al. Nationwide, Couple-Based Genetic Carrier Screening. N Engl J Med 2024;391:1877-1889
[3] Gregg AR, Aarabi M, Klugman S, et al. Screening for autosomal recessive and Xlinked conditions during pregnancy and preconception: a practice resource of the American College of Medical Genetics and Genomics (ACMG). Genet Med 2021; 23: 1793-806.
[4] 孕前及孕早期常见隐性单基因遗传病 携带者筛查临床应用专家共识. 中华围产医学杂志2024年1月第27卷第1期


