JAMA Cardiology 特邀评论 | 揭示克隆性造血与冠心病之间的深刻联系
- boke
- 2024-01-18
- 5:54 下午
2024年1月11日,心脏病研究顶级期刊-JAMA Cardiology在线发表了国家心血管病中心、中国医学科学院阜外医院顾东风院士和鲁向锋教授团队关于中国人群CHIP(潜能不明克隆性造血)相关体细胞基因变异与冠心病发生关系的研究成果[1]。
杂志同期对此项研究进行了特邀评论[2],称本研究填补了克隆性造血相关体细胞基因突变对心血管疾病作用的多个空白,建议通过高深度测序研发相应的遗传风险评估工具,推动冠心病的个体化精准防治。

在先天遗传方面,2022年,国家心血管病中心、中国医学科学院阜外医院顾东风院士和鲁向锋教授团队构建了首个适合中国人群的冠心病多基因风险评分模型(metaPRS),相关成果发表在心脏病研究顶级期刊-European Heart Journal [3],该成果已由伯科生物完成成果转化,正积极助力心脑血管疾病一级预防和该类疾病的全生命周期管理。
在后天基因变异方面,2024年1月11日,心脏病研究顶级期刊-JAMA Cardiology在线发表了国家心血管病中心、中国医学科学院阜外医院顾东风院士和鲁向锋教授团队关于中国人群CHIP(潜能不明克隆性造血)相关体细胞基因变异与冠心病发生关系的研究成果[4]。
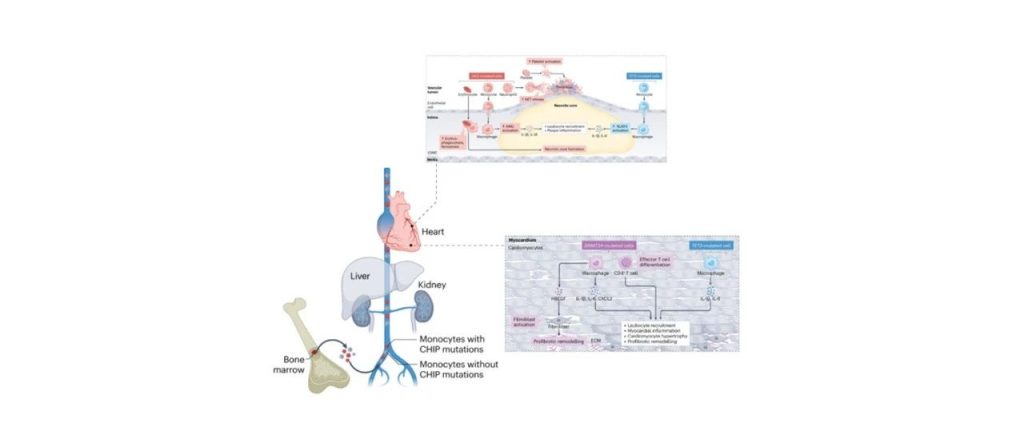
该成果首次解码了中国自然人群CHIP体细胞变异特征谱,发现CHIP体细胞变异携带会显著增加冠心病发生风险,同时,小克隆(VAF<2%)导致冠心病风险升高的作用也是不可忽视;此外,冠心病相关炎症基因可加重或抵消CHIP相关的冠心病风险。克隆性造血,常被称为潜能不明的克隆性造血(CHIP),正在被认识到是动脉粥样硬化心脑血管疾病(ASCVD)的一个重要且独立的风险因素。CHIP的发生源于造血干细胞获得体细胞突变,这些变异为突变细胞提供了竞争优势,导致它们在整个造血系统及其后代中进行克隆扩张,也包括免疫细胞。因此,携带CHIP的个体体内存在大量携带获得性突变的免疫细胞,这种情况可以深刻影响处于动脉粥样硬化病理生理中心的炎症反应。
在本期《美国医学会心脏病学杂志》(JAMA Cardiology)中,研究报告了克隆性造血在一个大型东亚人群中对冠状动脉疾病(CAD)相关事件的影响[1],丰富了我们对这一新兴心脑血管风险因素的理解。
这些参与者在基线时没有心脑血管疾病,作者对中国预测ASCVD风险项目(China-PAR)中的6181名参与者(中位年龄53.8岁;约50%为女性)进行了针对克隆性造血相关90个基因的深度靶向测序。然后,他们探讨了CHIP突变与中位随访期12.2年的CAD事件之间的关联,以及与通过东亚祖源特异性冠心病多基因风险评分(PRS)评估的遗传风险之间的潜在协同作用。
总体而言,这项研究揭示了三个主要发现。首先,携带变异等位基因频率(VAF)大于0.5%的CHIP突变与CAD事件的风险约为1.4倍。其次,CHIP和高PRS对CAD风险产生了类似加成效应,这主要是由CHIP突变和与炎症相关的遗传变异之间的协同互作驱动的。最后,CHIP与循环炎症生物标志物水平的增加相关,特别是白细胞介素6(IL-6),这与以前的研究一致。
这项精心开展的工作增加了克隆性造血作为ASCVD风险因素相关性的证据。它还为炎症作为CHIP和CAD之间联系的媒介提供了额外的支持。这项研究的一个显著优势是使用了一种深度靶向测序策略,与以前将CHIP与ASCVD联系起来的研究相比,提供了更高的检测CHIP突变的灵敏度,即使是降至0.5%的较低VAF限度。
此外,关注东亚人群是值得称赞的,因为这个祖源群体在以前的CHIP/CAD研究中被低估了,因为先前的这些研究主要在白种欧洲族群中进行。由于CHIP的发生率在不同的祖源背景中似乎有所不同,将测序工作扩展到多样性族群对于理解CHIP的更广泛临床意义至关重要。由于该项研究的样本量相对适中,限制了对仅次于最常突变的两个基因的基因特异性分析(DNMT3A和TET2)。在将来,将更大规模的高灵敏度测序数据集放在一起可以进一步了解其他CHIP基因突变对ASCVD相关的影响。
虽然CHIP与心脑血管疾病发生关联已经成为研究热点,但是,我们对于CHIP和CAD之间的关系仍然还是空白,为了充分理解这项研究的价值,有必要对该领域的背景进行介绍。
首先,这也许是最重要的,作者使用的深度靶向测序策略提供了有价值的新见解,即临床相关CHIP突变的克隆大小阈值。以前将CHIP与CAD联系起来的人类遗传学证据是从大型Biobank研究的全外显子测序(WES)数据集中得出的。虽然这种方法加速了该领域的进展,但它对检测低VAF的体细胞突变的灵敏度有限。考虑到这个限制,有大量的证据支持VAF 10%或更高的CHIP与CAD风险增加之间的关联。然而,尚不确定更为普遍的更小的突变克隆,它们是否也能提高CAD风险。在这个背景下,当前研究提供了有力的证据,表明携带VAF大于2%的CHIP突变足以增加CAD风险。此外,它表明,对于某些具有特别强效应的突变基因,如TET2,即使是VAF低至0.5%的突变克隆,在这种情况下也可能具有临床相关性。
这项研究中的另一个有趣的发现是DNMT3A基因突变的显著影响,这些突变与CAD事件风险大约增加40%有关。这一发现与以前基于WES的研究形成对比,这些研究报告白种欧洲人群中DNMT3A突变的影响最小或是几乎没有。考虑到这些研究的样本量足够大,同时测序深度不太可能造成分析差异,因此,可以进一步探究不同人群对DNMT3A突变与CAD风险关系的潜在影响。还有一个值得探索的有趣的可能性是,在携带这个基因突变的个体中,突变克隆大小与CAD风险之间可能存在复杂的关系,也许反映了特定细胞类型的效应和在不同循环白细胞谱系中突变细胞扩张的变化。由于DNMT3A突变是最常见的CHIP突变,理解它们在CAD中的作用对于阐明CHIP的临床意义至关重要。
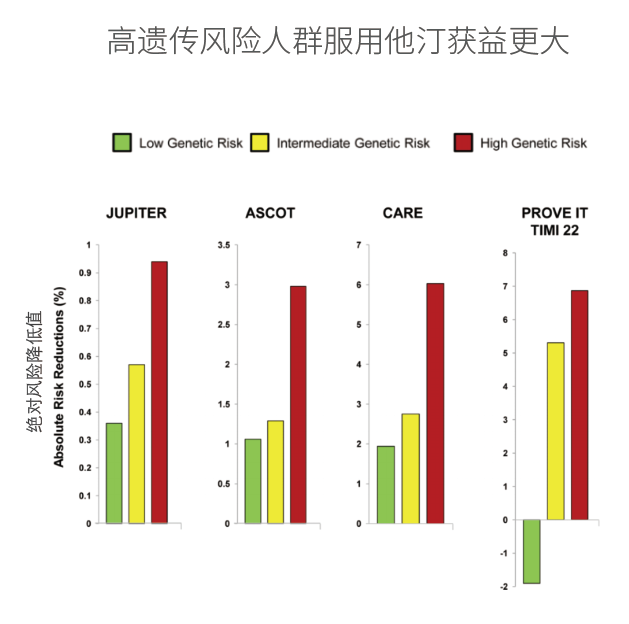
最后,这项研究提供的新见解,将有助于把CHIP相关的认识转化为管理ASCVD风险的个性化策略。在这个背景下,观察到的CHIP与CAD的遗传风险之间的加成关系在这个背景下就具有特别的价值。
同时具有CHIP和高PRS的个体,CAD风险增加至2.2倍以上。相反,在具有低PRS的个体中,CHIP对CAD风险的影响在很大程度上被抑制。这些相互作用主要依赖于炎症相关的遗传变异,支持了抗炎症疗法作为减轻CHIP对ASCVD影响的个性化方法的潜在价值,并提供了相关的遗传学证据。
这些观察结果还支持进一步开发CHIP和先天遗传风险结合的遗传风险评估工具的潜在价值,用于发现CAD或其他心血管疾病的高风险个体。例如,利用该工具对CAD不同风险人群进行精准分层,开展个性化精准医学以减轻CHIP突变携带者的CAD风险。在这个背景下,必须指出的是,以前用于抗炎药物临床试验中的ASCVD炎症风险的常见指标,如C反应蛋白,可能无法准确地发现与CHIP相关的风险,因为本研究[1]还揭示了,只有在VAF大于10%时,CHIP才与C反应蛋白水平升高相关。考虑到这项研究中较小的突变克隆对CAD风险的显著影响,很明显,这个常用的生物标志物无法体现CHIP带来的CAD风险增加。
综上所述,该项重要的研究工作[1]揭示了CHIP与CAD之间的深刻联系,并强调了使用高灵敏度测序技术工具以及评估CHIP在不同人群中的发生率和影响的重要性。
参考资料
1. Zhao K, Shen X, Liu H, et al. Somatic and Germline Variants and Coronary Heart Disease in a Chinese Population[J]. JAMA cardiology, 2024.
2. Fuster J J. Clonal Hematopoiesis and Coronary Artery Disease—A Deep Connection[J]. JAMA cardiology, 2024.
推荐阅读