ESC 2025 | (二)降脂治疗方向重要研究
- boke
- 2025-09-09
- 4:25 下午
一、Bempedoic acid/贝派地酸
一种新型降脂药物,属于ATP 柠檬酸裂解酶(ACL)抑制剂,通过抑制肝脏内胆固醇的合成来降低血液中低密度脂蛋白胆固醇(LDL-C)水平。既往临床随机对照试验已证实,贝派地酸在他汀类药物不耐受人群中不仅可作为替代方案,同时具有明确的心血管获益。
在 ESC 2025 发布的《2025 年 ESC/EAS 血脂异常管理指南重点更新》中,明确将 CLEAR Outcomes(Cholesterol Lowering via Bempedoic Acid, an ACL-Inhibiting Regimen Outcomes trial)结果作为推荐贝派地酸的核心证据:
临床应用:对于无法耐受他汀的患者,贝派地酸可作为降低 LDL-C 和减少心血管事件的选择(IA 类推荐)。
CLEAR Outcomes是一项评估贝派地酸对心血管结局影响的国际多中心随机对照试验。
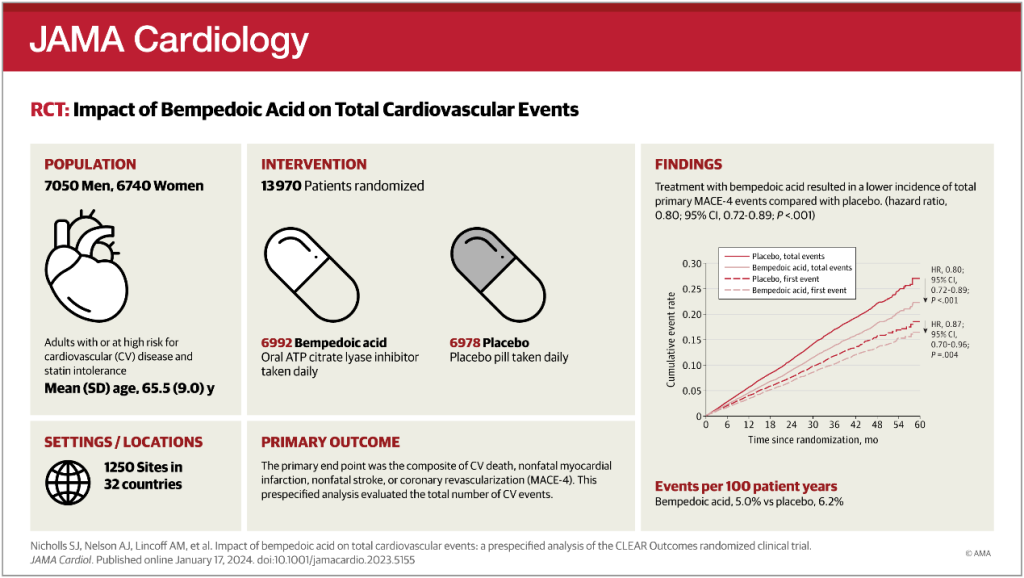
研究设计
纳入的患者需满足以下条件:患有心血管疾病或处于心血管疾病高风险、合并高胆固醇血症,且无法服用指南推荐剂量的他汀类药物。
本研究对 2016 年 12 月至 2022 年 11 月期间的研究数据进行了分析。
将患者随机分配至两组,一组每日服用贝派地酸,另一组每日服用安慰剂。
主要终点为首次发生以下复合事件的时间:心血管死亡、非致死性心肌梗死、非致死性卒中或冠状动脉血运重建,即主要不良心血管事件 – 4(MACE-4)。关键次要终点为首次发生心血管死亡、非致死性心肌梗死及非致死性卒中的时间,即主要不良心血管事件 – 3(MACE-3)。
本预设分析对比了两组(治疗组与安慰剂组)的总心血管事件数量。
研究结果
本研究共纳入 13970 例患者(平均 [标准差] 年龄 65 岁;男性 7230 例,占 51.8%)。其中,9764 例受试者(69.9%)既往患有动脉粥样硬化性心血管疾病,基线低密度脂蛋白胆固醇(LDL-C)水平为 139mg/dL;治疗 6 个月时,贝派地酸治疗使患者的 LDL-C 水平降低 21%,高敏 C 反应蛋白(hsCRP)水平降低 22%。中位随访时间为 3.4 年(四分位距 3.1-3.9 年)。
研究期间共记录到 1746 例确诊的首次MACE-4事件,以及 612 例患者中额外发生的 915 例 MACE 事件。其中,冠状动脉血运重建在首次事件中占比 32.8%(1746 例中占 573 例),在额外事件中占比 69.4%(915 例中占 635 例)。
就总心血管事件发生率而言,贝派地酸治疗与以下事件的风险降低相关:
MACE-4:HR=0.80,95% CI 0.72-0.89,P<0.001;
MACE-3:HR=0.83,95% CI 0.73-0.93,P=0.002;
心肌梗死:HR=0.69,95% CI 0.58-0.83,P<0.001;
冠状动脉血运重建:HR=0.78,95% CI 0.68-0.89,P<0.001;
卒中方面:未观察到统计学显著差异(HR=0.80,95% CI 0.63-1.03)。
随着患者发生 MACE 事件的次数增加,观察到贝派地酸的保护作用对应的风险比(HR)更低。
研究结论
通过贝派地酸降低低密度脂蛋白胆固醇(LDL-C)水平,可减少 “高心血管风险、他汀类药物治疗不耐受且低密度脂蛋白胆固醇(LDL-C)水平升高” 患者的总心血管事件数量。
二、Olezarsen/TRYNGOLZA
APOC3 作为甘油三酯调控的重要靶点,近年来备受关注。一种针对 APOC3 的变构寡核苷酸药物——Olezarsen,该药物以核苷酸结构为基础,Olezarsen 靶向载脂蛋白 C-III 的 mRNA,抑制甘油三酯清除,显示出良好的生物活性。临床研究表明,该药物能够显著降低甘油三酯水平,为现有治疗方案提供有效补充。
在小型 II 期试验和甘油三酯水平非常高的患者中,Olezarsen 已被证明可以降低甘油三酯水平。研究者在 ESSENCE-TIMI 73b 试验中研究了 Olezarsen 在 ASCVD 高风险的中度高甘油三酯血症患者中的疗效和安全性。

Olezarsen reduces levels of the blood fat, triglycerides, in patients at high cardiovascular risk
关键要点
尽管采用了最佳降脂疗法,但仍存在对降低残留心血管风险患者的甘油三酯水平的有效疗法的需求尚未得到满足。
ESSENCE-TIMI 73b试验研究了载脂蛋白C-III RNA靶向药物Olezarsen在中度高甘油三酯血症和心血管风险升高患者中的疗效和安全性。
与安慰剂相比,每月注射 Olezarsen 在 6 个月时可显着降低甘油三酯水平约 60%,超过 80% 的患者在 12 个月时使用 Olezarsen 达到正常甘油三酯水平。
研究内容
入组情况:安慰剂对照、双盲 III 期 ESSENCE-TIMI 73b 试验在北美和欧洲的 160 个地点进行。该试验纳入了中度高甘油三酯血症(甘油三酯 150−499 mg/dL)和心血管风险升高的成年患者,这些患者因确诊为 ASCVD 或 2 型糖尿病导致 ASCVD 风险增加,年龄为 ≥55 岁。预计患者在入组时将接受优化的稳定低密度脂蛋白胆固醇 (LDL-C) 降低治疗。ESSENCE-TIMI 73b试验还纳入了严重高甘油三酯血症(甘油三酯≥500mg/dL)患者。主要分析队列是中度高甘油三酯血症患者,因为重度高甘油三酯血症患者正在专门的单独试验中进行研究。
分析方法:包括 1,349 名中度高甘油三酯血症和心血管风险升高的患者,他们被随机分配至每 4 周皮下注射一次 Olezarsen 50 mg (n=254)、Olezarsen 80 mg (n=766) 或安慰剂组 (n=329),持续 12 个月。主要终点是与安慰剂组相比,6个月时甘油三酯水平相对于基线的百分比变化。主要分析人群的中位年龄为 64 岁,其中 40% 是女性。基线时甘油三酯水平中位为 238.5 mg/dL。
研究结果
在6个月时,Olezarsen显着降低了甘油三酯水平:安慰剂调整后的相对于基线变化百分比的最小二乘平均差异为Olezarsen 50mg的-58.4个百分点,Olezarsen 80mg的最小二乘平均差异为-60.6个百分点(均为p<0.001与安慰剂)。
在安慰剂组中,12.5% 的患者在 6 个月时甘油三酯水平为 <150 mg/dL,而 Olezarsen 50 mg 的患者为 85.0%,Olezarsen 80 mg 的患者为 88.7%(两者均为 p<0.001)。在 12 个月时,安慰剂组、Olezarsen 50 mg 和 Olezarsen 80 mg 的比例分别为 20.6%、82.8% 和 85.0%(与安慰剂相比,两者的比例分别为 <0.001)。Olezarsen 显着降低了其他脂蛋白(残余胆固醇、非高密度脂蛋白胆固醇和载脂蛋白 B)的水平,对 LDL-C 没有显着影响。
严重不良事件的发生率相似:Olezarsen 50 mg 组为 9%,Olezarsen 80 mg 组为 14%,安慰剂组为 11%。Olezarsen 50 mg (34.2%) 和 Olezarsen 80 mg (38.3%) 的肝转氨酶升高至任何程度高于正常范围上限的比例比安慰剂组 (17.6%) 更常见(均为 p<0.001);然而,具有临床意义的增加很少见,并且在各组之间相似。
研究总结
在中度高甘油三酯血症和心血管风险升高的人群中,每月服用 Olezarsen 导致甘油三酯大幅降低,高于目前可用疗法的预期,超过 80% 接受 Olezarsen 治疗的患者达到正常甘油三酯水平。
三、Inclisiran
近年来,PCSK9 抑制剂的应用已积累了丰富的临床经验,并伴随大量循证证据的发布。无论是单克隆抗体还是小干扰 RNA,其适用人群范围可能在新版指南中进一步放宽。例如,长效制剂Inclisiran有望被推荐用于依从性较差的人群,以提高 LDL-C 达标率并降低复合心血管事件风险。总体而言,PCSK9 抑制剂的推荐时机可能前移,覆盖人群也将进一步扩大。
VICTORION-Difference 研究的目的是比较 Inclisiran与安慰剂,除了单独优化的降脂疗法之外,在反映现实世界实践的人群中实现 LDL-C 目标以及与肌肉相关不良事件和疼痛相关生活质量 (QoL) 相关的新终点。
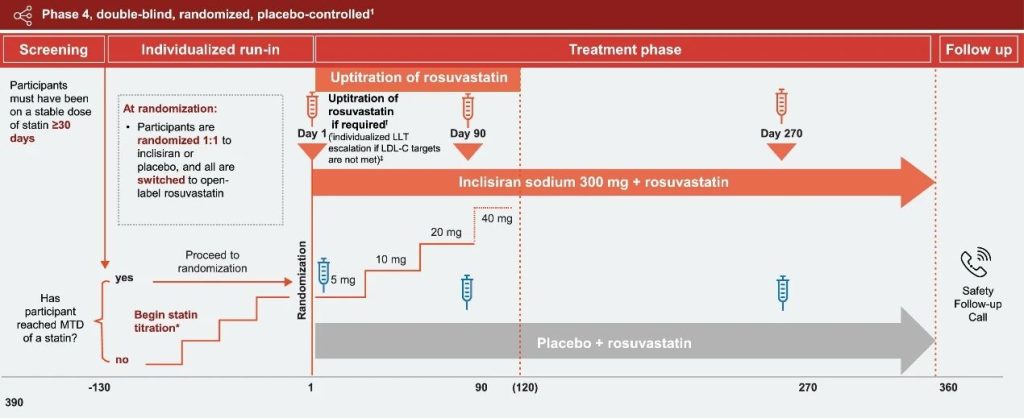
Early and sustained LDL-C goal achievement with Inclisiran in patients at high cardiovascular risk
关键要点
许多心血管事件高危患者无法通过可用的降脂疗法达到指南推荐的低密度脂蛋白胆固醇 (LDL-C) 目标。
VICTORION-Difference试验评估了每3-6个月皮下注射一次Inclisiran与安慰剂组相比,在心血管事件高/极高风险的高胆固醇血症患者中,在个体优化降脂治疗的基础上,疗效、安全性和生活质量结局。
与安慰剂相比,Inclisiran使更多患者达到早期和持续的LDL-C目标,不良肌肉事件明显减少,提供了一种可能有助于解决当前在LDL-C目标实现方面的差距的治疗策略。
研究内容
入组情况:双盲、安慰剂对照、随机 IV 期试验在133 个中心进行。根据 2019 年欧洲心脏病学会/欧洲动脉粥样硬化学会指南,符合条件的患者处于高或极高的 CV 风险尽管接受了个体化最大耐受他汀类药物剂量的治疗,但 LDL-C 升高。受试者以 1:1 的比例随机接受皮下注射 Inclisiran sodium 300 mg(相当于 284 mg Inclisiran)或安慰剂。除了 Inclisiran/安慰剂外,如果未达到个体 LDL-C 目标,则将开放标签Rosuvastatin(起始剂量为 5 mg/天或 10 mg/天)依次最佳滴定至最大耐受剂量。主要终点是在第 90 天达到 2019 年指南推荐的个人 LDL-C 目标(极高 CV 风险:<55 mg/dl [<1.4 mmol/l];高 CV 风险:<70 mg/dl [<1.8 mmol/l])3 的参与者比例。
共有 1,770 名个体被随机分配,平均年龄为 63.7 岁,其中 30.2% 为女性。大多数参与者 (92.3%) 被归类为具有非常高的 CV 风险。
主要终点,与标准治疗组相比,在90天时达到其个人指南推荐的LDL-C目标的受试者比例显著更高(84.9% vs. 31.0%;比值比[OR] 12.09;95%置信区间[CI] 9.59-15.24;p<0.0001)。
研究结果
在 Inclisiran 组和标准护理组中,从基线到第 360 天 LDL-C 降低的时间平均百分比分别为 -59.45% 和 -24.31%(最小二乘平均治疗差异 35.14%;p<0.0001)。
与标准护理组相比,在Inclisiran组中,经历肌肉相关不良事件的受试者较少(11.9% vs. 19.2%;p<0.0001)。此外,使用简短简要疼痛量表,与标准护理相比,疼痛相关严重程度(-0.11;p=0.0389)和干扰评分(-0.11;p=0.0285)的数值平均时间减少幅度更大,但未达到统计学意义。
治疗中出现的不良事件发生率在 Inclisiran 组和标准护理组之间具有可比性(分别为 71.3% 和 75.9%)。
研究结论
这项大型研究表明,与当前的常规护理相比,基于 Inclisiran 的治疗策略在使患者达到早期和持续的 LDL-C 目标方面具有有效性,并且不良肌肉症状显着减少。这些发现表明,对于目前对其他降脂疗法反应不佳的大量高危患者来说,Inclisiran是一种方便、有效和耐受性良好的治疗选择。
此外,MONO China 研究聚焦于 PCSK9 抑制剂单药治疗在中国人群中的应用。尽管现行指南仍将他汀作为治疗基石,但随着美国 FDA 批准Inclisiran在一级预防人群中的适应证,该药在中国也开展了针对一级预防人群的单药治疗研究。该研究旨在评估其在中国患者中对 LDL-C 的管理效果、安全性及依从性。
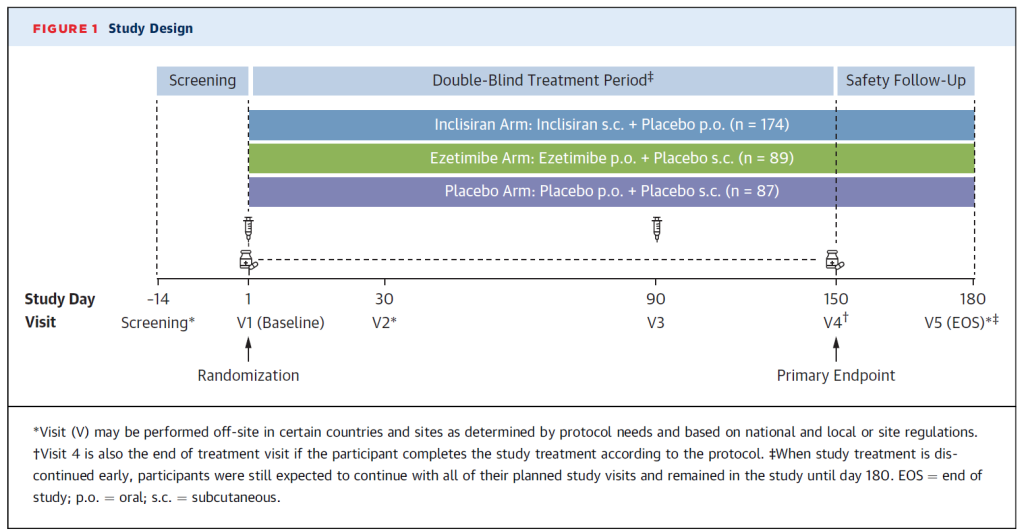
VICTORION-Mono China: efficacy and safety of Inclisiran as monotherapy in Chinese adults with low or moderate ASCVD risk and elevated LDL-C
研究目的
评价Inclisiran单药在低/中危ASCVD、LDL-C升高且未接受降脂治疗的中国成人患者中的疗效和安全性。
研究方法
入组情况:本项多中心、两部分的3期临床随机试验包括6个月的双盲、安慰剂对照治疗期和6个月的开放标签期。纳入年龄在18-75岁,根据中国指南具有低/中危ASCVD风险,筛查时空腹190 mg/dL>LDL-C≥130 mg/dL,且未接受降脂治疗的中国患者,按1:1随机分组,接受Inclisiran钠300 mg(Inclisiran 284 mg)或安慰剂。
主要目的是评估Inclisiran与安慰剂对LDL-C从基线到150天的平均百分比变化。次要目标包括在第150天LDL-C的绝对变化和其他致动脉粥样硬化脂质和PCSK9的百分比变化;第330天LDL-C变化百分比;以及Inclisiran的安全性和耐受性。
研究结果
共207名参与者被随机分配接受Inclisiran(n=103)或安慰剂(n=104)治疗。平均年龄47.9岁,58.5%为女性,平均基线LDL-C为149.9 mg/dL(表1)。
有167例患者(80.7%)为低危ASCVD风险,37例(17.9%)为中危ASCVD风险。Inclisiran治疗达到了主要终点:从基线到第150天,经安慰剂校正后LDL-C的平均百分比变化为-47.50%(95% CI: – 52.35, – 42.65, p<0.0001)。LDL-C降低在第30天明显,并持续到第360天(图)。在第150天,经安慰剂校正的LDL-C绝对变化为-69.73 mg/dL(95% CI: -76.60, -62.86; p<0.0001)。在第150天,Inclisiran还降低了PCSK9(- 77.83%)、总胆固醇(-31.49%)、非HDL-C(-40.57%)和ApoB(-36.84%)(p均<0.0001)。
在第330天,Inclisiran组LDL-C的平均百分比变化为-45.45%(95% CI: -48.57, -42.34)。在双盲期间,Inclisiran组和安慰剂组的不良事件发生率相似,分别为70.9%(73/103)和67.3%(70/104)。
治疗相关不良事件在Inclisiran组(13.6%)比安慰剂组(3.8%)更频繁,但都不严重。没有发现新的安全事件。
研究结论
在中国患者中,Inclisiran单药治疗耐受性良好,可持续有效降低LDL-C和其他促动脉粥样硬化性脂质,使其成为ASCVD风险患者的潜在有效治疗选择。
CHOLINET(CHOLesterol Italian Inclisiran NETwork)研究是一个意大利多中心前瞻性4期注册研究,在意大利44个中心进行,旨在评估Inclisiran治疗的有效性、安全性、依从性和持久性。
Efficacy and safety of inclisiran in patients with and without type 2 diabetes mellitus: a subgroup analysis from the CHOLINET Registry
研究目的
该亚组分析的目的是评估LDL-C从基线的百分比变化和达到LDL-C目标的患者比例,根据心血管风险等级,根据是否存在T2DM进行分层。
研究方法
根据标准临床实践,CHOLINET登记了接受Inclisiran治疗的患者。临床和人口学特征,伴随治疗,血液化学,记录在第一次处方时和随后的随访。根据是否存在T2DM进行分层分析。
研究结果
该亚组分析纳入了在CHOLINET登记的659例患者(20%为T2DM,69%为男性,平均年龄63岁)。其中529例患者达到3个月里程碑,其中513例(97%)接受了第二次剂量,178例患者达到9个月里程碑,其中171例(96%)接受了第三次剂量。3个月随访时T2DM患者为110例(21.4%),9个月随访时为38例(22.2%)。T2DM患者从基线到3个月LDL-C降低的中位数百分比为56.2%,而无T2DM患者为50% (p=0.015),T2DM患者从基线到9个月LDL-C降低的中位数百分比为69.5%,而无T2DM患者为51.4%(p=0.005)。此外,在随访3个月评估的患者中,65.5%的T2DM患者达到了LDL-C目标,而非T2DM组为55.3%。同样,在9个月的随访中,81.6%的T2DM患者达到了LDL-C目标,而无T2DM患者为60.9%(p=0.03)。
研究结论
来自CHOLINET登记研究的亚组分析证实了Inclisiran在降低LDL-C方面的有效性,在T2DM患者中具有更大的LDL-C降幅和更高的LDL-C目标达成。这些发现强调了Inclisiran在优化T2DM患者脂质管理中的潜在作用,并且可以部分解释为脱唾液酸糖蛋白受体的调节,该受体负责将Inclisiran摄取到肝细胞。
Efficacy of inclisiran in patients affected by familial hypercholesterolemia: data from CHOLINET Registry
研究目的
本研究的目的是评估Inclisiran对伴有和不伴有FH的患者的疗效。
研究方法
根据标准临床实践,CHOLINET登记了Inclisiran治疗的患者。临床和人口学特征,伴随治疗,血液化学,记录在第一次处方时和随后的随访。根据是否存在FH对分析进行分层。FH的诊断采用荷兰脂质临床网络评分(DLCNS)。
研究结果
该亚组分析纳入了513名在CHOLINET注册登记的患者,他们至少接受了3个月的剂量。其中78例(15.2%)为FH。基线时,FH患者的中位LDL-C为160 mg/dL,无FH患者的中位LDL-C为100 mg/dL。无FH患者接受其他降脂治疗(LLT)的患者比例高于FH患者(89.2% vs 74.4%)。在3个月的随访中,FH患者的中位LDL-C百分比降低显著低于无FH患者(46.3% vs 53.3%, p<0.001);同样,FH患者达到对应CV风险等级LDL-C目标的患者比例显著降低(24.4% vs 63.4%, p<0.001)。同样,在完成9个月随访的171例患者中,27例FH患者的中位LDL-C百分比降低显著低于144例无FH患者(47.6% vs 40.5%, p=0.004)。此外,在9个月的随访中,22.2%的FH患者达到了LDL-C目标,而没有FH的患者为73.6% (p<0.001)。在多变量分析中,FH (OR: 0.47; 95% CI: 0.23-0.95; p=0.036)是未能达到LDL-C目标的预测因子。
研究结论
FH可能涉及更多的病理生理机制,如基因型、LDL-C受体残留功能和多重突变,这可能解释了FH患者对Inclisiran反应的变异性。然而,需要进一步的研究来更好地描述FH患者的特征,并了解该人群中LDL-C降低的高个体差异的原因。
四、Obicetrapib
Obicetrapib(Obi)是一种新型胆固醇酯转移蛋白(CETP)抑制剂。
在Broadway(纳入 2500 余名高心血管风险人群)和Brooklyn(纳入 354 例杂合子家族性高胆固醇血症(HeFH)患者)这两项研究中,研究者进行了为期 12 个月的数据跟踪及分析,在 “虽接受他汀治疗但低密度脂蛋白胆固醇(LDL-C)仍升高” 的患者中,比较了 10mg Obicetrapib与安慰剂的疗效。结果均显示Obicetrapib可降低ASCVD或HeFH患者的LDL-C。但目前尚不清楚Obi的疗效是否会因背景降脂治疗(LLT)的类型和强度而异。

ESC 25: Pooled MACE Data for Obicetrapib
研究方法
对Broadway和Brooklyn试验进行预先指定的汇总分析,这两项试验将ASCVD或HeFH和LDL-C升高(尽管接受最大耐受LLT)的参与者随机分配到Obi 10mg,每日一次或安慰剂(Pb),随访1年。
主要终点是安慰剂校正后84天LDL-C较基线的变化,次要终点是载脂蛋白B(ApoB)和非HDL-C的变化。在这项分析中,根据他汀类药物的使用、强度(高、中/低)、依折麦布和PCSK9i以及联合治疗(定义为任意两类药物)的二元状态(是/否)对患者进行分层。
研究结果
研究共纳入2778名参与者,平均年龄64岁,女性占36.1%,HeFH患者占26.5%。平均基线LDL-C为2.66 mmol/L,ApoB为93.4 mg/dL,非HDL-C为3.30 mmol/L。
基线时,分别有69.3%和21.7%的患者服用高或中/低强度他汀类药物,9.0%的患者不服用他汀类药物。依折麦布使用率为29.9%,PCSK9i使用率为5.4%。联合治疗占28.3%,单药治疗占68.0%,未接受LLT者占3.6%。
Obi组经安慰剂校正的LDL-C总体降低了34.9% (CI:37.5,32.3),并且在不同背景LLT中始终优于Pb组。与Pb相比,Obi在不同LLT背景下均能观察到对ApoB(中图)和非HDL-C(右图)的一致获益。
研究结论
在极高危和高危的ASCVD或HeFH患者中,不管背景LLT如何,Obicetrapib均可以显著降低LDL-C和其他致动脉粥样硬化性脂质。对于LDL-C仍然不受控制的患者,Obicetrapib可作为现有LLT的一种潜在辅助疗法。
五、BW-00112
BW-00112 是一种全合成、化学优化的双链 ANGPTL3 小干扰 RNA(siRNA),通过与 N – 乙酰半乳糖胺(GalNAc)偶联实现靶向递送。这种创新疗法有望满足血脂异常管理中尚未被满足的临床需求。研究显示,该类药物不仅能够显著降低胆固醇水平,同时对甘油三酯也具有良好的降幅,其最大优势在于混合型高脂血症的治疗。

BW-00112 targeting ANGPTL3 results in prolonged reductions in plasma triglycerides, LDL-C, and remnant-C in Chinese healthy subjects
研究目的
本研究的主要目的是评估100 mg/dL ≤ LDL-C < 190 mg/dL和100 mg/dL ≤ TG <500 mg/dL的中国健康受试者接受单剂量BW-00112治疗12周的安全性和耐受性。本研究的次要目的是表征单剂量BW-00112治疗12周的药代动力学(PK)特征和评估药效学(PD)效应(ANGPTL3,TG, LDL-C,非HDL-C)。
研究方法
这是一项1期、随机、双盲、安慰剂对照的单剂量研究,旨在评估中国健康受试者(LDL-C升高且未接受降脂治疗)接受单剂量BW-00112皮下治疗的安全性、耐受性、PK和PD。
研究结果
BW-00112在中国健康受试者中单次皮下给药耐受性良好,剂量范围从150 ~ 600 mg。没有严重的不良事件,也没有因治疗不良事件(TEAEs)导致的死亡或研究中断。大多数TEAEs的严重程度较轻。特别关注的不良事件,包括注射部位反应和肝功能异常,没有引起安全性担忧。暴露量(AUC0-last和Cmax)在150~600 mg的线性范围内呈剂量依赖性增加。然而,增加幅度略大于剂量比例。BW-00112在给药12周后,150~600 mg剂量的ANGPTL3水平显著降低(平均-76%至-89%)。150~600 mg剂量的BW-00112也可使TG(平均-62%至-76%)、LDL-C(平均-31%至-34%)、ApoB(平均-26%至-31%)、非HDL-C(平均-32%至-36%)和RC(平均-38%至-41%)降低。
研究结论
BW-00112 150~600 mg单次皮下注射时,耐受性一般良好。单次皮下剂量BW-00112在150~600 mg范围内观察到大量PD效应,包括ANGPTL3、TG、LDL-C、ApoB、非HDL-C和RC的降低。澳大利亚和中国健康受试者在安全性、PK和PD方面无明显差异。
参考资料:
1.Stephen J. Nicholls, et al. Impact of Bempedoic Acid on Total Cardiovascular Events:A Prespecified Analysis of the CLEAR Outcomes Randomized Clinical Trial. JAMA Cardiol. 2024;9;(3):245-253. doi:10.1001/jamacardio.2023.5155
2.KARDIA-3: Zilebesiran as add-on therapy in adults with hypertension and established cardiovascular disease or at high cardiovascular risk’ presented during HOT LINE 4 on 30 August 2025 at 16:30 to 16:40 in Madrid (Main Auditorium).
3.Olezarsen in patients with hypertriglyceridemia at high cardiovascular risk: the Essence-TIMI 73b trial’presented during HOT LINE 4 on 30 August 2025 at 16:45 to 16:55 in Madrid (Main Auditorium) and simultaneously published in New England Journal of Medicine.
4.VICTORION-Difference study: Inclisiran-based strategy vs standard of care’presented during HOT LINE 4 on 30 August 2025 at 17:00 to 17:10 in Madrid (Main Auditorium).
5.Ulf Landmesser, et al. Design and rationale of the VICTORION-Difference study: A phase 4 randomized, double-blind, placebo-controlled clinical trial to assess inclisiran’s early efficacy, safety, tolerability, as well as its impact on quality of life in individuals with hypercholesterolemia. American Heart Journal. Volume 289, November 2025, Pages 117-126.
6.Pam R. Taub, et al. Safety and Lipid-Lowering Efficacy of Inclisiran Monotherapy in Patients Without ASCVD: The VICTORION-Mono Randomized Clinical Trial. JACC Journals. Vol. 86 No. 3.
7.Stephen J Nicholls, et al. Impact of Obicetrapib on Major Adverse Cardiovascular Events in High-Risk Patients: A Pooled Analysis. J Am Coll Cardiol. 2025 Aug 20:S0735-1097(25)07383-8. doi: 10.1016/j.jacc.2025.07.056. Online ahead of print.
8.Stephen J Nicholls, et al. Safety and Efficacy of Obicetrapib in Patients at High Cardiovascular Risk. N Engl J Med. 2025 Jul 3;393(1):51-61.doi: 10.1056/NEJMoa2415820. Epub 2025 May 7.
9.Emir Redzepagic, et al. BW-00112 targeting ANGPTL3 results in prolonged reductions in plasma triglycerides, LDL-C, and remnant-C in human subjects. Journal of Clinical Lipidology Volume 19, Issue 3, Supplement, May–June 2025, Page e105


