三种病毒基因组测序方法比较研究
病毒在传播过程中很有可能会发生变异,因而对其变异的监测变得尤为重要。在新冠病毒蔓延的情况下,如何在病毒检测中,既能提高检测灵敏度,又能获得完整的病毒全基因组序列以用于后续变异监测和研究,同时兼顾经济高效的方法成为许多检测机构都亟需解决的问题。
在《Genome Medicine》发表的方法学研究文章中使用伯科2019-nCoVirus Capture Panel捕获测序,分别与宏基因组测序(Meta)、扩增子测序(Amplicon)进行比较。从数据中可以看出伯科Panel性能优异,在病毒基因组覆盖均一性上与Meta数据相当,突变检测准确性与Meta高度一致,是新冠病毒基因组分析的有力工具。

发表时间:2020.06.30
影响因子:10.675
DOI:10.1101/2020.03.16.993584
实验设计
样本信息:标准品(10倍梯度稀释)+ 8例临床样本
建库方法:Meta、Capture、Amplicon
测序平台:MGISEQ-2000 platform
测序深度:Meta≥10X,Capture≥20X,Amplicon≥100X
主要参数比较:覆盖均一性,富集效率/成本效益,准确性(SNV、iSNV)
参数比较
01 覆盖均一性
Capture的覆盖均一性与Meta结果相当,相对优于Amplicon。研究人员认为,可能是由于2X探针设计以及DNBSEQ测序技术的优势。Amplicon偏好可能主要来自40个循环的PCR扩增以及无法获得Unique Reads。
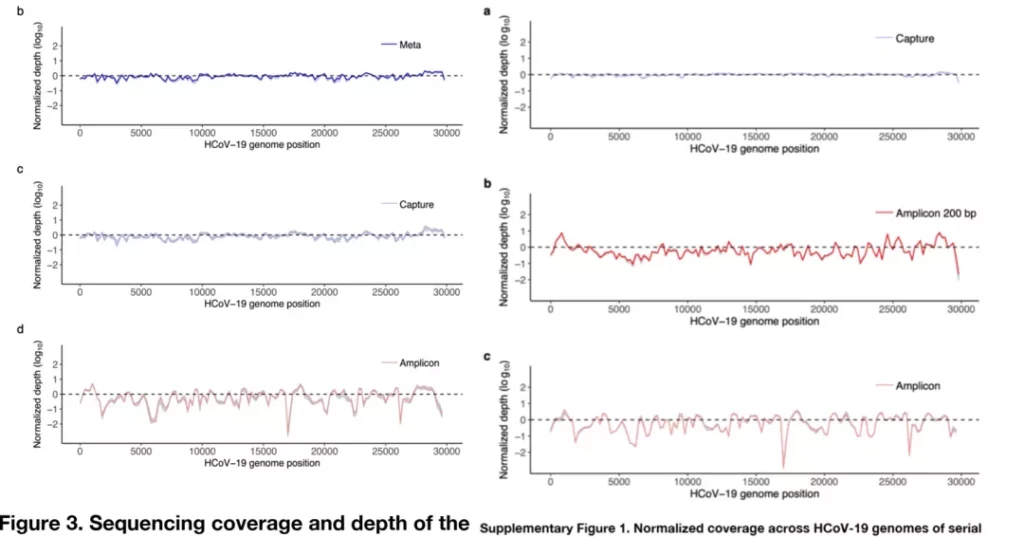
02 富集效率/成本效益
富集效率:在标准品测试中(Fig. 3e), Amplicon的富集效率优于Capture(Copies / mL<104)。值得注意的是,在临床样本中,Capture却展现出相对优异的富集效率。当病毒拷贝数较低时(Ct > 30),其效率高于Amplicon (Fig. 3f)。
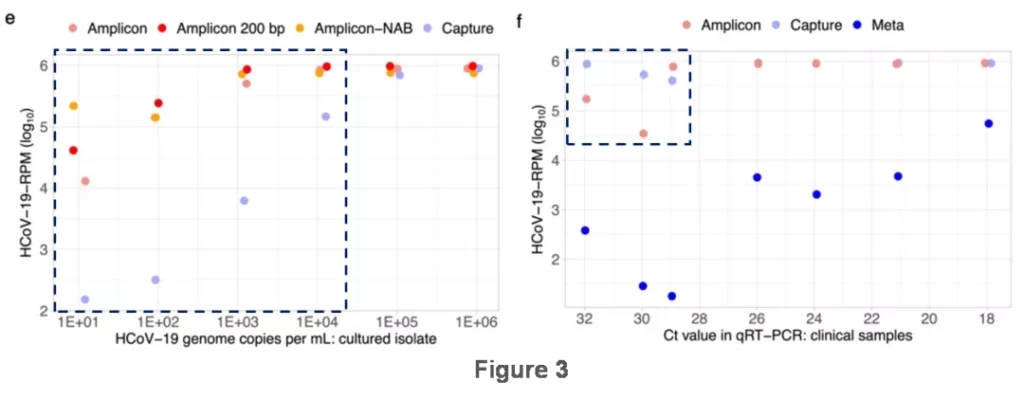
成本效益:由于Amplicon无法确定Unique Reads,基于上述富集效率并不能有效预测Amplicon的最小测序量(10X Depth+95% COV 或者High-confidence)。
即便采用上述富集效率进行推算,虽然在低拷贝数标准品中Amplicon的最小测序量低于Capture,但在临床样本中,无论病毒拷贝数高或低(除anal swab样本外),Capture所需最低数据量均少于Amplicon(Sup. Table 4)。
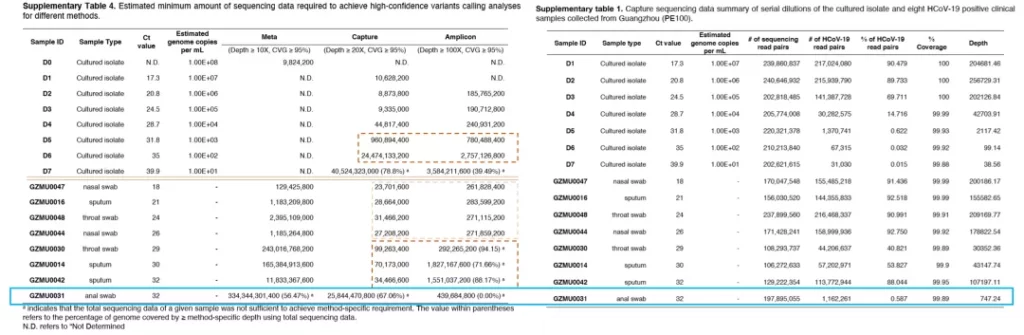
03 准确性(SNV、iSNV)
SNV:采用0.8的AF cutoff值,Capture漏检了GZMU0014样本中的G16535T突变,表明Capture可能存在一定的偏好,减少Post-PCR循环数(18)有助于减少偏好。
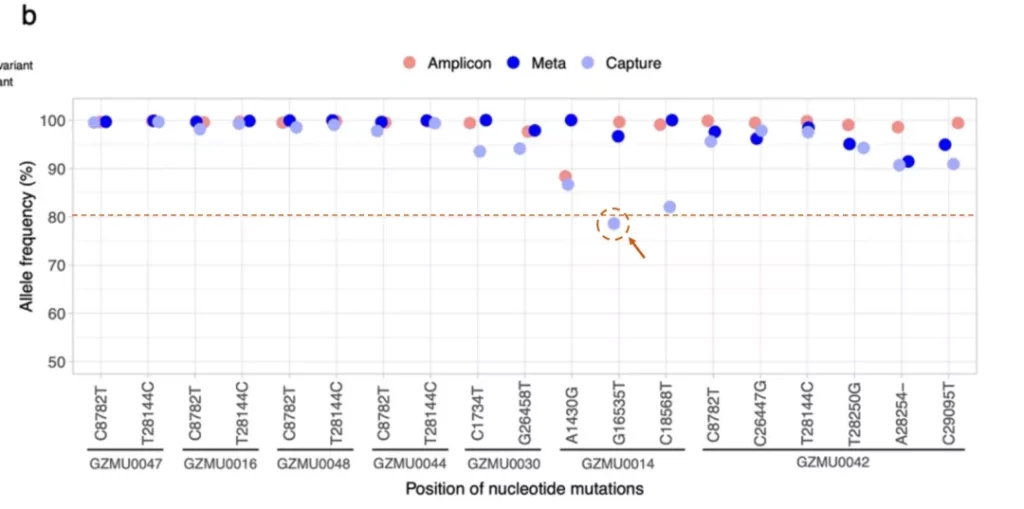
iSNV:在标准品中,Capture的iSNV检测准确性明显优于Amplicon,同时与Meta具有非常好的相关性.
04 特异性(iSNV)
在临床样本中,以Meta Calling作为标准,Capture的假阳性率和假阴性率分别为0.02%和0%,Amplicon分别为0.74%和66.7%。
文章总结
该研究系统性地解决了基于临床样品高效进行病毒全基因组测序分析的技术难点,研究披露的详细实验步骤和生物信息学流程,将极大地加速新冠病毒和其它新发病毒的基因组测序与分析,为更全面地实时监测病毒和更有效地进行疫情防控奠定基础。
伯科生物 Pathogen-Cap Panel
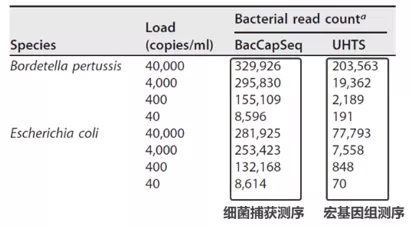
相对于传统宏基因组测序,病原微生物捕获测序可以得到更深的病原基因组覆盖(100-10000倍),更加准确和灵敏,再搭配快速杂交、自动化系统以及三代测序,捕获测序在时间、成本、通量上可以进一步提升,更加贴合临床需要。对于病原体微生物捕获,伯科已经为用户提供了针对多种亚型的HPV、HBV等基因Panel,并针对泛病原捕获开发了高效的探针设计软件,希望能为广大临床和科研机构提供更多助力。
产品特色
01 更加准确和灵敏
02 探针浓度已知,个性化Spike-in其他模块
03 高质量生产标准,结果均一稳定

为助力抗击新冠疫情,缩短病毒序列分析时间,降低检测成本,以便更好的进行病毒溯源、变异检测、进化演变等研究,伯科为临床和科研单位免费提供了超过1万人份新型冠状病毒捕获试剂盒。





