预防猝死
- boke
- 2024-05-15
- 10:21 上午
Circulation | 动脉粥样硬化是一种平滑肌细胞驱动的肿瘤样疾病
前段时间,《循环》期刊的一项研究发现[1],心脏小细胞外囊泡(sEVs),尤其是在心肌梗死后,心脏间充质基质细胞修复心脏所释放的sEVs(cMSC-sEVs),携带了多种促癌因子,当癌细胞摄取cMSC-sEVs后,会加速肿瘤的生长和转移。
近日,《循环》期刊发表的另一项研究则显示[2],动脉粥样硬化是一种平滑肌细胞驱动的肿瘤样疾病,这又拉近了肿瘤和心脑血管病的关系。

动脉粥样硬化是心脑血管疾病的主要原因之一,涉及到多种细胞类型的病理激活,包括免疫细胞(例如巨噬细胞和T细胞)、平滑肌细胞(SMCs)和内皮细胞。越来越多的证据表明,SMCs向其他细胞类型的转变,即所谓的表型转换,在动脉粥样硬化的发展和并发症中起着重要作用。
在这项研究中,采用SMC谱系追踪小鼠和人类组织,并应用分子、细胞、人类遗传学和药理学等一系列方法,研究了动脉粥样硬化中SMC衍生细胞的特征。
小鼠和人类动脉粥样硬化中的SMC衍生细胞表现出多种肿瘤细胞样特征,包括基因组不稳定性、逃避衰老、细胞过度增殖、抗细胞死亡、侵袭性和激活癌症相关基因调控网络。
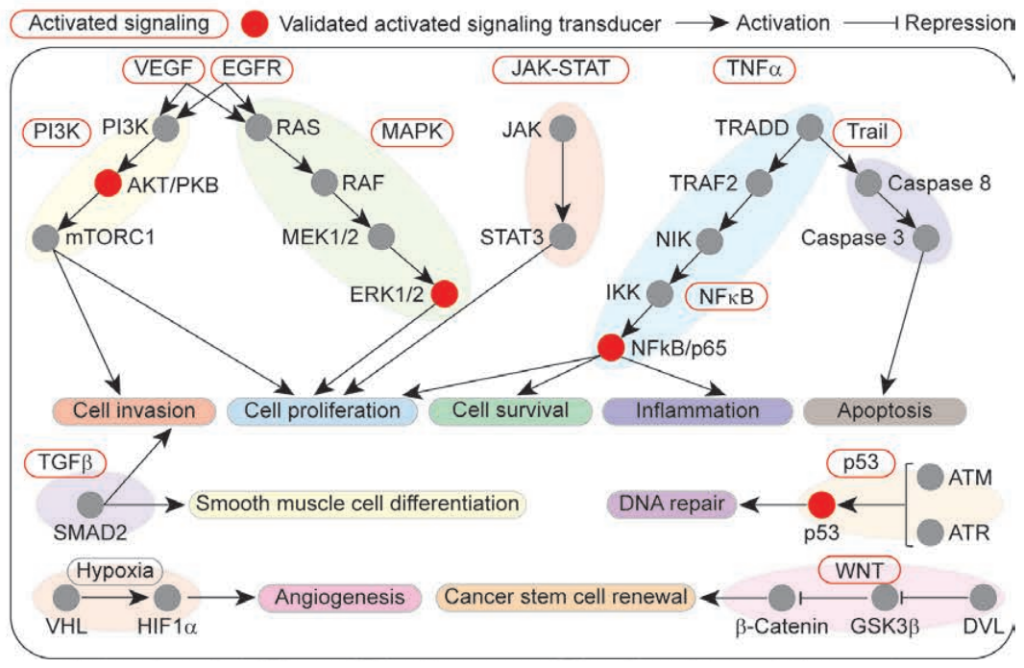
癌症相关信号通路在SMC衍生细胞中被激活 [2]
在SMCs中特异性表达致癌突变体KrasG12D促进了氧化性DNA损伤,加速了SMC的表型转变,并加重了小鼠的动脉粥样硬化。随后,研究人员还发现,一种针对DNA损伤修复的抗癌药物 Niraparib 不但可以减缓小鼠模型中的动脉粥样硬化进展,还能在疾病晚期诱导病变的恢复。这些发现表明,针对DNA损伤修复的治疗方法在小鼠模型中对动脉粥样硬化及斑块稳定性特征具有预防和治疗益处。
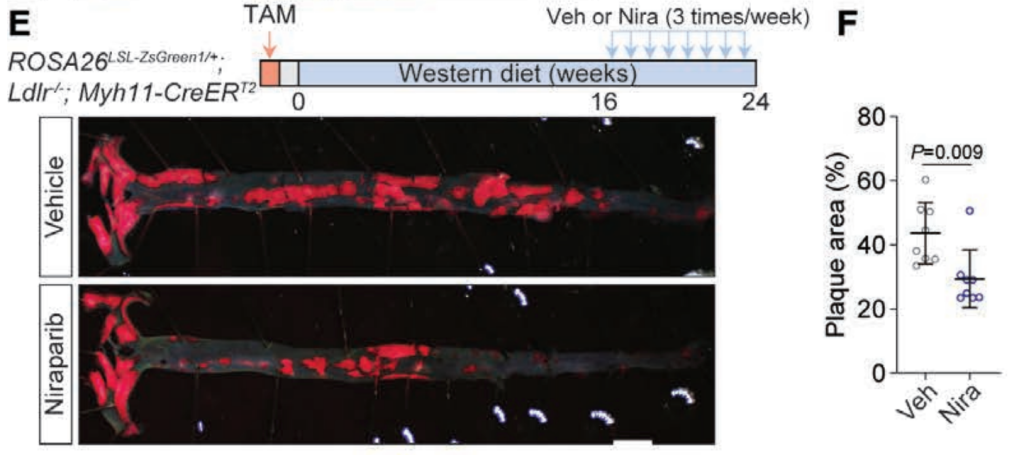
抗癌药物Niraparib减轻小鼠主动脉的动脉粥样硬化斑块负担[2]
基于上述结果,研究者认为,动脉粥样硬化是一种SMC驱动的肿瘤样疾病,推进了我们对其发病机制的理解,并提出了“动脉肿瘤学”概念模型(下图)作为动脉粥样硬化心血管疾病的基础和转化研究的综合概念。在模型中,血管本身的病变平滑肌衍生细胞以及流动的来自骨髓的潜能不明克隆性造血细胞共同影响了动脉粥样硬化斑块的产生和进展,为创新的精准分子策略开辟了预防和治疗动脉粥样硬化心血管疾病的新方向。
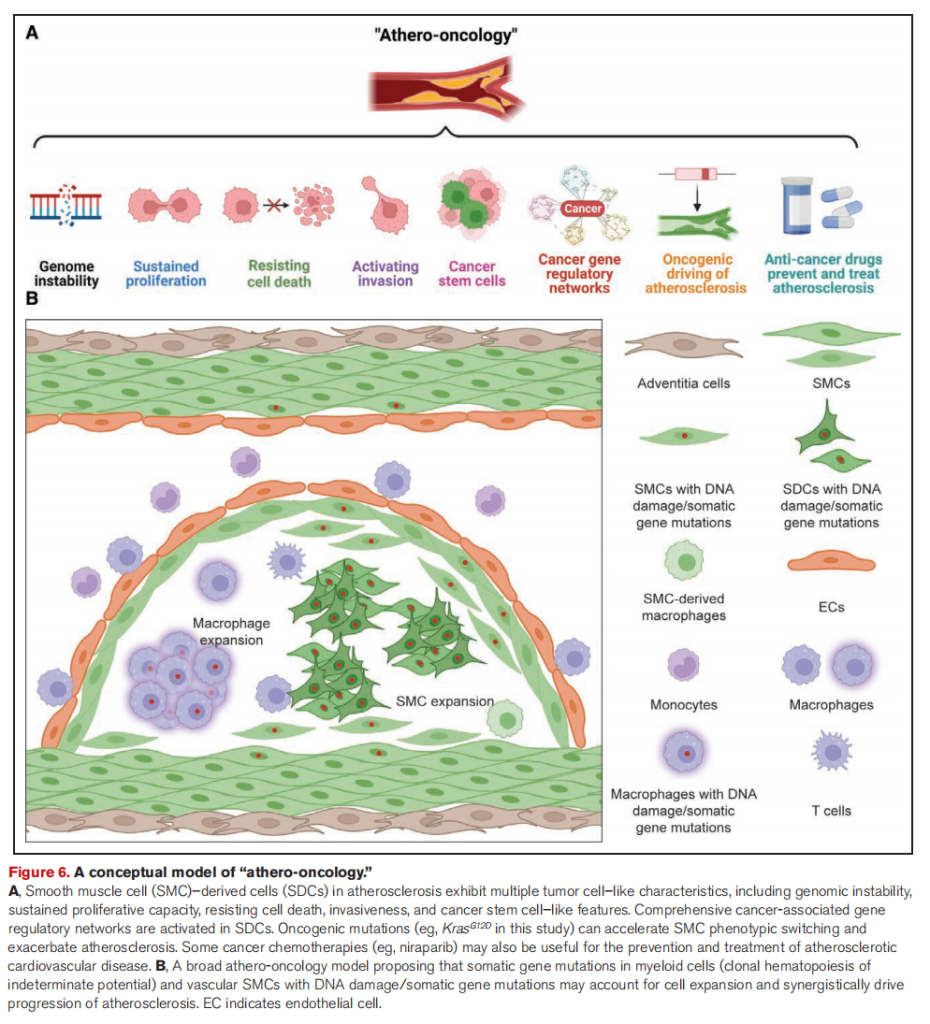
“动脉肿瘤学”概念模型[2]
在潜能不明克隆性造血对心脑血管疾病的作用方面,2024年1月11日,心脏病研究顶级期刊-JAMA Cardiology在线发表了国家心血管病中心、中国医学科学院阜外医院顾东风院士和鲁向锋教授团队关于中国人群CHIP(潜能不明克隆性造血)相关体细胞基因变异与冠心病发生关系的研究成果[3]。通过伯科生物设计开发的液相基因芯片(Gene Panel)分别检测先天遗传(冠心病PRS)和后天基因变异(CHIP),该成果首次解码了中国自然人群CHIP体细胞变异特征谱,填补了克隆性造血相关体细胞基因突变对心血管疾病作用的多个空白,进一步推动了冠心病的个体化精准防治。

参考资料
1. Caller T, Rotem I, Shaihov-Teper O, et al. Small Extracellular Vesicles From Infarcted and Failing Heart Accelerate Tumor Growth[J]. Circulation, 2024.
2. Pan H, Ho SE, Xue C, et al. Atherosclerosis Is a Smooth Muscle Cell-Driven Tumor-Like Disease. Circulation. 2024 Apr 30.
3. Zhao K, Shen X, Liu H, et al. Somatic and Germline Variants and Coronary Heart Disease in a Chinese Population[J]. JAMA cardiology, 2024.


