前瞻性研究,利用cfDNA绘制血液样本中的肿瘤特异性转录因子结合位点特征,预测小细胞肺癌患者亚型与治疗反应
- boke
- 2025-03-19
- 2:59 下午

1
背 景
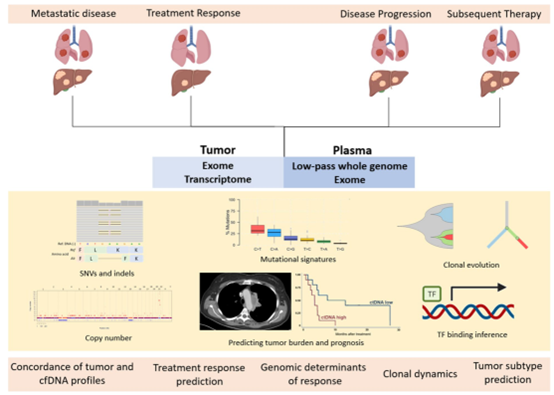
循环游离DNA (cfDNA) 检测分析已成为肿瘤医学实践中的重要基础,但cfDNA揭示肿瘤来源分子特征的有效性尚未在肿瘤前瞻性队列的患者中与标准单病灶肿瘤活检进行系统比较。对于小细胞肺癌 (SCLC) 患者而言,因为该癌症的临床进展迅速,这使得获取肿瘤活检材料非常困难,因此,采用血浆而非组织指导治疗尤其具有吸引力。
2
方 法
本研究分析了来自20例复发性SCLC患者的49份血浆样本,这些样本是在治疗前、治疗中和治疗后获得的。我们进行了cfDNA低深度全基因组测序(0.1X),并将其与匹配的肿瘤特征进行比较,该肿瘤特征通过全外显子组(130X)和转录组测序获得。
3
结 果
cfDNA和肿瘤活检的直接比较表明,cfDNA不仅反映了相应肿瘤的突变和拷贝数特征,还检测到了临床上相关的耐药机制和未在配对肿瘤活检中发现的驱动基因突变。纵向cfDNA分析能可靠地追踪肿瘤的反应、进展和克隆进化。血浆DNA片段在转录起始位点周围的测序覆盖率显示出显著的治疗相关变化,并反映了相应SCLC肿瘤中关键转录因子的表达,例如NEUROD1和REST,这也使得其能够预测SCLC神经内分泌表型和预测治疗反应。
4
结 论
cfDNA完整地反映了肿瘤的异质性和进化过程。目前SCLC作为一种单一实体进行治疗,这些发现对SCLC的无创分子分型具有重要意义。
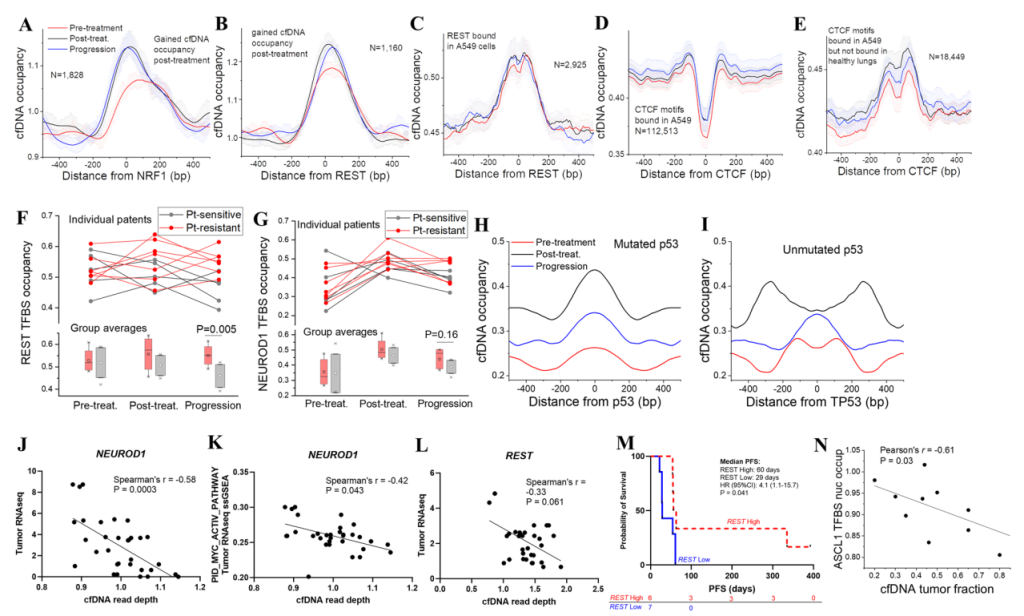
cfDNA转录因子结合位点占位预测小细胞肺癌 (SCLC) 表型和治疗反应
目前,大多数cfDNA应用都以基因为中心,侧重于体细胞变异,当肿瘤突变未知且肿瘤受失调转录程序驱动时,其效用有限。该研究发现cfDNA转录因子结合谱反映了治疗前后(治疗前、治疗后和肿瘤进展)以及化疗敏感性(铂敏感和耐药)的变化。NEUROD1和ASCL1此前已被认为是SCLC亚型的关键标志物。研究还发现,cfDNA对NEUROD1的可及性与其在相应肿瘤中的表达之间存在显著关联,该关联通过核小体足迹分析进行推断。在REST的可及性和表达之间也观察到类似趋势,这反映了神经内分泌分化程度低的肿瘤,且这些肿瘤对免疫疗法的反应可能性更高。另一个重要发现是,ASCL1结合位点的核小体占据率与cfDNA分数呈强烈的负相关。
SCLC肿瘤在神经内分泌特征表现出明显的肿瘤间异质性,这由谱系转录因子的表达驱动着。这些亚型是否会产生特定的治疗脆弱性,有待进一步研究。临床验证这些亚型的一个主要障碍是高质量肿瘤分子分析样本的有限性。基于cfDNA结合位点(如REST、ASCL1和NEUROD1)的转录因子可及性,可以区分SCLC神经内分泌表型,从而实现对患者的非侵入性表征和治疗。
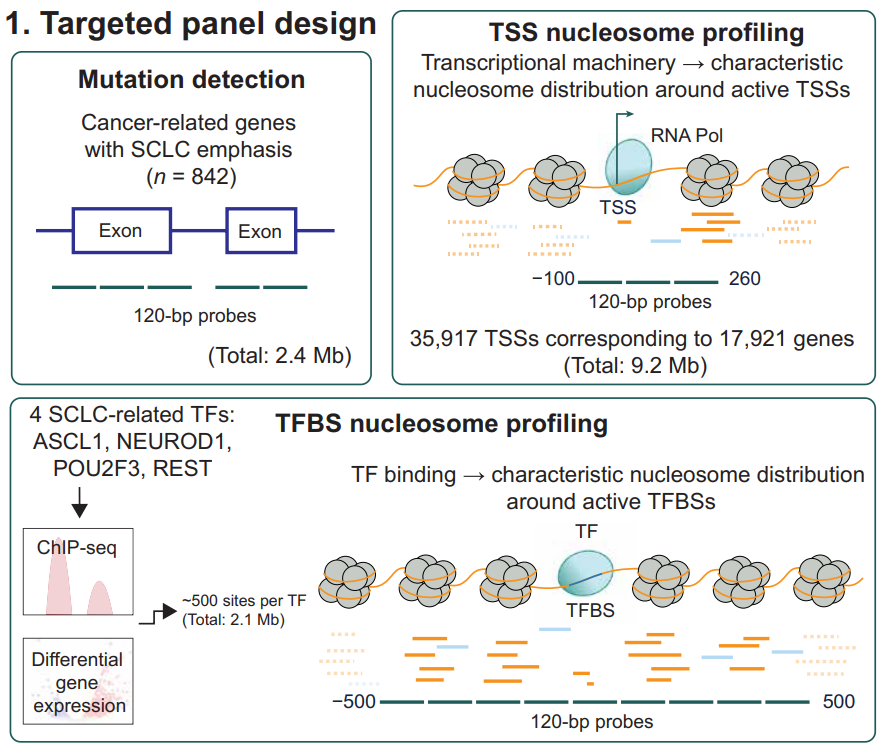
针对cfDNA测序方法,靶向捕获基因组中已知转录起始位点或SCLC特异性转录因子结合位点的cfDNA片段,这可能会使该方法更易于临床应用。最近,基于靶向高深度cfDNA测序结合基因表达分析,利用NEUROD1、ASCL1和REST结合位点进行SCLC亚型分型[2]。
参考资料
[1] Takahashi, N., Pongor, L., Agrawal, S.P. et al. Genomic alterations and transcriptional phenotypes in circulating free DNA and matched metastatic tumor. Genome Med 17, 15 (2025).
[2] Joseph B. Hiatt et al. ,Molecular phenotyping of small cell lung cancer using targeted cfDNA profiling of transcriptional regulatory regions.Sci. Adv.10,eadk2082(2024).


