NCCN 2026.V3.0 | 前列腺癌诊断与精准治疗
- boke
- 2026-03-06
- 5:05 下午
提到男性高发癌症,很多人会先想到肺癌、胃癌,却常常忽略一个“沉默的杀手”——前列腺癌。作为男性生殖系统最常见的恶性肿瘤,前列腺癌的发病率在全球男性恶性肿瘤中位居第二,且随着人口老龄化加剧,我国的发病率正逐年攀升。不同于其他恶性肿瘤,前列腺癌早期症状隐匿,很多患者确诊时已处于中晚期,错失了最佳治疗时机。但值得庆幸的是,前列腺癌进展缓慢,若能早期发现、规范治疗,5年生存率可高达90%以上[1]。
前列腺癌风险因素[2]:
(1)遗传因素:前列腺癌是一种具有高度遗传性的癌症,据估计约40%~50%的前列腺癌与遗传因素相关[3]。

(2)年龄与种族:年龄是前列腺癌最重要的危险因素之一,前列腺癌的发病率随年龄增长显著上升;不同种族的前列腺癌发病率存在差异,非洲裔男性发病率较高,亚洲人发病率相对较低。
(3)生活方式和环境:高脂肪、高热量饮食可能增加发病风险,而富含蔬菜、水果、全谷物、番茄红素、豆类等的食物可能有助于降低风险;长期暴露于某些环境污染物、辐射,或昼夜节律紊乱可能增加前列腺癌的发病风险。
(4)疾病:前列腺炎、良性前列腺增生等前列腺疾病可能与前列腺癌发病风险相关。
一、前列腺癌诊断
前列腺癌的诊断并非单一检查就能确诊,而是一个“层层递进”的过程,核心是排除良性病变、明确癌症分期,为后续治疗提供依据。
1
初步筛查
前列腺癌的初步可疑诊断依据为直肠指检(DRE)异常或前列腺特异性抗原(PSA)水平升高。
2
确诊检查
前列腺穿刺活检:确诊前列腺癌的金标准。在超声或MRI引导下,用细针穿刺前列腺组织,获取样本进行病理学检查,明确是否存在癌细胞、癌细胞类型及分化程度等。
影像学检查:
磁共振成像(MRI):帮助判断肿瘤位置、范围及是否侵犯周围组织,对临床分期有重要价值。
计算机断层扫描(CT):用于评估肿瘤是否转移至盆腔淋巴结或其他器官,对晚期前列腺癌的分期有帮助。
骨扫描或PET-CT:用于判断是否存在骨转移或其他远处转移,尤其适用于晚期患者或PSA升高但影像学检查未发现明显病灶的情况。
3
风险分级与分期
活检结果中,“Gleason分级”是关键指标:分级越高,癌细胞恶性程度越高,预后越差;确诊后,需根据肿瘤侵犯范围、转移情况进行分期(常用TNM分期),不同分期的治疗方案差异极大。
二、前列腺癌的治疗
前列腺癌的治疗需结合患者年龄、身体状况、肿瘤分期、分级等因素综合判断,核心原则是“根治优先、姑息为辅”,同时兼顾患者的生活质量。
1
临床局限性前列腺癌的治疗方案
局限性前列腺癌初始风险分层:
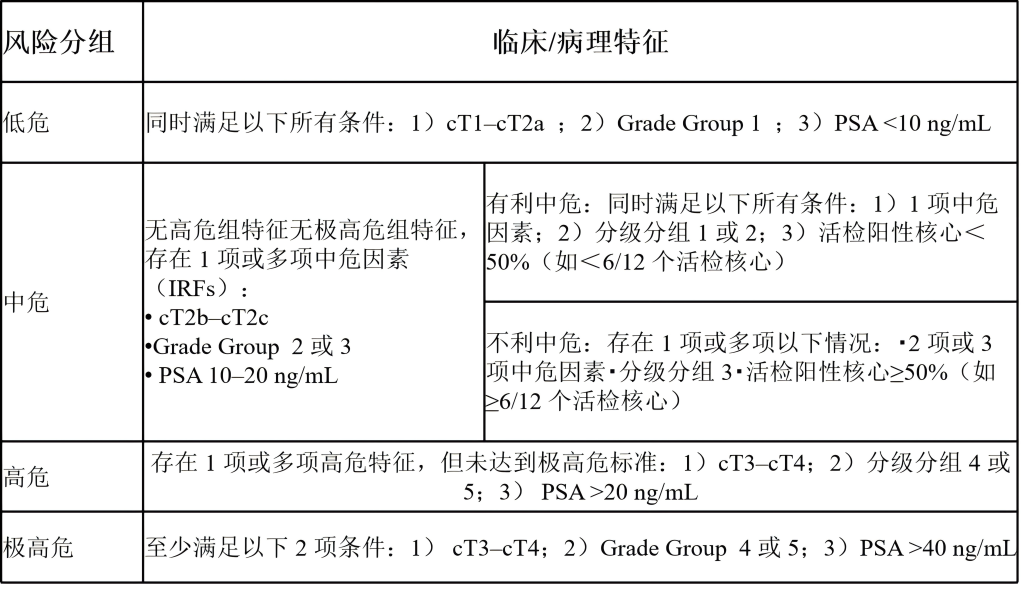
局限性前列腺癌的初始治疗:
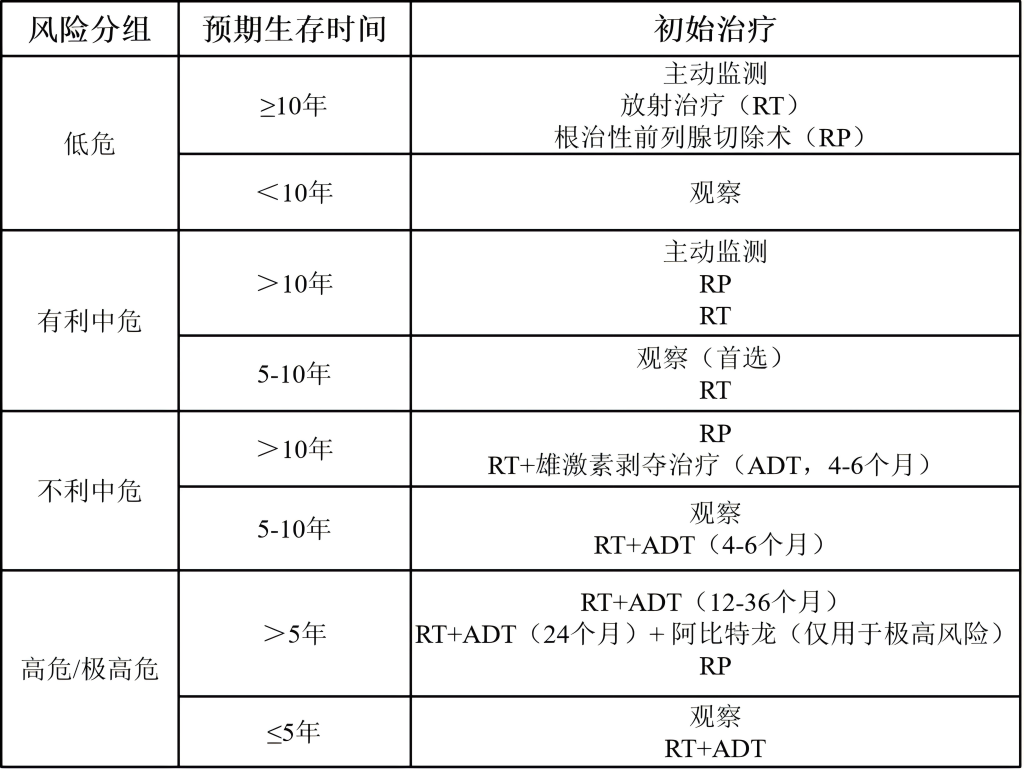
2
区域性前列腺癌方案
预期生存>5年或有症状的患者:
放疗(RT)+ADT(24个月)+阿比特龙(首选)或RT+ADT(24–36个月)
ADT±阿比特龙
选择性患者行根治性前列腺切除术(RP)
预期生存≤5年且无症状的患者:
观察
放疗(RT)
ADT±RT
3
异时寡转移去势敏感性前列腺癌(CSPC)的检查与治疗
转移灶检查:体格检查、分期影像学检查、PSA检测及PSADT计算、预期寿命评估、胚系和体细胞基因检测及家族史采集(若之间未进行)、生活质量评估。
治疗:MDT(多学科团队)±ADT。
4
低瘤负荷M1期(异时性或同时性)或同时性寡转移性去势敏感性前列腺癌的检查与治疗
转移灶检查:同上。
治疗:
同时性低瘤负荷转移或同步寡转移:
ADT+首选方案(阿比特龙、阿帕他胺、恩扎鲁胺)或其他推荐(达罗他胺)
ADT+多西他赛+阿比特龙/阿帕他胺/达罗他胺/恩扎鲁胺(仅低瘤负荷疾病)
ADT+原发肿瘤外照射放疗(EBRT)±阿比特龙/阿帕他胺/多西他赛/恩扎鲁胺
异时性低瘤负荷转移:
ADT+首选方案(阿比特龙、阿帕他胺、恩扎鲁胺)或其他推荐(达罗他胺)
监测:体格检查+PSA每3–6个月,定期影像学检查,监测治疗反应。
注:低瘤负荷前列腺癌是转移性前列腺癌的一种亚型,通常指转移范围相对局限、肿瘤负荷较低的前列腺癌患者。
5
高瘤负荷M1期去势敏感性前列腺癌(CSPC)的检查与治疗
转移灶检查:同上。
治疗:ADT+多西他赛+首选方案(阿比特龙/达罗他胺)或其他推荐(阿帕他胺/恩扎鲁胺)
ADT+首选方案(阿比特龙/阿帕他胺/恩扎鲁胺)或其他推荐(达罗他胺)
注:高瘤负荷前列腺癌是前列腺癌的一种晚期阶段,具有较高的肿瘤负荷和较差的预后。
6
M0去势抵抗性前列腺癌(CRPC)的评估与治疗
继续雄激素剥夺治疗(ADT),维持血清睾酮去势水平(<50 ng/dL)。
根据PSADT分层治疗:
PSADT>10个月:首选监测,或选择其他二线激素治疗;
PSADT≤10个月:阿帕他胺、达罗他胺、恩扎鲁胺(首选);其他二线激素治疗(其他推荐)。
治疗后监测与进展处理
治疗后需定期评估PSA和影像学检查:
若PSA稳定且无转移证据:维持当前治疗,可考虑定期疾病评估;
若PSA升高或影像学提示转移:进行影像学检查。
若仍为M0(无转移):调整或维持当前治疗,继续定期进行疾病评估
进展为M1(转移):进入M1 CRPC诊疗方案。
注:去势敏感性前列腺癌(CSPC)与去势抵抗性前列腺癌(CRPC)是前列腺癌发展过程中的不同阶段。
CSPC:指肿瘤细胞的生长和增殖依赖雄激素,经雄激素剥夺治疗(ADT)降低体内雄激素水平后,肿瘤生长可得到有效抑制,疾病对ADT治疗敏感。
CRPC:指在ADT治疗后,肿瘤仍继续进展。肿瘤细胞仍能通过多种机制(如雄激素受体突变、自分泌雄激素合成增强等)继续生长和增殖,对传统的内分泌治疗产生抵抗。
7
M1型CRPC的检查和治疗
(1)初始检查与评估:
转移性病变活检、同源重组修复(HRR)、微卫星不稳定性(MSI)/错配修复缺陷(dMMR)和肿瘤突变负荷(TMB)的体细胞检测(之前未进行)。
(2)治疗方案:
首选治疗:继续ADT以维持血清睾酮的去势水平(<50 ng/dL)
其他治疗选择:如果出现骨转移,则使用地舒单抗(首选)或唑来膦酸进行骨抗吸收治疗;对疼痛性骨转移进行姑息性放疗;最佳支持治疗。
(3)病理分层与后续治疗:
小细胞/神经内分泌前列腺癌(NEPC):
一线及后续治疗方案:顺铂/依托泊苷、卡铂/依托泊苷、多西他赛/卡铂、卡巴他赛/卡铂;最佳支持治疗。
腺癌:
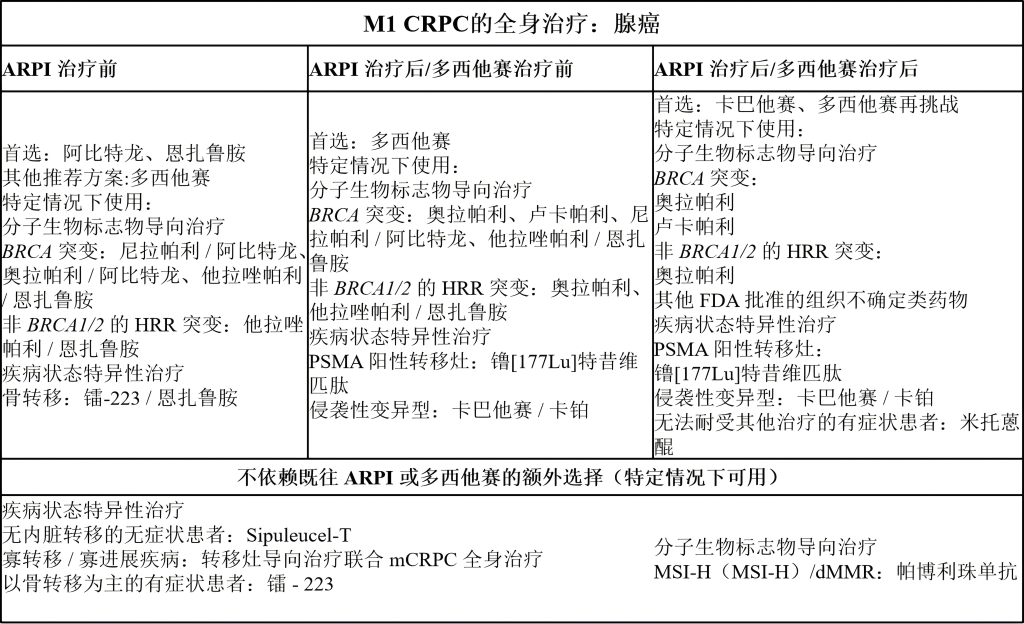
三、前列腺癌常用治疗药物
1
内分泌治疗药物
雄激素合成抑制剂:阿比特龙
促黄体生成素释放激素类似物(LHRH激动剂):戈舍瑞林、亮丙瑞林、曲普瑞林
促黄体生成素释放激素拮抗剂(LHRH拮抗剂):地加瑞克、瑞卢戈利
非甾体类抗雄药:
一代:比卡鲁胺、氟他胺、尼鲁米特
二代:恩扎卢胺、阿帕他胺、达罗他胺、瑞维鲁胺
2
化疗药物
多西他赛、卡巴他赛
3
靶向治疗药物
PARP抑制剂:奥拉帕利、卢卡帕尼、他拉唑帕利
放射性配体疗法:镥[177Lu]特昔维匹肽
4
免疫治疗药物
帕博利珠单抗、Sipuleucel-T(自体细胞免疫疗法)
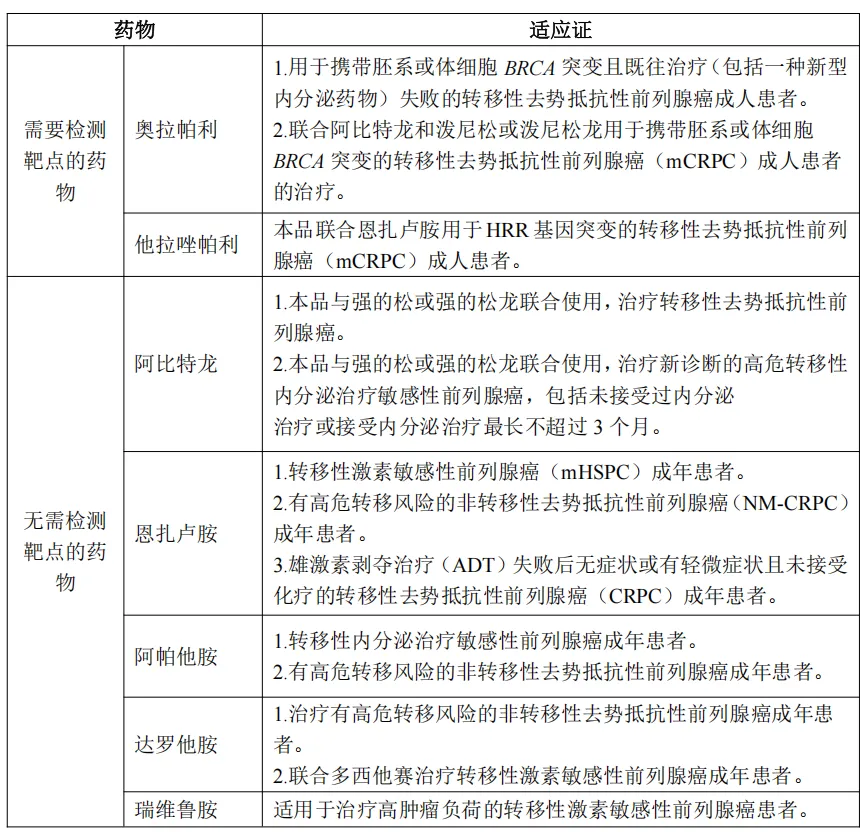
部分前列腺癌治疗药物及适应证[4]
四、前列腺癌基因检测
前列腺癌具有高度异质性,不同患者的生存时间、治疗效果和生存预后均存在很大差异。且在前列腺癌病程的不同阶段,需要综合运用手术、放疗、药物等多种治疗手段。随着二代测序(NGS)技术在前列腺癌诊疗中愈加广泛的应用,越来越多的患者能够从前列腺癌精准治疗中获益。基因检测能满足前列腺癌患者个性化诊疗需求,为患者治疗、预后和遗传风险提供指导和评估[5]。


伯科生物在国内已经建设了全流程国产化的高通量核酸合成与应用技术转化中心,建立了GMP厂房和ISO9001、ISO13485质量体系。已经为国内外数百家知名医院、科学研究机构、临床检验所开发了上千款Gene Panel(液相基因芯片),并配套完整的检测试剂,各项性能参数均与国际竞品相当或优于(详见附表1),在基因组、转录组、甲基化组及病原体的检测应用方向均有成熟的产品管线。
附表1: 产品简介
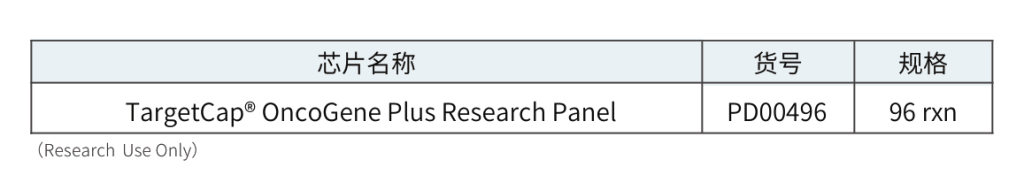
肿瘤液相基因芯片
伯科设计的TargetCap® OncoGene Plus Research Panel基于美国食品药品监督管理局(FDA)批准的用于肿瘤基因检测的FoundationOne CDxTM与MSK-IMPACTTM,其覆盖702个肿瘤相关基因编码区和34个基因的非编码区(融合基因),含有6个MSI和53个化药相关位点,探针覆盖2.32Mb区间。这些区域涵盖更多基因,检测范围更泛,涉及肿瘤高频突变、肿瘤易感、药物靶向、药物耐受等多种类型基因。
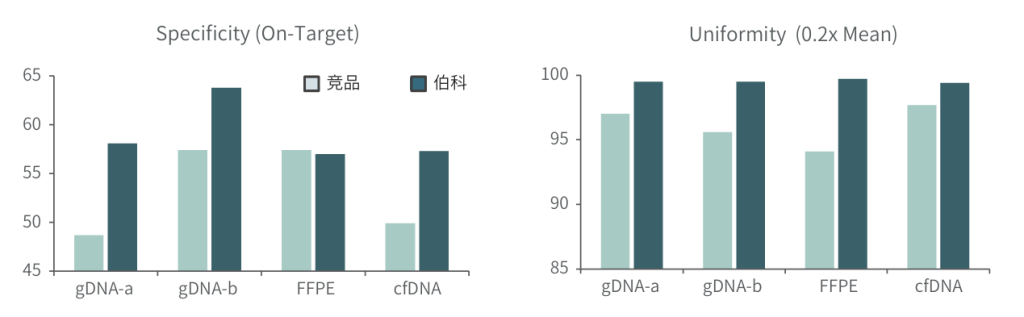
性能表现
竞品评测
采用gDNA/cfDNA/FFPE/泛肿瘤800gDNA标准品文库,分别使用伯科商品化肿瘤大Panel-OncoGene Plus Research Panel与竞品肿瘤大Panel进行性能比较(二者大小相近),在捕获特异性上(On-Target)和覆盖均一性(0.2XMean)上,伯科均优于竞品。
对于gDNA标准品,竞品测序35.9Gb,伯科测序19.6Gb,虽然伯科测序数据少,深度低,但二者的突变频率检出无明显差异,伯科对EGFR的19号外显子缺失变异的检出优于竞品。
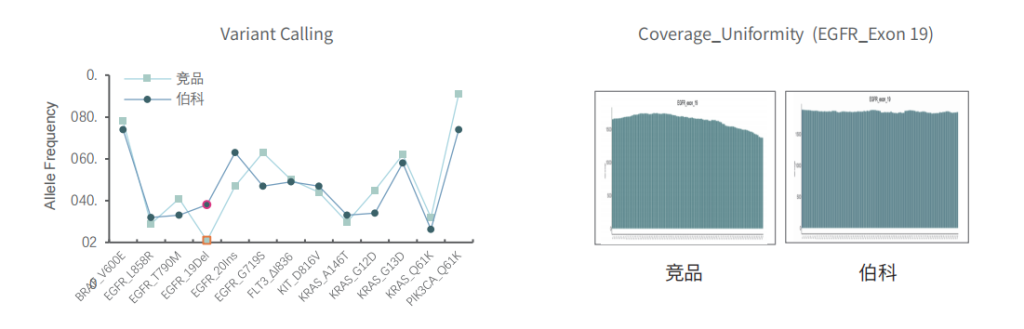
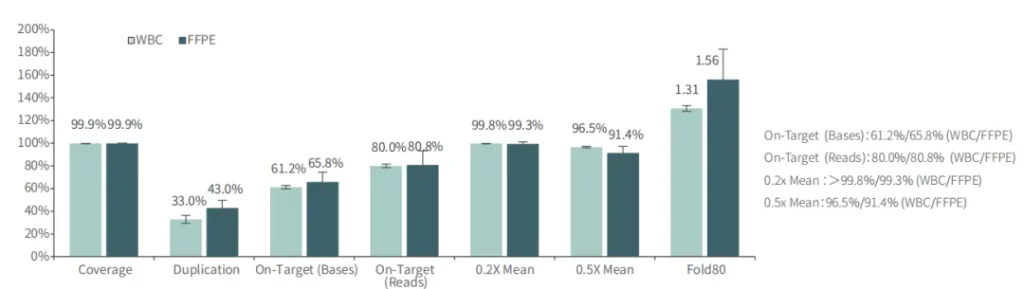
不同样本类型表现
对不同质量的gDNA样本 (WBC/FFPE, >150例),TargetCap® OncoGene Plus Research Panel表现稳定。
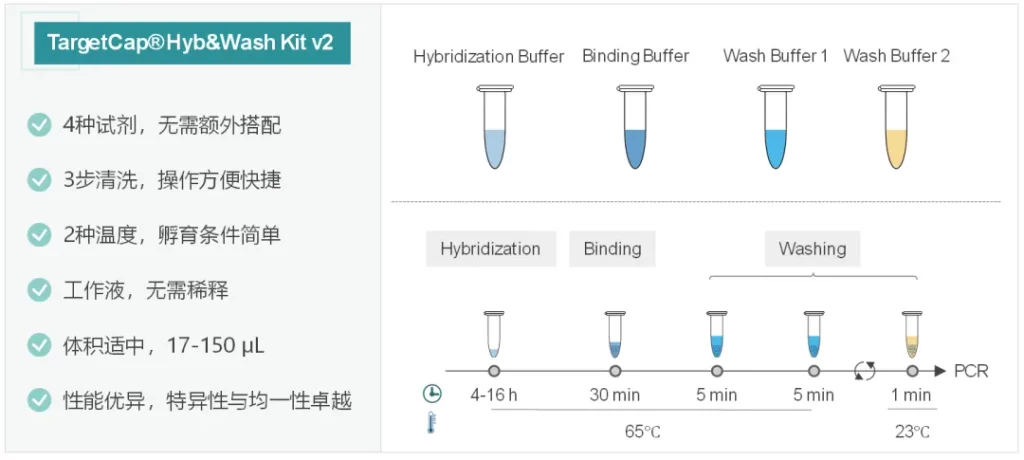
杂交与清洗试剂盒v2 简介
试剂盒概述
伯科杂交与清洗试剂盒v2 (TargetCap® Hybridization and Wash Kit v2,下文简称Hyb&Wash Kit v2)简化了试剂组分和操作流程,同时仍保持优异的捕获性能。Hyb&Wash Kit v2包含4种缓冲液组分,仅需3步清洗,操作流程更加便捷。
性能表现介绍
Ⅰ. 基本QC表现
使用NA12878和NA24694 gDNA标准品,采用三款不同大小的Gene Panel (650Kb、2.3Mb和42Mb) 对Hyb&Wash Kit v2 和 v1 进行比较测试。
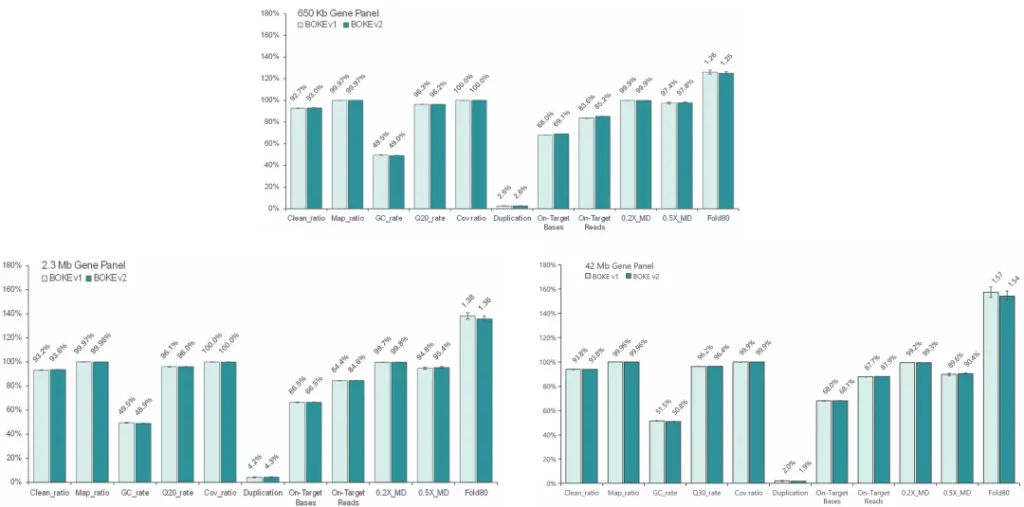
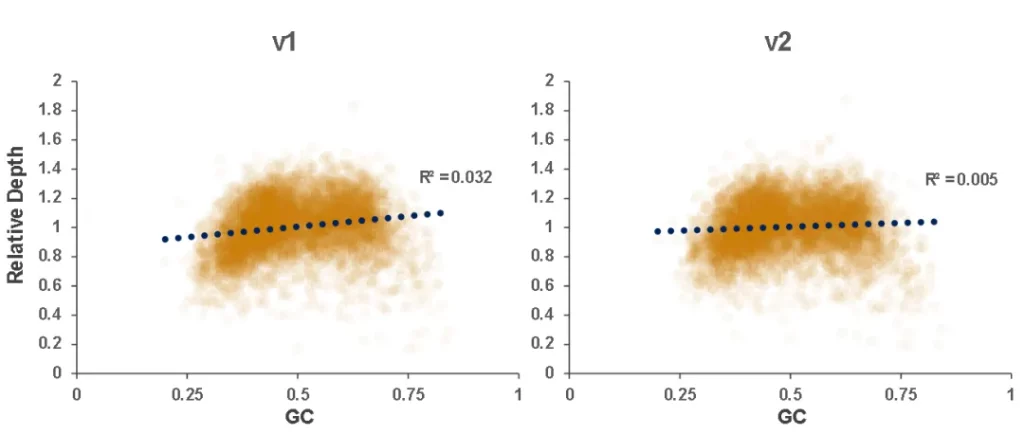
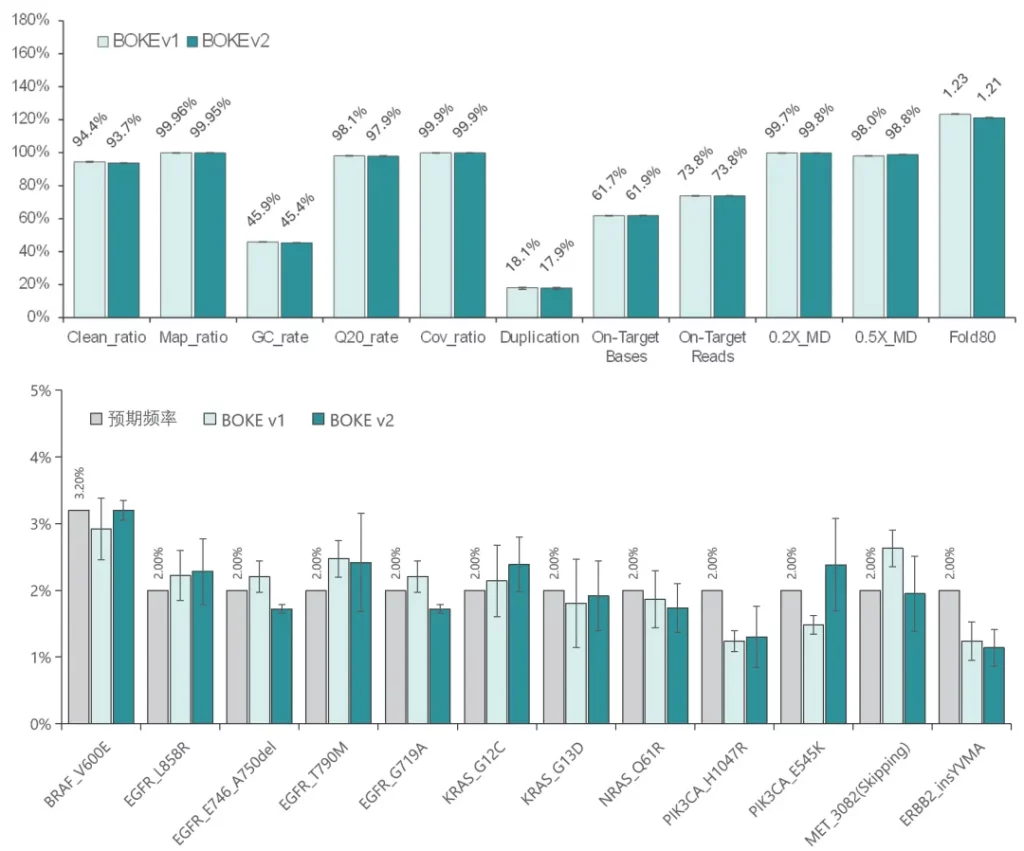
结果显示,在不同大小的Gene Panel中,对于杂交与清洗试剂盒的关键参数-中靶率和均一性,v2与v1试剂盒表现相当,v2试剂盒表现更好的均一性(0.2X_MD、0.5X_MD和Fold80)。
Clean_ratio、Map_ratio等基本参数两款试剂盒表现一致,由于v2试剂盒对低GC目标区域覆盖更佳,其GC_rate率略低于v1。
Ⅱ. 低频变异检测
使用肿瘤 SNV gDNA 标准品Ⅱ (GW-OGTM006) 对Hyb&Wash Kit v2的低频变异检测性能进行验证。GW-OGTM006 DNA标准品包含 EGFR、KRAS、NRAS、BRAF、PIK3CA、FGFR3、Her2、MET 等多个常见伴随诊断基因及位点,包含点突变、插入和缺失等多种变异类型。
采用300 Kb Gene Panel对该标准品进行捕获,捕获数据显示,v1与v2试剂盒的基本捕获性能表现相当,v2的中靶率与均一性略优于v1。同时,v1与v2试剂盒均能对12个已知变异准确检出。
参考文献:
1.Litwin M S, Tan H J. The diagnosis and treatment of prostate cancer: a review[J]. Jama, 2017, 317(24): 2532-2542.
2.前列腺癌危险因素及病因学相关防控策略[J].中华泌尿外科杂志,2025,46(11): 816-821.
3.中国家族遗传性肿瘤临床诊疗专家共识(2021年版)—家族遗传性前列腺癌.
4.新型抗肿瘤药物临床应用指导原则(2025年版),国家卫生健康委.
5.中国前列腺癌患者基因检测专家共识(2020年版)[J].中国癌症杂志,2020,30(07):551-560.
6.NCCN Clinical Practice Guidelines in Prostate Cancer (2026 Version 3).


