NCCN 2025 V2.0|胰腺癌诊断与精准治疗
- boke
- 2026-02-10
- 9:27 上午
一、疾病概述
在众多癌症之中,胰腺癌有着“癌中之王”的称号,严重威胁着公众健康。2025年最新报道,胰腺癌在男性和女性中的发病率均已位列恶性肿瘤前10,其死亡率在男性中居第4位,在女性中居第3位,是最致命的恶性肿瘤之一。约57%的胰腺癌患者在确诊时已发生转移,转移性患者的5年生存率尚不足5%[1]。
胰腺癌的风险因素包括:
(1)生活方式:吸烟、饮酒已明确与胰腺癌相关;部分研究证明大量摄入红肉/加工肉类和乳制品可能增加胰腺癌风险。
(2)化学物质暴露:接触β-萘胺、联苯胺、农药、石棉、苯和氯代烃等化学物质及重金属,会增加胰腺癌风险。
(3)疾病:慢性胰腺炎、糖尿病等疾病与胰腺癌风险增加相关。
(4)遗传因素:5%~10%的胰腺癌患者具有遗传易感基因。携带致病性突变(ATM、BRCA1、BRCA2、CDKN2A、MLH1、MSH2、MSH6、PALB2、PMS2、STK11和TP53)的患者,或有癌症家族史(尤其是胰腺癌家族史)的患者,无论突变状态如何,均建议进行遗传咨询[2]。
二、胰腺癌分期

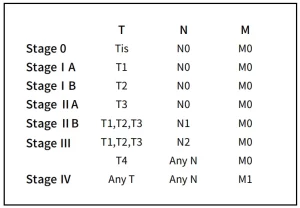
三、胰腺癌的诊断与治疗
1
临床表现和检查
临床怀疑胰腺癌或出现胰腺和/或胆管扩张(狭窄)时,首先进行胰腺CT或腹部MRI;完成影像学检查后,进行多学科会诊。
(1)无转移
胸盆腔CT、超声内镜(EUS)、MRI(性质不明的肝脏病变)、PET/CT(针对高危患者)、考虑进行逆行胆管造影(ERCP)+支架置入、经充分胆道引流后进行的肝功能及CA 19-9基线检测、遗传突变检测(确诊胰腺癌)。
根据检查结果分为无肿块或未确诊(患者转诊至高容量医疗中心进行评估)、可切除、边缘可切除疾病、局部晚期、转移性疾病,按照各自治疗方案进行治疗。
(2)存在转移
首选对转移部位进行活检确认,后续进行遗传突变的基因检测、肿瘤组织的分子特征分析、使用胸部和盆腔CT完成分期,最后按照转移性疾病方案进行治疗。
2
可切除胰腺癌的治疗
(1)无高危特征(无新辅助治疗)
进行开腹或微创手术,可考虑分期腹腔镜检查。术后若成功切除,进入辅助治疗与监测;若术中发现不可切除,按照术中不可切除疾病方案治疗。
(2)新辅助治疗后手术(无论是否有高危特征)
治疗前进行EUS引导活检(之前未完成)、支架置入(有临床指证)、PET检查及CA19-9基线检测,后进入新辅助治疗。
完成新辅助治疗之后,进行胰腺CT、腹部MRI、胸部/盆腔CT、考虑进行PET扫描、治疗后的CA 19-9水平以重新评估病情。
注:CA 19-9(糖类抗原19-9)是唾液酸化Lewis血型抗原家族,是目前已验证的、临床应用最广泛的胰腺癌早期检测和监测生物标志物,在胰腺癌的诊断、筛查、分期、可切除性判断、术后预后评估以及化疗反应预测中均具有潜在应用价值。
疾病进展未排除手术可能:考虑更换新辅助全身治疗,后续再评估手术可行性。
疾病进展排除手术可能:按照局部晚期或转移性疾病方案治疗。
疾病稳定/缓解:若未行分期腹腔镜,需补充该检查;后续若可进行手术切除,术后进入辅助治疗;若不可切除,则按照术中不可切除疾病方案治疗。
(3)医学上无法手术
按照局部晚期疾病方案治疗。
3
边缘可切除胰腺腺癌的治疗
首先进行EUS引导活检(优先选择,之前未进行)、腹腔镜肿瘤分期(可选)、基线CA19-9检测及PET(可选),根据活检结果进行不同治疗:
(1)活检阴性(未确诊癌症)
重复活检,若仍未确诊,患者转诊至高容量医疗中心进行评估)。
(2)活检阳性
考虑进行ERCP+支架置入,后进入新辅助治疗。
4
局部晚期胰腺癌治疗
首先进行活检,根据活检结果进行治疗:
(1)未确诊癌症
重复活检(若存在黄疸,需进行ERCP+支架置入),若仍未确诊则转诊至高容量中心;若确诊其他癌症则按相应指南治疗;若确诊腺癌则进入后续评估。
(2)确诊腺癌
进一步完善遗传突变检测(之前未完成)及肿瘤分子谱分析(之前未完成);若存在黄疸,优先经ERCP置入自膨式金属支架(SEMS),后按照局部晚期疾病方案治疗。
(3)确诊其他癌症
按对应的NCCN指南治疗。
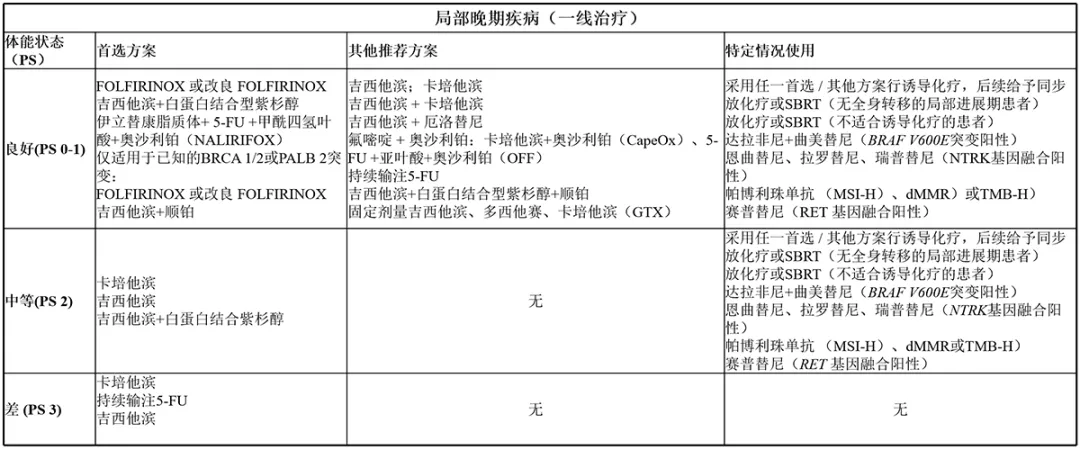
5
不可切除胰腺癌治疗方案
首先活检确认诊断和遗传突变的基因检测(之前未完成),根据是否存在黄疸进行不同治疗:
有黄疸:考虑胃空肠吻合术(有临床指征),疼痛时进行腹腔神经丛神经松解术。
无黄疸:考虑胆道旁路或SEMS±胃空肠吻合术(有临床指征),疼痛时进行腹腔神经丛神经松解术。
根据疾病进展情况,随后按照局部进展或转移性疾病方案治疗。
6
术后辅助治疗
首先完成术后基线评估(胸/腹/盆腔增强CT、CA19-9、遗传突变检测),再根据术前是否接受新辅助治疗进行不同辅助治疗方案:
(1)既往无新辅助治疗(无复发/转移)
优先推荐临床试验,或选择单纯化疗、化疗序贯放化疗(有临床指征)±后续化疗。
(2)既往新辅助治疗(无复发/转移)
考虑额外的化疗±考虑化放疗(有临床指征)。
(3)转移性疾病:按照转移性疾病方案治疗。
7
手术切除后出现复发的治疗
首先活检确认,并完成遗传突变检测(若未完成)及肿瘤组织分子谱分析。
(1)仅胰腺:外科会诊和多学科审查。
(2)胰腺手术部位:临床试验(首选)、全身治疗±放化疗、SBRT(如果之前未进行)、姑息治疗和最佳支持治疗。
(3)转移性疾病:按照转移性疾病的复发方案治疗。
8
转移性胰腺腺癌的一线治疗与维持治疗
若存在黄疸,需放置SEMS;同时完成遗传突变检测(若未完成)及肿瘤分子谱分析,后续按照体能状态进行不同治疗。
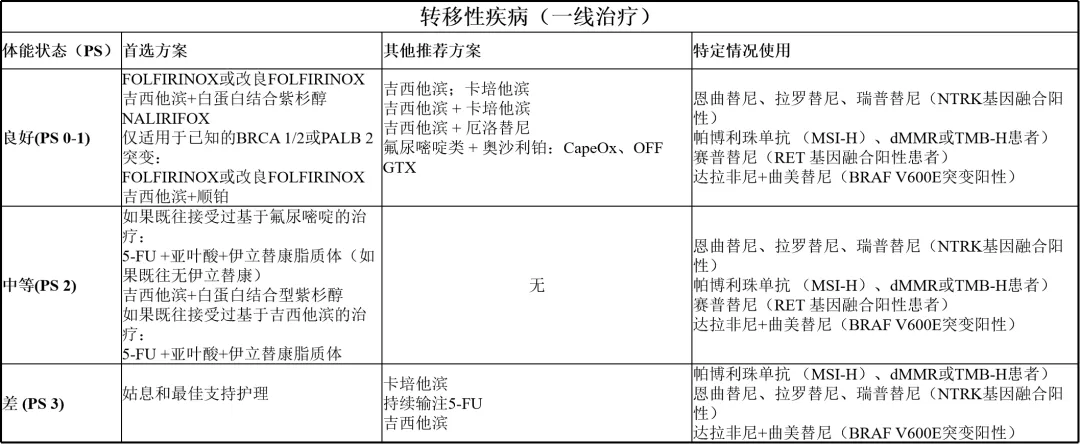

9
疾病出现进展后续治疗
如果没有足够的组织可用于分子分析,则考虑重新活检。
(1)PS良好/中等:临床试验(首选)、全身治疗(可能包括靶向治疗或免疫治疗)、RT治疗镇痛治疗难治性重度疼痛,后续进入姑息支持治疗或临床试验。
(2)PS差:姑息性和最佳支持性治疗并考虑单药化疗、靶向治疗或姑息性RT。
10
术后出现转移治疗
(1)完成初始治疗≥6个月
临床试验(首选)、既往重复全身治疗或替代全身治疗(既往未使用)、姑息治疗和最佳支持治疗。
(2)完成初始治疗<6个月
临床试验(首选),换用吉西他滨为基础的方案(若原方案为氟尿嘧啶类)、换用氟尿嘧啶为基础的方案(若原方案为吉西他滨类)、即往未使用全身治疗,或姑息支持治疗。
四、胰腺癌相关生物标志物检测
NCCN指南推荐对局部晚期/复发性疾病/转移性疾病的胰腺癌患者进行肿瘤/体细胞分子谱检测,以鉴定潜在的可治疗靶点,这些潜在的靶点包括:融合(ALK、NRG1、NTRK、ROS1、FGFR2、RET),突变(BRAF、BRCA1/2、KRAS、PALB2),扩增(HER2)、微卫星不稳定性(MSI)、错配修复缺陷(MMR)、肿瘤突变负荷(TMB)。RNA-NGS测序分析是检测RNA融合的首选方法,通过IHC±FISH的HER2过表达。
推荐使用肿瘤组织进行检测,当肿瘤组织无法提供时,可考虑使用循环中的细胞游离DNA(cf DNA)来替代。
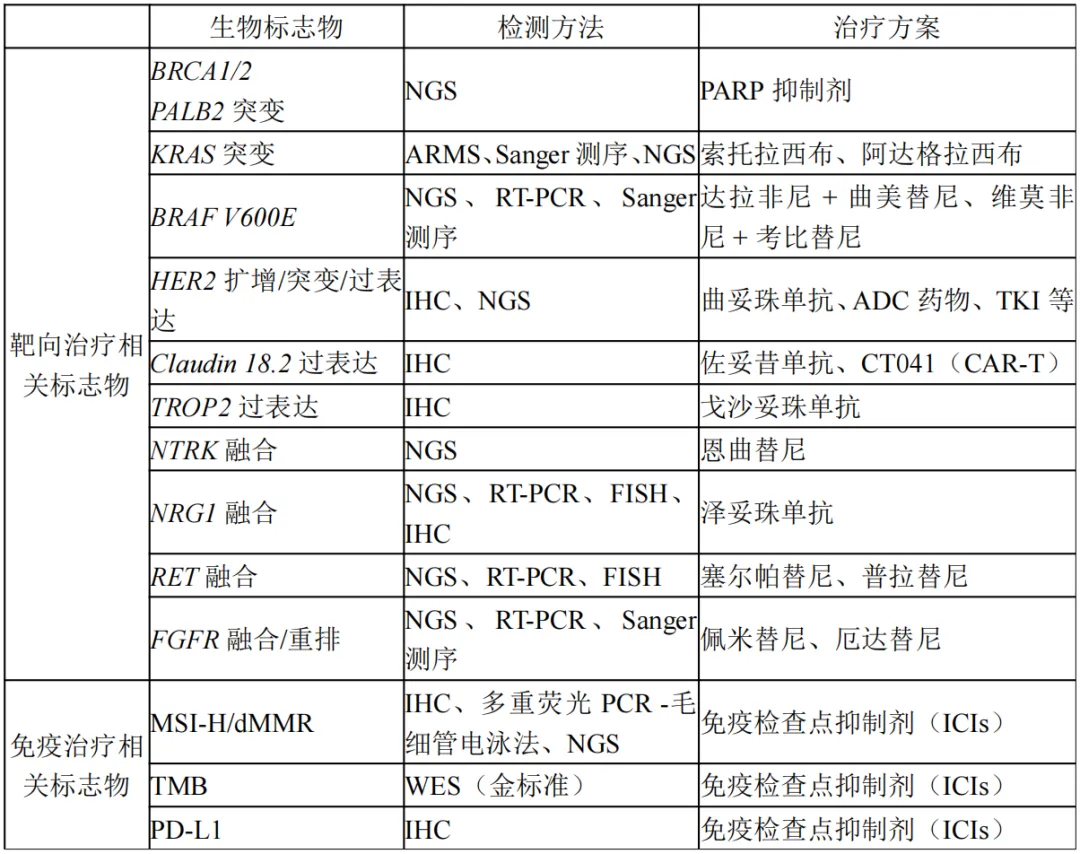
高通量测序(NGS)在胰腺癌诊疗中发挥着关键作用,可通过检测易感基因(如BRCA2、PALB2、ATM 等)突变实现早期风险评估与诊断;可检测BRCA1/2、KRAS、BRAF、HER2等靶向治疗靶点,同时检测MSI、TMB等免疫治疗标志物以指导胰腺癌的精准治疗;还能通过液体活检检测ctDNA监测治疗反应并提示复发风险。
伯科生物在国内已经建设了全流程国产化的高通量核酸合成与应用技术转化中心,建立了GMP厂房和ISO9001、ISO13485质量体系。已经为国内外数百家知名医院、科学研究机构、临床检验所开发了上千款Gene Panel(液相基因芯片),并配套完整的检测试剂,各项性能参数均与国际竞品相当或优于(详见附表1),在基因组、转录组、甲基化组及病原体的检测应用方向均有成熟的产品管线。
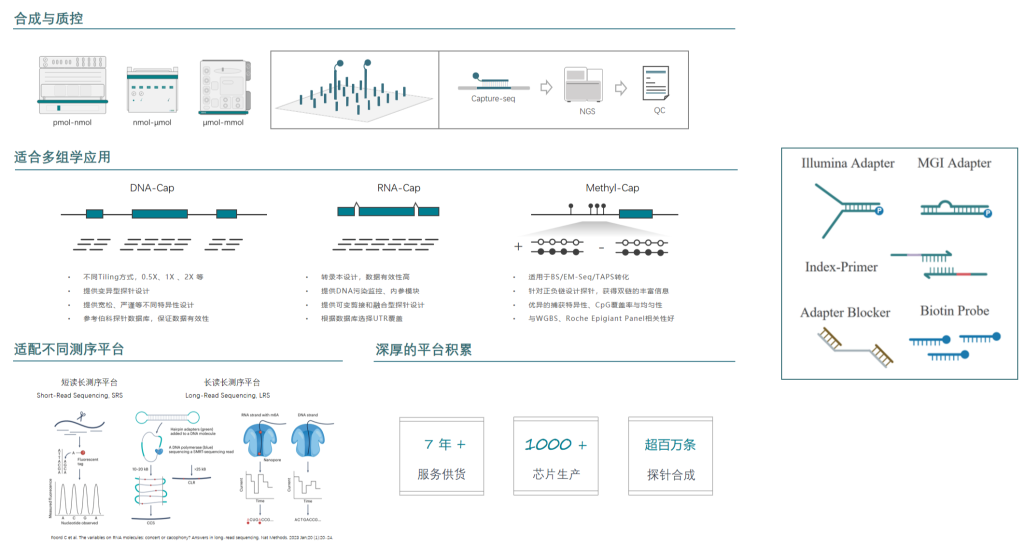
附表1: 产品简介
肿瘤液相基因芯片
伯科设计的TargetCap® OncoGene Plus Research Panel基于美国食品药品监督管理局(FDA)批准的用于肿瘤基因检测的FoundationOne CDxTM与MSK-IMPACTTM,其覆盖702个肿瘤相关基因编码区和34个基因的非编码区(融合基因),含有6个MSI和53个化药相关位点,探针覆盖2.32Mb区间。这些区域涵盖更多基因,检测范围更泛,涉及肿瘤高频突变、肿瘤易感、药物靶向、药物耐受等多种类型基因。
性能表现
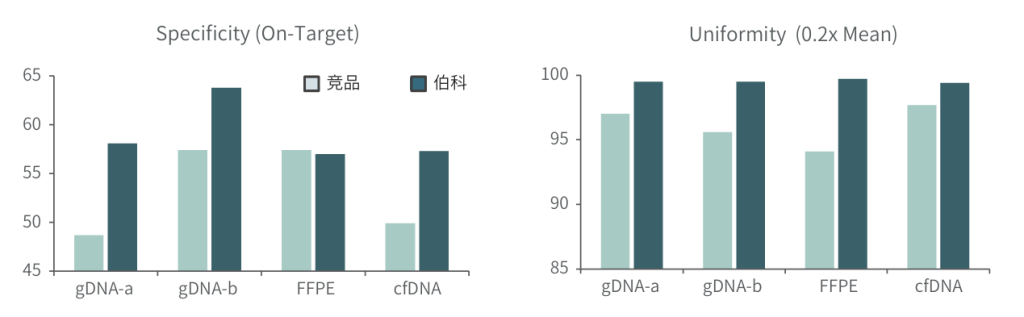
竞品评测
采用gDNA/cfDNA/FFPE/泛肿瘤800gDNA标准品文库,分别使用伯科商品化肿瘤大Panel-OncoGene Plus Research Panel与竞品肿瘤大Panel进行性能比较(二者大小相近),在捕获特异性上(On-Target)和覆盖均一性(0.2XMean)上,伯科均优于竞品。
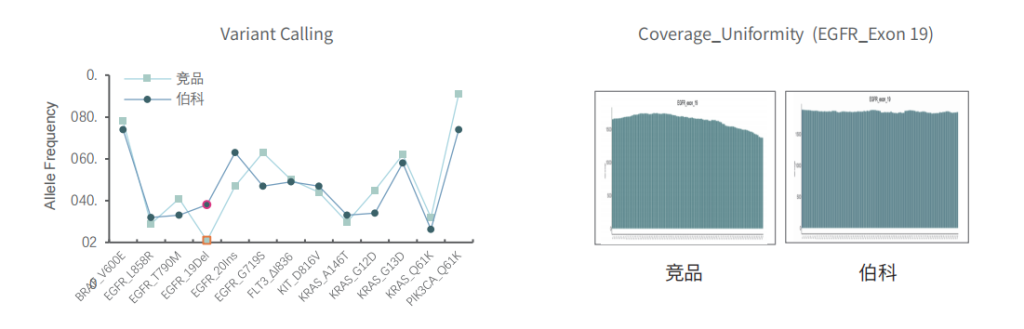
对于gDNA标准品,竞品测序35.9Gb,伯科测序19.6Gb,虽然伯科测序数据少,深度低,但二者的突变频率检出无明显差异,伯科对EGFR的19号外显子缺失变异的检出优于竞品。
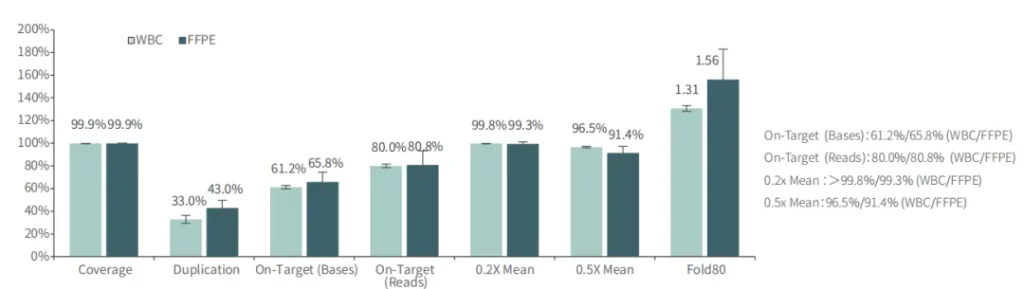
不同样本类型表现
对不同质量的gDNA样本 (WBC/FFPE, >150例),TargetCap® OncoGene Plus Research Panel表现稳定。
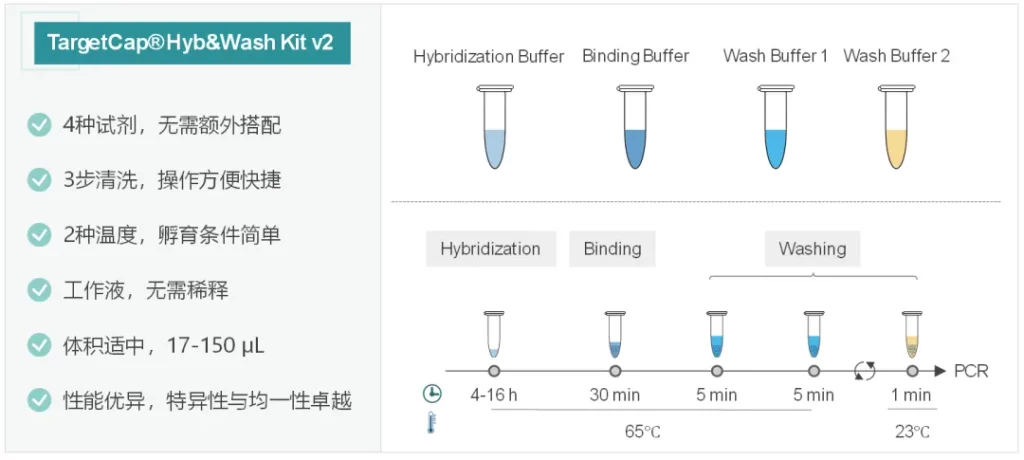
杂交与清洗试剂盒v2 简介
试剂盒概述
伯科杂交与清洗试剂盒v2 (TargetCap® Hybridization and Wash Kit v2,下文简称Hyb&Wash Kit v2)简化了试剂组分和操作流程,同时仍保持优异的捕获性能。Hyb&Wash Kit v2包含4种缓冲液组分,仅需3步清洗,操作流程更加便捷。
性能表现介绍
Ⅰ. 基本QC表现
使用NA12878和NA24694 gDNA标准品,采用三款不同大小的Gene Panel (650Kb、2.3Mb和42Mb) 对Hyb&Wash Kit v2 和 v1 进行比较测试。
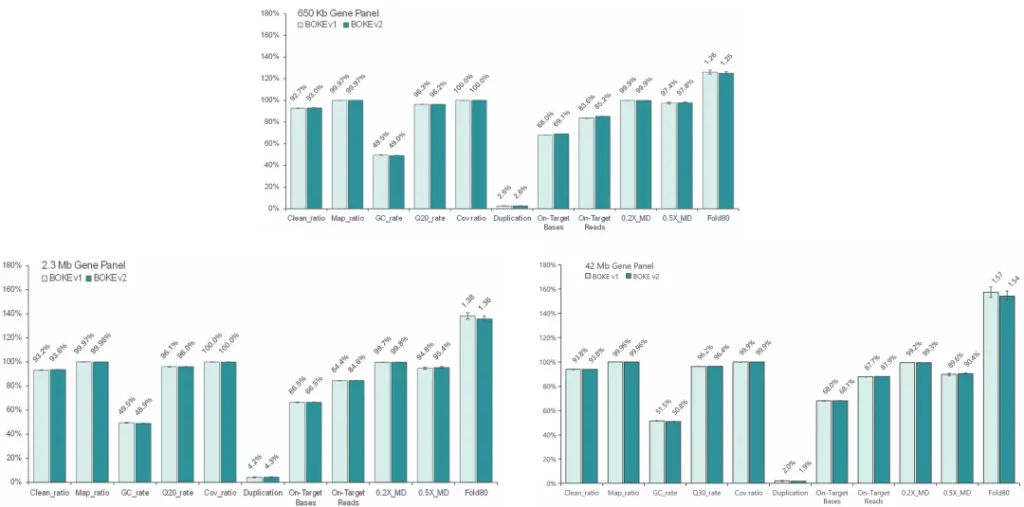
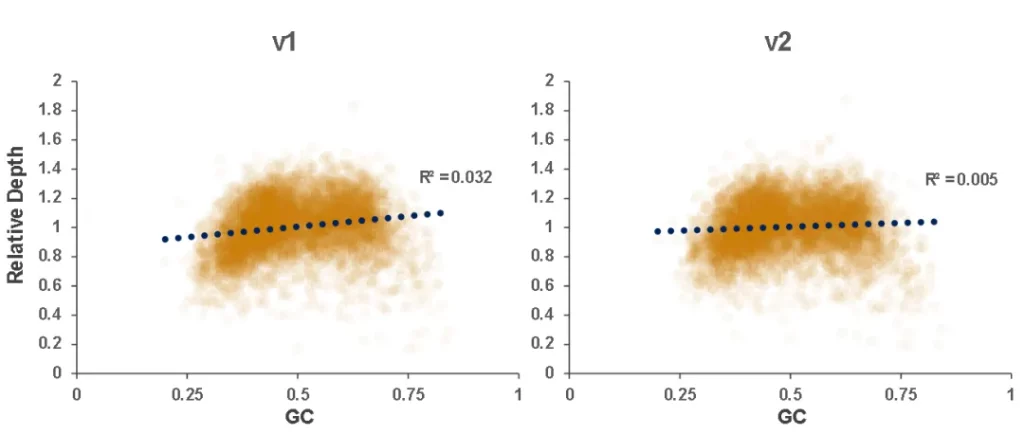
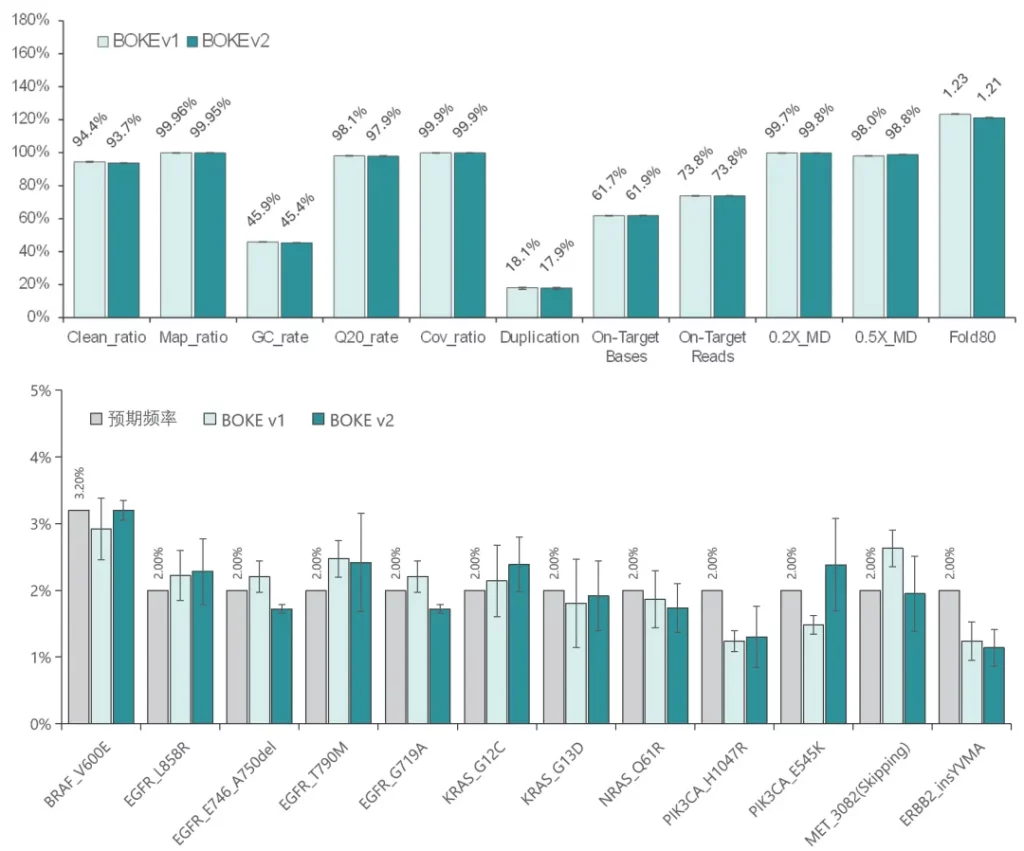
结果显示,在不同大小的Gene Panel中,对于杂交与清洗试剂盒的关键参数-中靶率和均一性,v2与v1试剂盒表现相当,v2试剂盒表现更好的均一性(0.2X_MD、0.5X_MD和Fold80)。
Clean_ratio、Map_ratio等基本参数两款试剂盒表现一致,由于v2试剂盒对低GC目标区域覆盖更佳,其GC_rate率略低于v1。
Ⅱ. 低频变异检测
使用肿瘤 SNV gDNA 标准品Ⅱ (GW-OGTM006) 对Hyb&Wash Kit v2的低频变异检测性能进行验证。GW-OGTM006 DNA标准品包含 EGFR、KRAS、NRAS、BRAF、PIK3CA、FGFR3、Her2、MET 等多个常见伴随诊断基因及位点,包含点突变、插入和缺失等多种变异类型。
采用300 Kb Gene Panel对该标准品进行捕获,捕获数据显示,v1与v2试剂盒的基本捕获性能表现相当,v2的中靶率与均一性略优于v1。同时,v1与v2试剂盒均能对12个已知变异准确检出。
参考文献:
1.胰腺癌精准检测与分子诊断中国专家共识(2025版),临床肿瘤学杂志,2025.
2.NCCN Clinical Practice Guidelines in Pancreatic Adenocarcinoma (2025 Version 2).


