Science | 完整解析LDLR基因错义变异的功能图谱,为HeFH患者的精准诊疗奠定坚实基础
- boke
- 2025-12-04
- 5:32 下午
一、研究背景
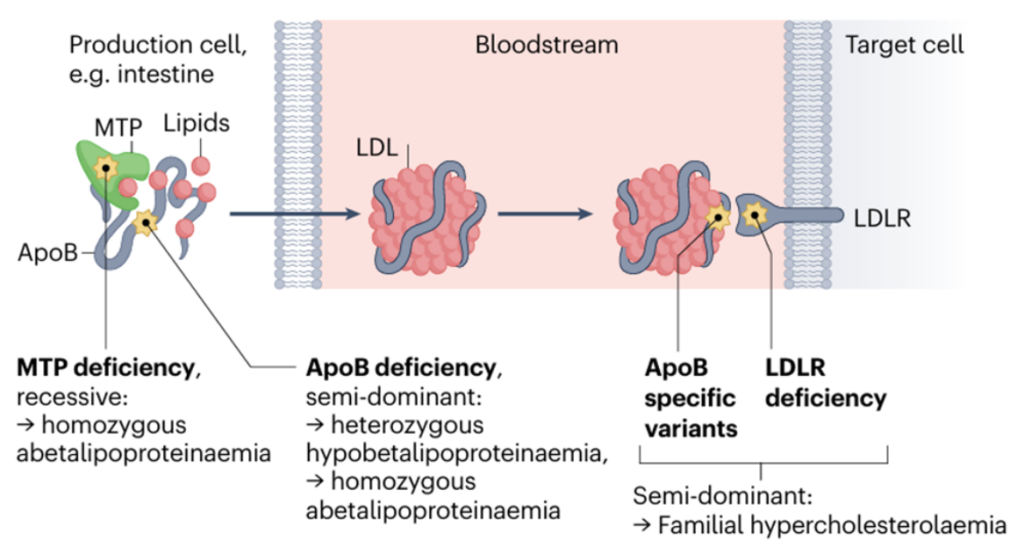
杂合子性家族性高胆固醇血症(Heterozygous familial hypercholesterolemia,HeFH)是一种常见且严重的遗传病,主要特征是血液中低密度脂蛋白胆固醇(LDL-C)水平过高。约80%的确诊HeFH病例是由LDL受体(LDLR)基因变异引起的,这种变异破坏了LDLR正常清除血液中LDL的功能,导致LDL堆积,极大增加早发性动脉粥样硬化性心血管疾病的风险。鉴定致病性LDLR变异有助于实现精准诊断,并能在标准脂质谱分析之外提供预后评估和治疗管理依据,同时通过级联筛查,有望识别出更多高危亲属。然而,目前大多数LDLR编码区变异缺乏明确的临床分类,这限制了HeFH的早期诊断及患者风险分层的开展。
二、研究方法
1
构建覆盖全长的LDLR变异文库
采用改良POP Code法,针对LDLR蛋白860个氨基酸位点分别设计NNK简并引物,构建覆盖约17,200种可能氨基酸替换的cDNA文库。
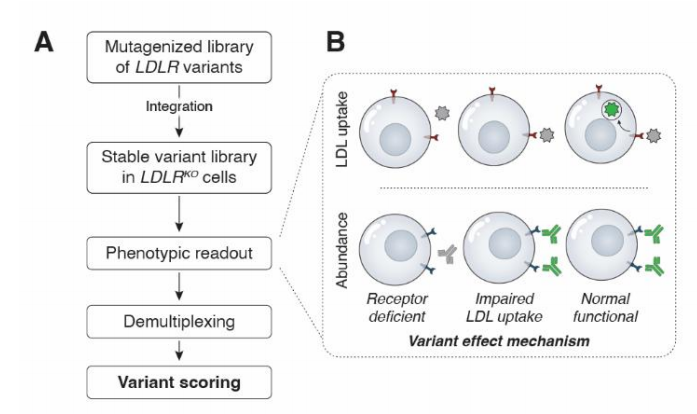
Fig. 1 (A)实验流程概述;(B)表型筛选。
2
细胞模型与高通量功能筛选
使用HeLa细胞系,通过CRISPR-Cas9敲除内源性LDLR,并利用Bxb1整合酶系统将LDLR变异cDNA文库稳定整合至基因组中,实现单细胞单变异表达。
3
通过流式细胞荧光分选技术(FACS)法对以下两个关键功能指标进行定量筛选
(1)LDL内化能力:使用pHrodo Green标记的LDL颗粒,其在包涵体中荧光增强,定量检测LDL摄取能力。
(2)细胞表面LDLR蛋白丰度:用流式细胞术进行检测。
4
功能评分与验证
通过比较筛选前后各变异barcode的丰度,计算每个变异的功能评分(Functional Score),评分范围-0.5至1.5,致病变异多集中在低分区(≤0),良性变异多在高分区(≥0.5)。
三、研究结果
1
LDLR序列-功能图谱构建与验证
本研究检测了16,677个(97%)可能的LDLR错义变异在LDL摄取方面的功能影响,以及16,105个(94%)变异在细胞表面表达水平的影响,并建立LDLR功能评分体系,范围-0.5至1.5。
多项分析验证了该数据集的整体质量,功能评分结果显示:
(1)无义变异与同义变异的评分分布存在显著差异(P<0.001),与预期一致。
(2)错义变异的评分呈双峰分布,说明部分变异会导致LDLR功能丧失,部分变异对功能无影响。
(3)在UK biobank和All of Us队列中,降低LDL摄取能力的替换变异在高次要等位基因频率区间分布较少,与预期分布一致。
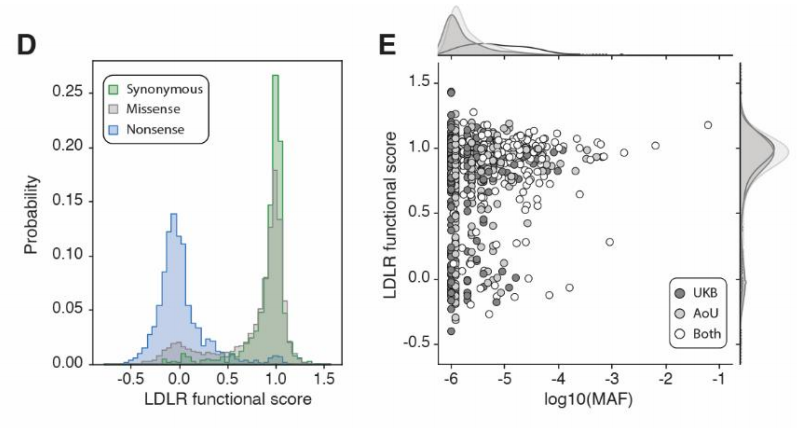
Fig. 2 (D) LDLR功能评分分布;(E) 功能分数,作为lgMAF(次要等位基因频率)的衡量标准。
2
序列-功能图谱与生物化学机制的关联
LDLR的配体结构域包含7个LA模块(LDL Receptor A-type Module,LA),传统上被认为是功能相似的重复单元,通过与ApoB100(LDL的主要结构成分)相互作用促进脂蛋白清除。
研究结果发现LA3、LA4、LA5、LA7对ApoB100(LDL主要结构成分)结合至关重要,其关键残基(如半胱氨酸、酸性Ca+ 配位残基、芳香族残基)对替换高度敏感。LA1、LA2、LA6替换变异在LDL摄取实验中表现出较高的耐受性,说明其在与ApoB100结合中作用有限。

Fig. 3 功能评分,用于测量LDLR中所有可能的氨基酸替换对LDL摄取的影响。
结合结构生物学数据,LA3–5和LA7与ApoB100的β-带紧密结合,而LA1、LA2和LA6结合较弱或未解析。
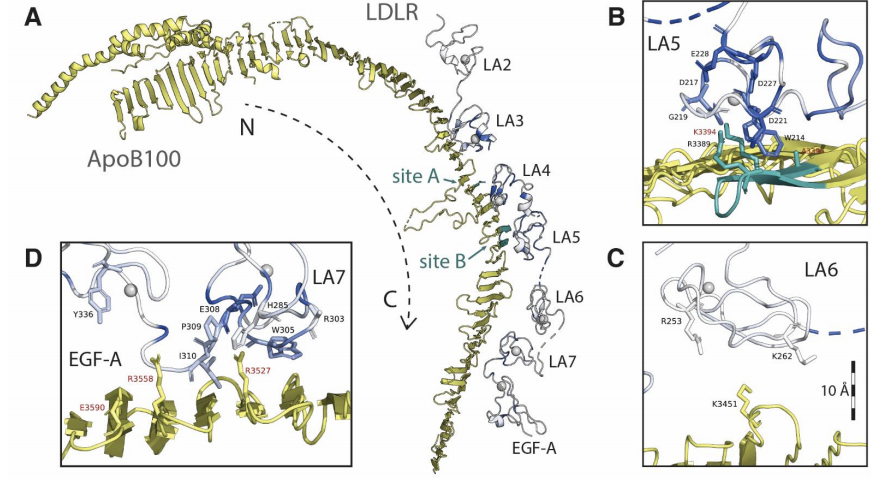
Fig. 4 功能评分捕捉LDLR-ApoB100相互作用的原子水平细节
在加入过量外源VLDL的条件下,LA2和LA6中部分原本耐受的变异表现出LDL摄取能力下降。这表明LA2和LA6可能在VLDL结合或竞争性抑制中发挥作用,不同LA模块在结合不同脂蛋白亚型时存在功能分工。
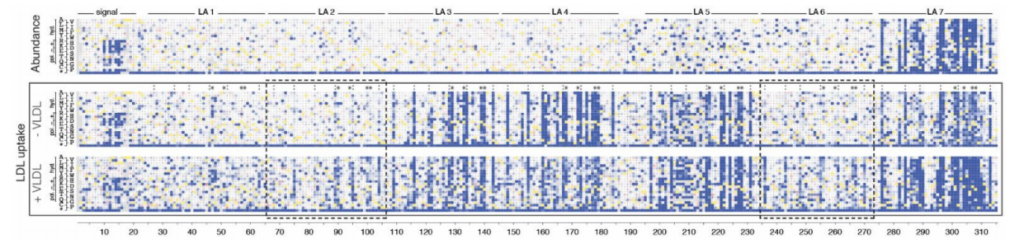
Fig. 5 LDLR配体结合域(LA 1 ~ 7)中所有可能的氨基酸替换变异的功能评分。(上)LDLR细胞表面丰度;(中)不含VLDL(-VLDL)的LDL摄取;(下)含4:1过量VLDL(+ VLDL)的LDL摄取。
除LA模块外,序列-功能图谱还捕捉到了其他已知的生物化学特征。例如,被认为介导受体构象变化的β-螺旋结构域对替换变异敏感;LDLR的跨膜结构域对极性残基替换高度敏感。细胞质尾部NPxY基序的破坏(该基序是受体-配体复合物内化所必需的)也会损害LDL摄取功能。
3
LDLR功能评分的潜在临床应用
(1)致病性变异的鉴定
在ACMG/AMP遗传变异分类系统下,本研究校准了各功能评分对应的致病性概率,为7287种LDLR错义变异提供了功能证据,其中包括约括约400种目前注释为意义未明变异,有望极大地促进这些变异的重新分类。
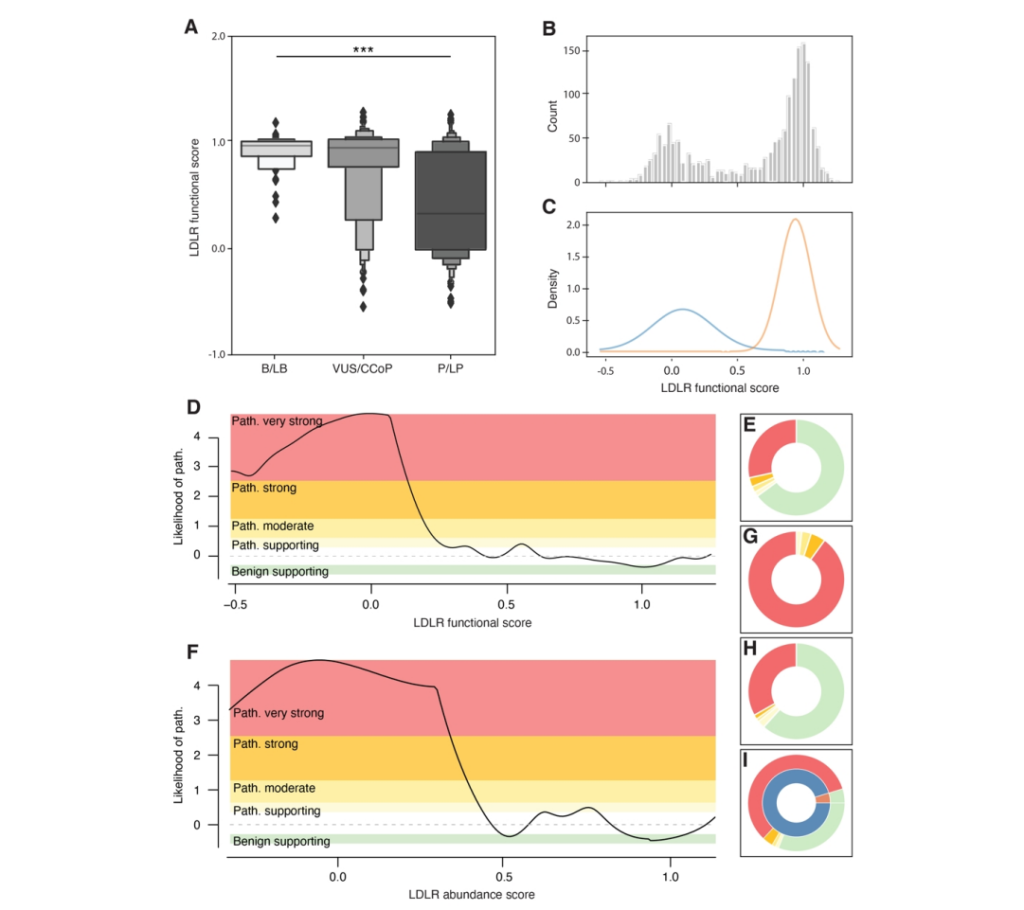
Fig. 6 功能评分为临床变异分类提供了证据。
(2)功能评分在HeFH风险量化中的潜在临床应用
功能评分能有效区分HeFH风险。携带破坏性变异的个体患HeFH的风险极高(OR=21.9,95% CI:14.4-33.2),与已知致病变异携带者相当(OR=22.5,95% CI:16.7-30.4);而携带正常评分变异的个体风险则很低(OR=1.3,95% CI:1.1-1.5),低于所有 LDLR 变异体携带者的总体风险(OR=1.6,95% CI:1.4-1.8),且与携带良性变异体(良性或可能良性)的参与者风险相当(OR=1.3,95% CI:1.1-1.5)。
即使在已知的致病变异携带者中,功能评分也能进一步进行风险分层。相较于所有致病性变异体携带者,携带破坏性评分致病性变异体的个体HeFH风险约高4倍(OR=44.3,95% CI:27.4-71.5),而携带正常评分致病性变异体的个体风险较低(OR=10.5,95% CI:6.0-18.3)。结果表明,定量功能评分可补充现有变异体致病性注释,更精准地推断HeFH风险。
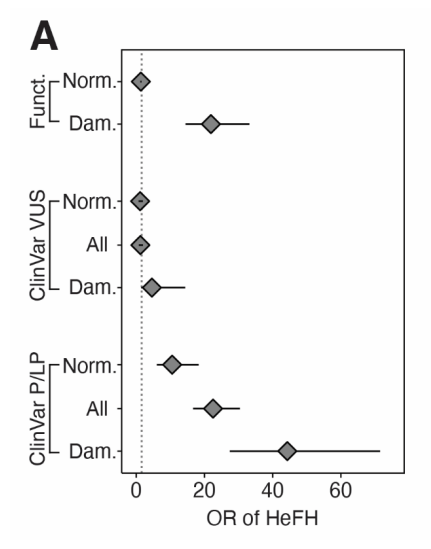
Fig. 7. 功能评分有助于HeFH风险的量化。
(3)功能评分在HeFH诊断中的潜在临床应用
为进一步推动实验结果向临床转化,基于荷兰临床脂质网络(Dutch Lipid Clinic Network,DLCN)诊断标准,研究者提出:功能评分≤0.04可作为“功能性突变”的阈值,其对应5%的假阳性率。在UK Biobank中筛选出携带罕见LDLR编码区变异体的参与者,应用此阈值,可将UK Biobank中符合明确HeFH诊断标准的携带未注释变异个体数量增加10倍以上,显著提高了诊断率。
每一项明确的变异体分类均可支持级联筛查,有望识别出更多高危亲属(约50%的一级亲属和25%的二级亲属),并降低其患心血管疾病风险。
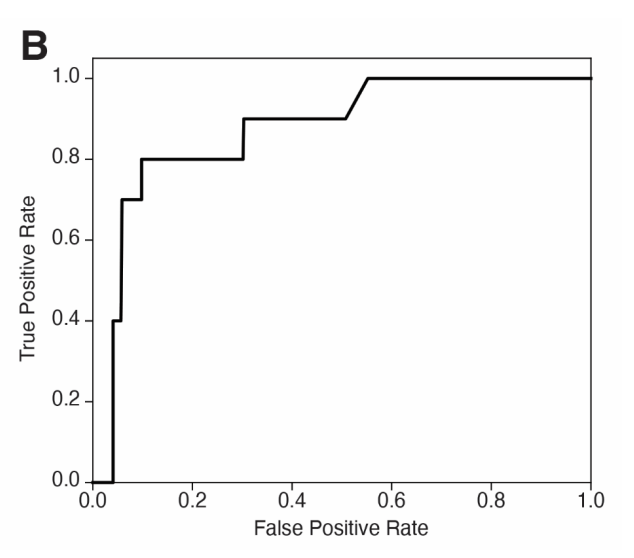
Fig. 8. 功能评分有助于HeFH临床诊断。
(4)预测HeFH相关表型的潜在价值
基于UK Biobank数据,功能评分与血脂异常表型显著相关,包括低密度脂蛋白胆固醇(LDL-C)升高(P=0.01)和降胆固醇药物的使用(P=0.02)。进一步分析了血管健康和心血管疾病相关标志物,发现与携带正常评分变异体的参与者相比,携带破坏性变异体的参与者发生主动脉瓣狭窄(OR=2.1,95% CI:1.2-3.7)或颈动脉内中膜厚度处于高五分位数(OR=2.2,95% CI:1.1-4.3)的风险更高。
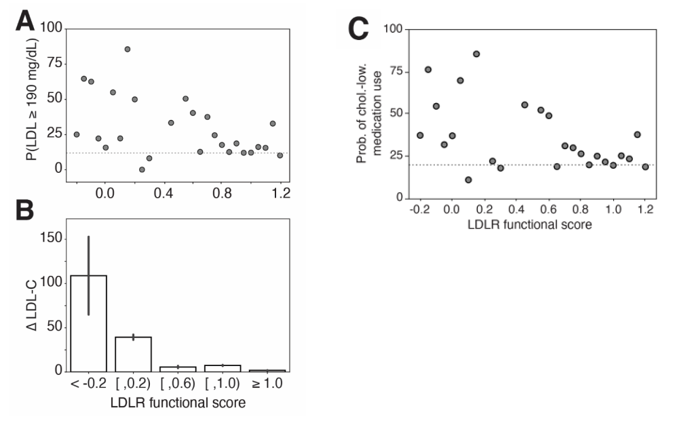
Fig. 9. 功能评分与血脂异常表型显著相关。
(5)功能评分与多基因风险评分(PRS)联合应用
研究首次在大规模人群中系统展示了LDLR功能评分与PRS在风险预测中的协同作用。结果显示PRS与LDLR功能评分在预测高脂血症和冠心病风险中具有累加效应:同时携带功能丧失型LDLR变异和高PRS的个体,其高脂血症和冠心病风险最高,且发病年龄更早
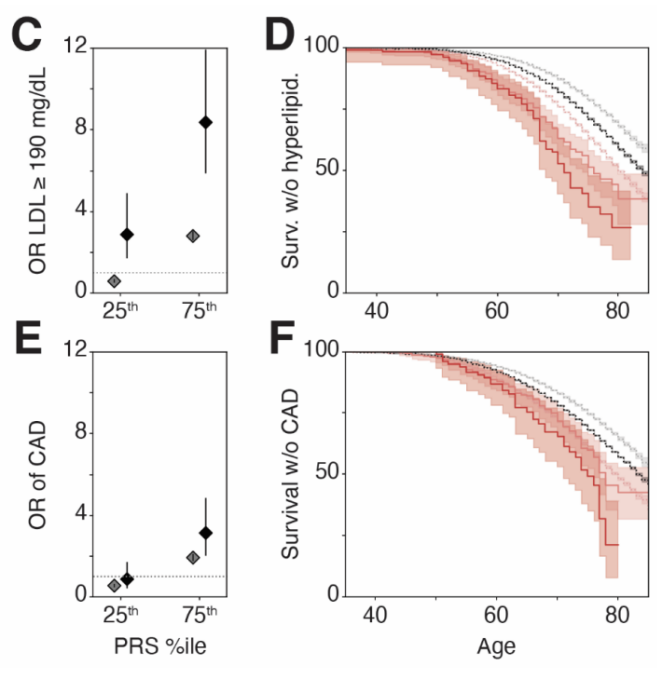
Fig. 10. LDLR功能评分与PRS在风险预测中的协同作用。
(6)跨人群适用性
在更具种族多样性的All of Us队列中重复分析,得到了与UK Biobank一致的结果,在种族和祖先背景多样化的人群中,LDLR 功能评分仍具有改善HeFH风险推断的潜力。
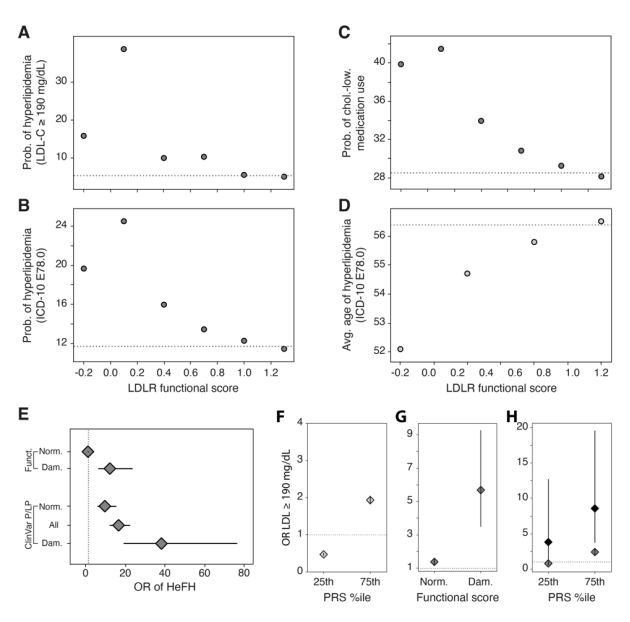
Fig. 11. 基于LDLR变异功能评分和多基因风险评分推断All of Us参与者表型。
四、研究意义与局限性
1
研究意义
(1)本研究建立了科学、可靠的LDLR功能评分体系,可精准区分LDLR基因变异的致病性,明确了配体结合域和EGF-A结构域是变异的高风险区域,关键位点(如E228、D217、R3558等)的变异可通过破坏配体结合、受体内化等过程导致LDLR功能缺陷。
(2)LDLR功能评分与HeFH的发病风险、血清LDL-C水平及降脂治疗响应密切相关,可作为HeFH精准诊断、风险分层和治疗方案优化的分子标志物,显著提升HeFH临床诊疗的精准度。
(3)功能评分结合多基因风险评分(PRS)能更准确地预测HeFH发病风险,为遗传咨询和个性化治疗提供依据。
2
局限性
(1)检测依赖于cDNA,未涵盖非编码变异体,也未捕捉编码变异体在剪接等方面的影响。
(2)细胞表面丰度检测中,某些替换变异可能恰好构成了检测抗体所识别的表位,从而影响了检测结果。
(3)检测中使用的细胞模型为HeLa细胞,无法完全模拟LDLR发挥作用的生理条件。
(4)仅评估了LDLR的两种功能,而LDLR可能还通过其他机制影响动脉粥样硬化。
五、总结
该研究通过构建LDLR基因近乎完整的错义变异功能图谱,系统揭示了其不同结构域对氨基酸替换的敏感性差异。基于大规模人群队列数据,研究证实功能评分与变异在人群中的频率呈显著负相关,并成功将定量功能数据转化为符合ACMG/AMP指南的临床证据强度,为超过7000个变异(包括约400个VUS)提供了分类依据。另外该研究将功能评分与多基因风险评分(PRS)相结合,能进一步改善高胆固醇血症的风险推断。
序列-功能图谱既再现了已知的生物化学机制,又提供了新的功能见解,同时为临床变异解读提供参考,为HeFH患者的精准诊断、风险分层和个性化管理奠定了坚实基础。
参考文献
1. Tabet R D , et al.The functional landscape of coding variation in the familial hypercholesterolemia gene LDLR.[J].Science (NewYork,N.Y.),2025,eady7186.DOI:10.1126/SCIENCE.ADY7186.
2. Zschocke J, Byers PH, Wilkie AOM. Mendelian inheritance revisited: dominance and recessiveness in medical genetics. Nat Rev Genet. 2023 Jul;24(7):442-463. doi: 10.1038/s41576-023-00574-0. Epub 2023 Feb 20. PMID: 36806206.


