MRD检测的研究进展与临床应用
- boke
- 2025-08-26
- 3:48 下午
随着检测技术的进步,MRD 在血液系统恶性肿瘤和实体瘤中的临床价值日益凸显,但在标准化、临床普及等方面仍面临挑战 [12]。
一
MRD 检测技术及其发展
MRD检测正朝着更高灵敏度、更低成本、多组学整合和临床实用性方向发展,为肿瘤个体化治疗提供了重要工具。
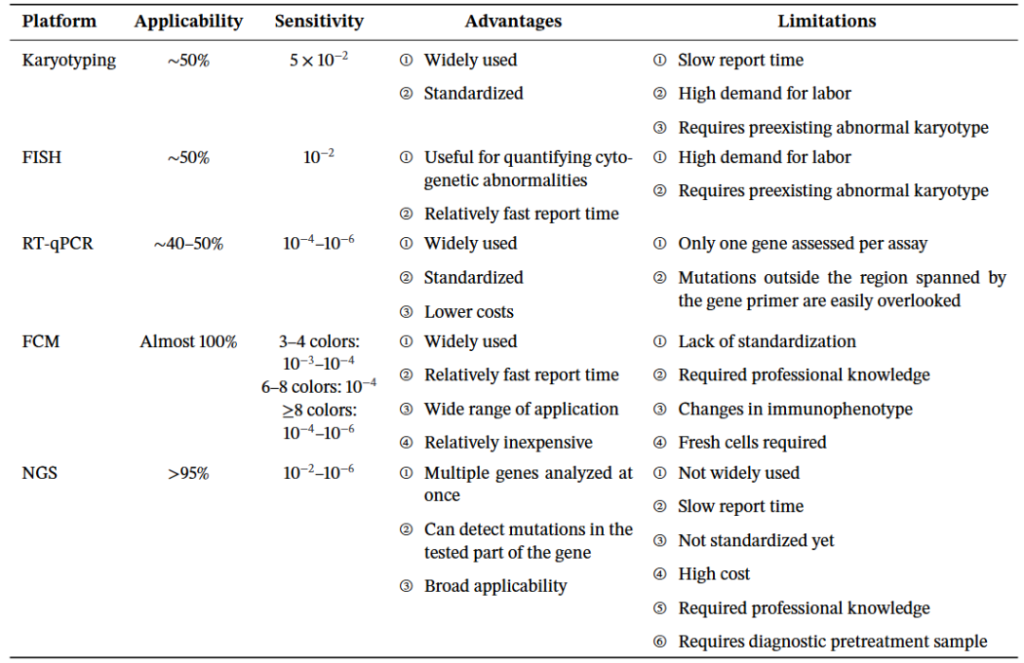
Table1 Comparsion of different MRD detection methods
(一)传统检测技术
1. 多参数流式细胞术(MFC):通过识别恶性细胞异常表型标志物检测 MRD,具有操作快速、成本较低的优势。但该技术存在标准化不足、依赖操作者经验等局限 [2,8]。
2.聚合酶链反应(PCR)技术:包括实时定量 PCR(qPCR)、等位基因特异性寡核苷酸 qPCR(ASO-qPCR)等,通过检测肿瘤特异性基因重排或融合片段实现 MRD 定量。但其适用性受限于特定遗传异常,且存在标准化难题 [8,49]。
(二)新型检测技术:
1.下一代测序(NGS)
通过高通量测序追踪克隆特异性突变或基因重排,敏感性达 10⁻⁵~10⁻⁶,可同时评估克隆演化。但该技术成本高、生物信息学分析复杂,标准化仍需完善 [4,21]。
NGS作为一种有效技术手段,用于ctDNA检测已受到国内外专家认可并推荐。其技术路线基于是否需要对肿瘤组织样本检测分析分为两大类:肿瘤知情(Tumor-Informed)策略和肿瘤非知情(Tumor-Agnostic)策略[3]。其中,Tumor-Informed按照MRD Panel的类型又分为固定、定制和半固定三种,并可通过多重PCR和液相基因芯片靶向捕获结合NGS技术实现。
2025年发表的一篇综述,对Tumor-Informed策略以及Tumor-Agnostic策略进行比较,探讨关于这两种方法在敏感性、特异性、成本效益及临床可行性方面孰优孰劣[3]。
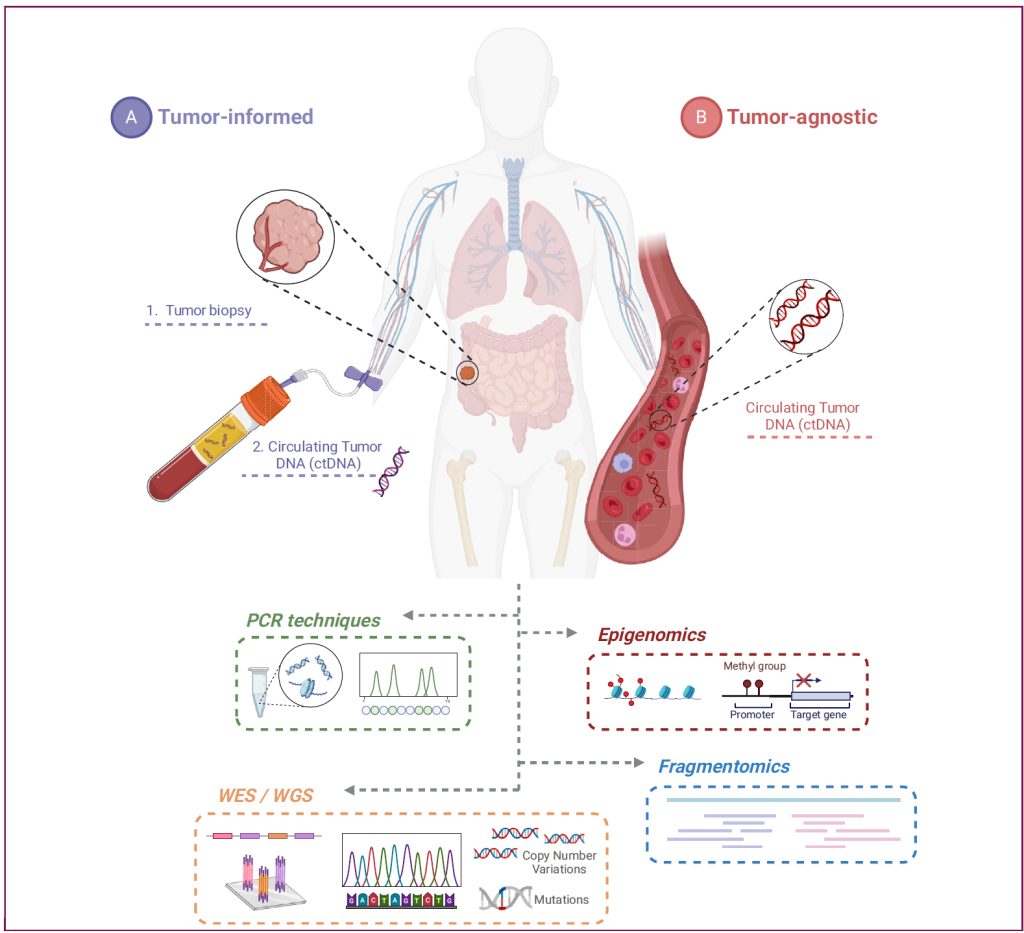
Figure 1. Overview of the tumor-informed and tumor-agnostic assays, including the type of sample required for each approach and the available technologies for the ctDNA analysis, such as PCR, genomic and epigenomic sequencing and fragmentomics.
2.数字 PCR(dPCR):通过绝对定量肿瘤特异性片段提高检测精度。
在慢性粒细胞白血病(CML)中可增强 MRD 监测准确性,助力酪氨酸激酶抑制剂(TKIs)停药决策 [24]。
在 ALK 阳性间变性大细胞淋巴瘤(ALCL)中,dPCR 对 NPM-ALK 转录本的检测敏感性达 10⁻⁵,且质控较 qPCR 更简便 [29]。
二
MRD 在不同癌症中的临床应用
2024年4月18日,陈俊仁团队在《Leukemia》发表观点性文章 [10]。该研究汇总2013年1月至2023年10月发表在17种高影响因子医学期刊的1510篇MRD相关论文,聚焦于能阐明MRD和复发率之间关系的数据,最终筛选了符合严格数据要求且队列人数>50的95篇论文进行深度分析,仅18篇论文有对比数据可用于分析基于MRD的治疗方案如何影响复发率。

研究结论
预测复发:MRD 阳性与癌症复发高度相关(血液肿瘤 OR=3.5,实体瘤 OR=9.1),但阳性预测值(PPV)波动大(血液肿瘤 PPV 55%(IQR 40-70%),NPV 77%;实体瘤 PPV 75%,NPV 88%。)。
指导治疗:理论上,MRD 阴性可降阶治疗(如减少化疗 / 移植,5篇论文的数据支持);阳性需升阶治疗(如强化疗 / 移植,7篇论文的数据支持)。
临床转化:仅儿童 ALL 有明确降阶治疗指南,其他癌种需等待 III 期 RCT 结果(如 CTONG2201、CINTS-R 研究)。
(一)血液系统恶性肿瘤
01
多发性骨髓瘤(MM)
MRD 阴性是独立预后因素,与更长的无进展生存期(PFS)和总生存期(OS)相关 [6,19]。抗 CD38 单克隆抗体(如伊沙妥昔单抗、达雷妥尤单抗)联合治疗可提高 MRD 阴性率 [6];维持治疗阶段的 MRD 动态监测有助于指导个体化治疗 [7]。下一代流式细胞术(NGF)和NGS 是主要检测方法,灵敏度均可达 10⁻⁵~10⁻⁶[5,9,25]。
2025年4月7日,来自纳瓦拉大学应用医学研究中心的Bruno Paiva教授在Nature Reviews Clinical Oncology上发表综述,概述了多发性骨髓瘤MRD评估的当前进展和挑战[13]。

从方法学角度来看, MRD评估在MM中已准备好进入临床应用黄金期。大量证据强调了使用高灵敏度NGF和NGS技术确定的MRD状态在评估治疗效果及因此预测患者预后的价值。
研究要点
MRD评估已在MM的临床管理中迎来成熟应用阶段:临床试验中产生的大量高质量、标准化的MRD数据已促使MRD阴性被接受为加速MM治疗药物监管批准的早期终点
MRD 阴性的完全缓解(CR)可被视为多发性骨髓瘤中 CR 的新定义。
新方案在诱导更深层次、更持久的 MRD 阴性应答方面的疗效,与患者生存延长明确相关。
2024 年,针对MRD 阴性作为支持多发性骨髓瘤新疗法加速审批的早期终点这一作用,已达成共识。此外,由于残留疾病通常存在于检测限(LOD)以下的水平,部分无法检测到MRD的患者仍然会出现疾病复发,作者更倾向于使用“MRD无法检测”这一术语,而非“MRD阴性”。
MRD 与侵入性较小的外周血残留病(PRD)检测的序贯应用,或许会成为疗效评估的下一个前沿方向。6个月PRD可能与每24个月的MRD相关;而PRD复发将自动意味着MRD阴性的“失效”。
今年,ASCO上法国多发性骨髓瘤协作组报告了MIDAS研究的结果,该研究评估基于 MRD 指导的巩固治疗策略对适合自体干细胞移植(ASCT)患者的作用,或许具有临床价值[14]。

研究方法
791例新诊断骨髓瘤接受6周期Isa-KRd。
MRD 阴性组(经下一代测序评估,10⁻⁵灵敏度下每 10 万个正常细胞中癌细胞数 <1):分为 “ASCT+2 周期 Isa-KRd” 组(ASCT 组)或 “6 周期 Isa-KRd” 组(Isa-KRd 组)。
MRD 阳性组(10⁻⁵灵敏度下 MRD 阳性):分为 “序贯 ASCT(短期内 2 次移植;序贯 ASCT 组)” 或 “ASCT+2 周期 Isa-KRd” 组(单次 ASCT 组)。
主要终点:维持治疗前、10⁻⁶更高灵敏度 下的 MRD 阴性状态。
研究结果
MRD 阴性亚组(485 例):ASCT 组和 Isa-KRd 组在维持治疗前、10⁻⁶灵敏度下 MRD 阴性的比例为 86% vs. 84%(校正相对风险 1.02,95% 置信区间 [CI] 0.95~1.10,P=0.64),无显著差异。
MRD 阳性亚组(233 例):序贯 ASCT 组和单次 ASCT 组在维持治疗前、10⁻⁶灵敏度下 MRD 阴性的比例为 32% vs. 40%(校正相对风险 0.82,95% CI 0.58~1.15,P=0.31),亦无显著差异;且序贯 ASCT 组中 15% 患者未完成第二次移植。
安全性:巩固治疗期间,5 例疾病进展、2 例非疾病进展相关死亡(均发生在 Isa-KRd 组或序贯 ASCT 组),未发现新安全信号。
随访:ASCT 组和 Isa-KRd 组中位随访 16.8 个月,序贯 ASCT 组和单次 ASCT 组为 16.3 个月。
02
急性淋巴细胞白血病(ALL)
MRD 是关键预后标志物,诱导治疗后及造血干细胞移植(HSCT)后 MRD 阴性患者结局更优 [4,28]。在儿童 ALL 中,HSCT 前高 MRD 负荷与复发风险增加相关,而术后 MRD 监测可预测复发并指导抢先治疗 [28];NGS 在识别分子残留病灶灶和克隆演化方面优于传统方法,对 CAR-T 细胞治疗后复发的预测价值高 [4,22]。
陈俊仁和竺晓凡团队2023年在《Leukemia》杂志发文,聚焦于白血病治疗后MRD检测结果的准确性问题 [15]。

研究内容
传统 MRD 检测结果(MRDconventional)在低水平 MRD 检测时,受抽样误差影响准确性存疑。通过对 883 例儿童ALL数据的分析,提出基于贝叶斯推理的MRDworst – case评估方法。
研究结果
在MRDconventional <0.01%时,MRDworst – case对复发风险的预测能力显著优于MRDconventional,且结合诊断时的复发风险评估,能更好地对 ALL 患儿进行危险分层。
研究结论
MRDworst – case可改善 ALL 复发风险预测,对临床治疗决策有重要意义。
近期《Blood Advances》杂志发表了一篇关于成人ALL MRD检测的综述文章,总结了MRD检测应用中的常见临床问题,并给出合理化建议[17]。

要点:
核心定位:MRD 是成人 ALL 预后评估和治疗决策的关键指标,其价值受检测方法、标本来源、评估时机、疾病特征(如细胞分子风险)共同影响;基于 NGS 的 IG/TR 检测(灵敏度 1×10⁻⁶)是目前最优检测方法之一,尤其适用于 B 细胞 ALL。
7 大临床问题核心建议
(1)最优 MRD 检测方法:B 细胞 ALL 优先选 IG/TR NGS;Ph 阳性 ALL 中 IG/TR NGS 与 BCR:ABL1 RT-PCR 互补;T 细胞 ALL 中 IG/TR NGS 需结合 MFC。
(2)适宜标本来源:骨髓优先(至 MRD 阴性),后续可换外周血 NGS 监测;髓外病变可尝试外周血检测。
(3)评估时机与频率:一线治疗:诱导后评估,随后 2~3 年每 3~4 个月 1 次;HSCT/CAR-T 后:前 1 年每 2~3 个月 1 次。
(4)指导一线治疗 HSCT 决策:标危 MRD 阴性者不推荐 HSCT;高危 MRD 阴性者个体化决策;MRD 阳性者优先清除 MRD 后 HSCT。
(5)指导挽救治疗 HSCT 决策:复发 / 难治性 ALL 无论 MRD 反应均需 HSCT/CAR-T 巩固;CAR-T 后 MRD 阳性者需进一步干预。
(6)指导非移植干预:MRD 持续 / 复发者需 MRD 导向治疗,优先博纳吐单抗(未接受过 CD19 靶向治疗者)。
(7)NGS-MRD 报告解读:低于 LOD 的低水平 MRD 需结合序列独特性和动态变化判断;T 细胞 ALL TR 序列解读需谨慎。
关键趋势:NGS-MRD 推动 ALL 治疗从 “经验性” 向 “精准导向” 转变,可识别无需 HSCT 的低危患者和需早期干预的高危患者;
持续性研究:未来需进一步探索极低水平 MRD(10⁻⁴~10⁻⁶)的干预价值,以及新型治疗方案中 MRD 的动态变化意义,以提高治愈率。
03
慢性淋巴细胞白血病(CLL)
今年发表的篇关于CLL的综述通过系统分析 2000-2024 年相关研究,针对 7 个核心临床问题提出专家建议,并指出:MRD是ALL预后的关键预测因素,其结果不仅能评估复发风险,还日益用于指导治疗决策。然而,MRD 的临床意义受疾病特征(如细胞分子风险)、检测特征(如灵敏度、样本来源、检测时机)等多重因素影响,增加了临床决策的复杂性[21]。
04
急性髓系白血病(AML)
MRD 阴性患者复发率低、生存率高,欧洲白血病网(ELN)推荐将 MRD 纳入治疗反应评估 [26]。MFC 是最常用方法,NGS 和 qPCR 可作为补充,多技术联合可提高预后价值。MRD 指导的风险适应性治疗(如中危患者 MRD 阳性行异基因 HSCT)可改善结局 [45]。
AML中,即使患者达到CR, MRD仍可通过基因突变(如NPM1或FLT3-ITD)检测到,并与复发风险显著相关[22,23]。
今年发表在《Cancer》上的一篇单中心回顾性研究,探讨了在异基因造血干细胞移植(HSCT)围移植期(移植前及移植后早期),伴有赖氨酸甲基转移酶 2a 重排(KMT2Ar)的成人急性髓系白血病(AML)患者中,可测量残留病(MRD)动态变化的影响[26]。

研究方法
纳入 2015 年至 2024 年间接受 HSCT 的 144 例伴有 KMT2Ar 的成人 AML 患者。入组患者需在 HSCT 后至少 3 个月无复发存活,采用实时定量聚合酶链反应检测 MRD。
研究结果
根据移植前后的 MRD 状态,队列被分为四组:MRD 阴性 / 阴性组(n=81)、MRD 阴性 / 阳性组(n=2)、MRD 阳性 / 阴性组(n=43)和 MRD 阳性 / 阳性组(n=18)。三组的 3 年总生存率(OS)、无白血病生存率(LFS)和累积复发率(CIR)存在显著差异(均 p<0.001):
MRD 阴性 / 阴性组预后最佳(OS 88%、LFS 85%、CIR 10%);
MRD 阴性 / 阳性组和 MRD 阳性 / 阳性组预后最差(前者 OS 0%、LFS 0%、CIR 100%;后者 OS 29%、LFS 31%、CIR 69%);
MRD 阳性 / 阴性组预后中等(OS 63%、LFS 58%、CIR 32%)。
围移植期 MRD 动态变化是独立影响因素,可区分不同死亡和复发风险的患者群体。在预测 CIR(0.68 vs. 0.58 vs. 0.56)、LFS(0.74 vs. 0.69 vs. 0.64)和 OS(0.73 vs. 0.68 vs. 0.66)时,围移植期 MRD 动态检测的 C 统计值均高于单独的移植前或移植后 MRD 检测。
研究结论
与单时间点 MRD 评估相比,围移植期 MRD 动态变化具有更优的预后准确性。
05
其他血液肿瘤
在 AL 型淀粉样变性中,MRD 阴性与更高心脏和肾脏缓解率及更好 PFS 相关 [8];在 HCL 中,MRD 清除可改善长期结局,MFC 和针对 BRAF V600E 的分子检测是主要手段 [40,41]。
(二)实体瘤
2025年发表在Nat Rev Clin Oncol的综述,对利用ctDNA检测和监测实体瘤患者 MRD 的当前研究进展进行分析,并探讨了 ctDNA 指导的 MRD 检测与特征分析如何有望开启新型 “辅助治疗后疗法” 的新纪元[27]。

灵敏的血液检测方法能够检测到极低浓度的ctDNA,浓度可低至 < 10 ppm。
检测极低浓度的 ctDNA 是检测实体瘤患者MRD的必要条件。
MRD 检测可与无进展生存期、总生存期等临床结局相关联。
基于 ctDNA 的 MRD 检测可比基于影像的复发检测早数月,具体取决于肿瘤类型和分期。
可通过 ctDNA 检测到的 MRD 向显性转移的转变,可能取决于残留肿瘤负荷和宿主反应(例如抗肿瘤免疫)。
目前需要对实体瘤且 MRD 阳性的患者开展介入性临床研究,以评估何种治疗可清除这些患者的 MRD。
01
乳腺癌
乳腺癌作为最早探索MRD术后风险分层的实体瘤之一,通过ctDNA动态追踪可优化术后管理,并为基于MRD基因特征的个体化治疗奠定基础,具有高风险患者分层(如:ctDNA阳性患者可优先纳入强化辅助治疗临床试验)的临床应用潜力[30]。
有研究证实ctDNA检测可在影像学复发前预警乳腺癌复发 [31],多项研究证实MRD状态对不同分子亚型(包括激素受体阳性、HER2阳性、三阴性乳腺癌)的预后和个体化治疗具有重要价值。
在 HR+/HER2 – 早期乳腺癌中,ctDNA 检测的 MRD 阳性患者远处复发风险高,44% 的 ctDNA 阳性患者存在可靶向基因组改变(如 PIK3CA 突变),且 PIK3CA 突变者无远处复发生存期(DRFS)更短[63] 。MRD 检测可指导辅助治疗升级或降级 [18]。
2024年的一项研究,采用了一种针对乳腺癌的个性化、肿瘤定制的ctDNA检测方法(SignateraTM),并评估其在乳腺癌患者长期随访中检测分子复发的敏感性[32]。

研究方法
共纳入 156 例原发性乳腺癌患者,在手术和辅助化疗后进行长达 12 年的临床随访。前瞻性每半年采集一次血液样本,回顾性利用基于原发肿瘤全外显子测序数据开发的 ctDNA 检测方法,通过超深度测序分析MRD。
研究结果
在 34 例复发患者中,个性化 SignateraTM检测在 30 例患者的临床或影像学复发前检测到 ctDNA(患者水平敏感性为 88.2%)。复发预测的领先时间最长达 38 个月(中位 10.5 个月,范围 0-38 个月);ctDNA 阳性与更短的无复发生存期(P<0.0001)和总生存期(P<0.0001)相关。
所有复发的三阴性乳腺癌患者(7/23 例)在中位 8 个月内(范围 0-19 个月)均出现 ctDNA 阳性;而 16 例未复发的三阴性乳腺癌患者在中位 58 个月的随访中(范围 8-99 个月)持续 ctDNA 阴性。
复发前检测为阴性的 4 例患者均为激素受体阳性(HR+)疾病;相反,122 例未复发患者中,有 5 例(均为 HR+)出现偶发的 ctDNA 阳性。
研究结论
术后连续 ctDNA 评估具有显著的预后价值,为更早的治疗干预提供了潜在窗口,且可能比当前的临床检测更有效。本研究证实,ctDNA 持续阴性的患者临床结局更优,这为乳腺癌患者提供了信心。对于部分 HR + 病例,即使 ctDNA 检测阳性,治疗管理决策仍可能需要结合连续监测结果。
02
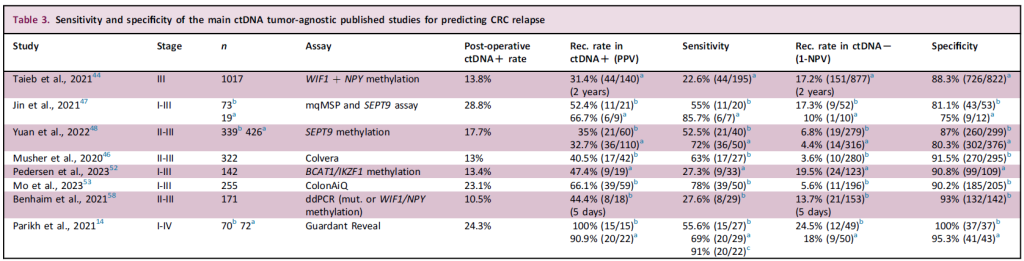
结直肠癌(CRC)
自2016年以来,越来越多的研究证实:ctDNA分析已成为检测CRC患者MR的微创工具。这一技术可实现动态风险分层、更早的复发检测及术后治疗优化。
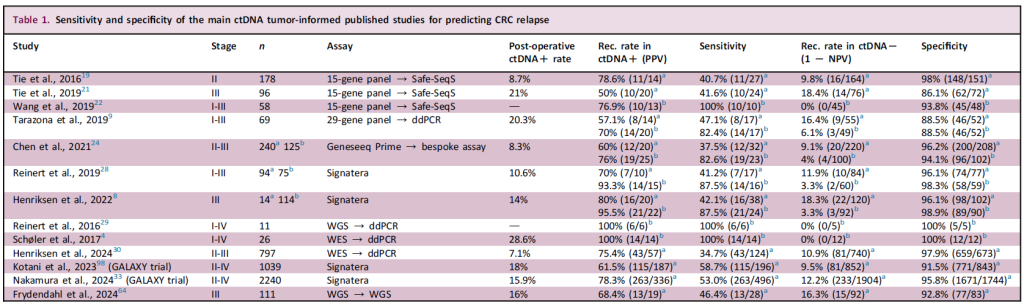
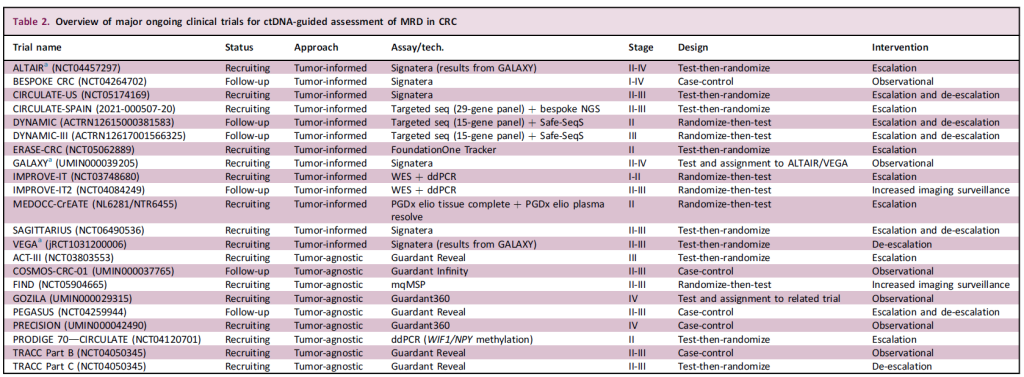
2022年发表在《新英格兰医学杂志》上的一项关于ctDNA在II期结肠癌辅助治疗中应用的研究(DYNAMIC试验),旨在评估 ctDNA 指导的治疗策略是否能在不增加复发风险的前提下减少辅助化疗的使用[33]。

研究方法
II 期结肠癌患者按 2:1 比例随机分配,分别接受 ctDNA 结果指导的治疗决策或基于标准临床病理特征的治疗决策。在 ctDNA 指导管理中,术后 4 周或 7 周 ctDNA 阳性的患者接受以奥沙利铂为基础或氟嘧啶类化疗;ctDNA 阴性的患者不接受治疗。主要疗效终点为 2 年无复发生存期,关键次要终点为辅助化疗使用率。
研究结果
共 455 例患者完成随机分组,其中 302 例分配至 ctDNA 指导组,153 例分配至标准管理组,中位随访时间为 37 个月。
ctDNA 指导组的辅助化疗使用率显著低于标准管理组(15% vs. 28%;相对风险 1.82,95% 置信区间 [CI] 1.25~2.65)。
在 2 年无复发生存期评估中,ctDNA 指导管理非劣于标准管理(分别为 93.5% 和 92.4%;绝对差异 1.1 个百分点,95% CI -4.1~6.2 [非劣效性界值为 – 8.5 个百分点])。
ctDNA 阳性且接受辅助化疗的患者 3 年无复发生存率为 86.4%,ctDNA 阴性且未接受治疗的患者为 92.5%。
研究结论
ctDNA 指导的 II 期结肠癌治疗策略减少了辅助化疗的使用,且未影响无复发生存期。
CIRCULATE-Japan为一系列三个研究,分别涵盖了预后观察,升级和降级完整三个方面。
CIRCULATE-Japan Galaxy研究[35]:这是一项大规模的前瞻性研究,已在23和24年连续在Nat Med上报告结果,最新发表内容是探索基于 ctDNA 的 MRD 检测在结直肠癌肝转移(CLM)患者中的应用,研究结果为ctDNA监测用于切除术后复发和死亡风险分层提供了证据,或可用于指导结直肠癌辅助治疗。
CIRCULATE—VEGA 试验是一项随机 III 期研究,其设计目的是:在 GALAXY 研究中,对于根治性手术后 4 周 ctDNA 状态为阴性的高危 II 期或低危 III 期结肠癌患者,验证单纯术后观察是否非劣于为期 3 个月的卡培他滨联合奥沙利铂标准治疗[36]。
CIRCULATE —ALTAIR 试验是一项双盲 III 期研究,旨在证实:在 GALAXY 研究中循环肿瘤阳性的切除后结直肠癌患者中,三氟尿苷 / 替吡嘧啶的疗效优于安慰剂[36]。

研究方法
纳入 GALAXY 研究(UMIN000039205)中无肝外疾病的 CLM 患者。在调整年龄、性别、肝转移数目及大小、RAS 状态和原发性癌症既往奥沙利铂使用史后,评估 ACT 在 MRD 阳性组和阴性组中的无病生存期(DFS)获益。采用个性化的肿瘤定制 16 重聚合酶链反应 – 下一代测序(mPCR-NGS)检测 ctDNA。在根治性手术后 2-10 周、ACT 开始前评估基于 ctDNA 的 MRD 状态。
研究结果
在 GALAXY 研究注册的 6061 例患者中,纳入 190 例未接受术前化疗的手术切除 CLM 患者,中位随访时间为 24 个月(1-48 个月)。
MRD 检测窗口期内ctDNA阳性率为 32.1%(61/190)。25.1%(48/190)的患者接受了 ACT。
在 MRD 阳性组中,接受 ACT 治疗的患者 24 个月 DFS 更高 [33.3% vs 未达到,调整后风险比(HR):0.07,P<0.0001];而在 MRD 阴性组中未观察到 ACT 的获益(24 个月 DFS:72.3% vs 62.2%,调整后 HR:0.68,P=0.371)。
多变量分析显示,在 MRD 阳性组中,肝转移大小(HR:3.94,P=0.031)是 DFS 的预后因素;而在 MRD 阴性组中,无任何临床病理因素与 DFS 相关。
研究结论
本研究数据提示,ACT 可能对 MRD 阳性的 CLM 患者具有显著临床获益。基于 MRD 状态的风险分层有望纳入未来的 CLM 临床试验中。
2025 ESMO GI上,复旦大学附属肿瘤医院彭俊杰教授报告了FIND研究,尝试将ctDNA动态监测嵌入术后随访流程中,而且采用手术这一根治性更强的手段[37]。

研究方法
FIND 是一项前瞻性多中心随机 Ⅲ 期试验。符合条件的患者在术后被随机分配至 ctDNA 甲基化监测组或标准监测组。ctDNA 分析采用单管甲基化特异性定量聚合酶链反应(mqMSP)检测方法,针对 10 个甲基化标志物,可检测低至 0.01% 等位基因频率的肿瘤 DNA。
试验组将 ctDNA 监测与标准影像学检查相结合:ctDNA 检测阳性时立即启动 CT 成像检查;若影像学检查为阴性,则每两个月进行一次 CT 扫描,同时每季度进行一次 ctDNA 检测。在连续两次 ctDNA 检测结果为阴性后,影像学检查恢复为标准频率。
主要终点为:术后 2 年内接受根治性治疗的复发患者比例 。
研究结果
2023 年 7 月至 2024 年 6 月期间,728 例患者被随机分组(363 例为 ctDNA 引导组,365 例为标准组 )。截至 2025 年 2 月,中位随访时间为 12 个月 。
ctDNA 组有 74 例患者、标准组有 70 例患者出现方案偏离情况 。
意向性治疗(ITT)分析和符合方案(PP)分析显示,累积复发率无显著差异(ITT 分析:P = 0.671;PP 分析:P = 0.738 )。
然而,与标准监测相比,ctDNA 引导的监测显著提高了复发患者接受根治性治疗的比例 [50.0%(95% 置信区间 31.4–68.6%) vs. 22.6%(11.4–39.8%);相对风险 2.214(1.060–4.780);P = 0.034] 。
研究结论
FIND 试验的中期分析表明,与基于标准影像学的随访相比,ctDNA 甲基化引导的术后监测显著提高了复发的非转移性结直肠癌患者接受根治性治疗的可能性。
03
非小细胞肺癌(NSCLC)
根治性治疗后 ctDNA-MRD 阳性患者复发风险高,多时间点监测可提高复发预测敏感性(82%~100%)[20]。肿瘤知情方法(如基于 WES 的定制检测)可提高特异性 [16]。
2024年发表在JAMA Oncology上的一篇研究,评估了在晚期 NSCLC 患者中,经局部巩固治疗(LCT)达到完全缓解后,采用基于循环肿瘤 DNA(ctDNA)指导的适应性降阶酪氨酸激酶抑制剂(TKI)治疗的临床可行性[11]。


研究方法
前瞻性非随机对照试验于 2020 年 6 月 3 日至 2022 年 7 月 19 日在单中心开展,纳入 60 例存在驱动基因突变的晚期 NSCLC 患者,这些患者经 TKI 治疗联合 LCT 后无影像学可检测的病变。中位(范围)随访时间为 19.2(3.8~29.7)个月。数据分析时间为 2022 年 12 月 15 日至 2023 年 5 月 10 日。
干预措施:停用 TKI 治疗并每 3 个月随访一次。当患者出现疾病进展(依据实体瘤疗效评价标准 1.1 版定义)、ctDNA 可检测到或癌胚抗原(CEA)水平升高(以最先出现者为准)时,重启治疗;若随访监测中所有指标均为阴性,则继续暂停治疗。
研究结果
在 60 例研究参与者中(中位 [范围] 年龄 55 [21~75] 岁;女性 33 例 [55%]),中位 PFS 为 18.4 个月(95% 置信区间:12.6~24.2 个月),中位(范围)总治疗中断持续时间为 9.1(1.5~28.1)个月。
14 例患者(A 组)持续停用 TKI,中位(范围)治疗中断时间为 20.3(6.8~28.1)个月;31 例患者(B 组)因 ctDNA 可检测到和 / 或 CEA 升高接受再治疗,中位 PFS 为 20.2 个月(95% 置信区间:12.9~27.4 个月),中位(范围)总治疗中断时间为 8.8(1.5~20.6)个月;15 例患者(C 组)因疾病进展接受 TKI 再治疗,中位 PFS 为 5.5 个月(95% 置信区间:1.5~7.2 个月)。
所有参与者的 TKI 再治疗缓解率为 96%,中位至下次治疗时间为 29.3 个月(95% 置信区间:25.3~35.2 个月),总生存期数据尚未成熟。
研究结论
对于 LCT 后无病变且 ctDNA 检测阴性的 NSCLC 患者,采用这种适应性降阶 TKI 策略具有可行性。这可能为部分晚期 NSCLC 患者提供一种以 ctDNA 为指导的降阶治疗方案。
2025年3月,广东省人民医院吴一龙教授、美国耶鲁大学Roy S. Herbst共同通讯在Nature Medicine发表的研究报告了EGFR突变IB–IIIA期非小细胞肺癌切除后奥希替尼辅助治疗的MRD分析结果[38]。

研究结果
-
MRD 检测较影像学 DFS 事件中位提前 4.7 个月(95% 置信区间:2.2–5.6 个月)被检出。
-
奥希替尼组与安慰剂组 36 个月的 DFS 和 MRD 无事件率分别为 86% 和 36%(风险比:0.23,95% 置信区间:0.15–0.36)。
-
奥希替尼组中,28 例(25%)患者出现 DFS 或 MRD 事件;大多数事件发生在奥希替尼停药后(28 例中的 19 例,占 68%),且其中 11 例(19 例中的 58%)发生在停药后 12 个月内。
-
奥希替尼治疗结束后 24 个月,DFS 和 MRD 无事件率为 66%。
除此之外, 2024年的ASCO 大会上,一项关于 MRD 检测用于高危 NSCLC 患者术后评估和监测的研究显示,存在高危因素如肿瘤血栓和肺泡间隙扩散的 NSCLC 患者,即使行 R0 切除,术后 MRD 阳性率也很高[42]。

研究内容
本研究纳入接受根治性手术(R0 切除)的 NSCLC 患者,术后收集其组织样本。通过全外显子测序(WES)明确个体体细胞突变信息,据此设计个性化 MRD 检测面板用于后续检测。术后 3-4 周采集血浆样本,采用下一代测序(NGS)技术以 100,000× 测序深度分析 MRD 状态。
研究结果
本研究共纳入 124 例 NSCLC 患者,中位年龄 60 岁(范围 29-86 岁)。队列中男性 63 例(50.8%),女性 61 例(49.2%)。病理分期方面,92 例为 I 期,5 例为 II 期,17 例为 III 期,10 例为 IV 期。
共在 6,315 个基因中检出 10,260 个体细胞突变,包括 639 个插入 / 缺失(InDels)、9,613 个单核苷酸变异(SNVs)和 8 个基因融合。最常见的突变基因为 EGFR(58.87%),其次为 TTN(45.97%)、TP53(40.32%)、CEP192(20.97%)、XIRP2(19.35%)、ZFHX4(19.35%)和 TOPAZ1(16.94%)。
患者 MRD 阳性率为 29.0%(36/124),其中男性阳性率(34.9%,22/63)高于女性(22.9%,14/61)。按分期划分,I 期患者 MRD 阳性率为 16.3%(16/92),II 期为 40.0%(2/5),III 期为 47.0%(8/17),IV 期为 100%(10/10)。在存在高危因素的患者中,31.6%(12/38)的 STAS 阳性患者、60.0%(6/10)的 TT 阳性患者以及 53.8%(7/13)的胸膜侵犯患者 MRD 阳性,表明高危组术后 MRD 阳性率更高。
研究结论
具有 STAS、TT 等高危因素的 NSCLC 患者,即使在 R0 切除后,术后 MRD 阳性率仍较高。现有研究表明,术后 MRD 是复发、转移及不良预后的指标。本研究结果提示,携带这些高危因素的 NSCLC 患者更易发生复发和转移,可能需要术后辅助治疗以实现有效管理。
04
淋巴瘤
在 ALK 阳性 ALCL 中,基于 PCR 的 MDD 和 MRD 检测是独立预后参数,用于临床分层 [29];在套细胞淋巴瘤(MCL)中,MRD 作为治疗后结局预测指标的价值日益受到关注 [34]。
05
卵巢癌
2025年ASCO上一篇关于卵巢癌的摘要对卵巢癌血浆ctDNA与组织基因组变异一致性的关键影响因素及其预后价值进行分析[44]。

研究方法
采用定制的 2365 基因面板,对 29 例初治卵巢癌患者的匹配治疗前组织和血浆样本进行分析。总一致性率和个体一致性率计算为总一致突变数与总组织突变数的比值,患者被分为高一致性组(≥50%)和低一致性组(<50%)。分析影响一致性的临床病理及肿瘤分子因素,并在晚期患者中评估一致性率与临床结局(包括化疗敏感性 [KELIM 评分] 和无进展生存期 [PFS])的关系。
研究结果
-
队列主要由 FIGO III-IV 期患者(89.7%)和高级别浆液性癌患者(89.7%)组成,中位随访时间为 306 天(66-570 天)。组织 – 血浆总体一致性率为 42%,共享变异在不同样本类型中呈现一致的丰度模式(r=0.25,p=0.0074),且包含 66.1% 的组织驱动突变。组织特异性突变的变异等位基因频率低于共享突变(中位数 4.4% vs 28.7%)。单核苷酸变异的血浆检出率高于结构变异(47.3% vs 25.4%)。个体一致性率差异显著(0-83.3%)。
-
高一致性组的肿瘤 Ki-67 指数(中位数 85% vs 70%)、组织肿瘤突变负荷(TMB,中位数 5.1 vs 4.1 个突变 / 兆碱基)和血浆 ctDNA 分数(中位数 8.1% vs 0.9%)均更高。两组在最大肿瘤直径、CA125 水平、肿瘤样本来源(原发灶或转移灶)、BRCA 突变状态 / 同源重组状态方面无显著差异。多变量分析显示,更高的 TMB(OR 1.931,95% 置信区间 1.064-3.504)和血浆 ctDNA 分数(OR 1.416,95% 置信区间 1.060-1.893)与高一致性率独立相关。
-
在晚期患者中,低一致性组的 KELIM 评分更低(中位数 0.7 vs 1.2;评分≥1 的患者占比 15.4% vs 69.2%),提示化疗敏感性降低。一致性率与 KELIM 评分呈强相关性(r=0.71,p<0.0001)。低一致性组的 PFS 更短(中位数 436 天 vs 未达到,p=0.037)。
研究结论
研究发现卵巢癌治疗前肿瘤组织与血浆 ctDNA 突变谱的一致性为中度,受技术和生物学因素影响。组织 – 血浆一致性或可作为一种新型化疗敏感性和预后指标。
三
结论及展望
MRD 检测已成为癌症精准诊疗的核心工具,在预后评估、治疗指导和复发监测中发挥关键作用。随着检测技术的进步和标准化的推进,MRD 有望在更多癌症类型中实现临床普及,推动癌症治疗从 “经验性治疗” 向 “MRD 驱动的个体化治疗” 转变。未来需通过多学科协作克服技术和临床障碍,充分释放 MRD 在改善患者结局中的潜力[3]。
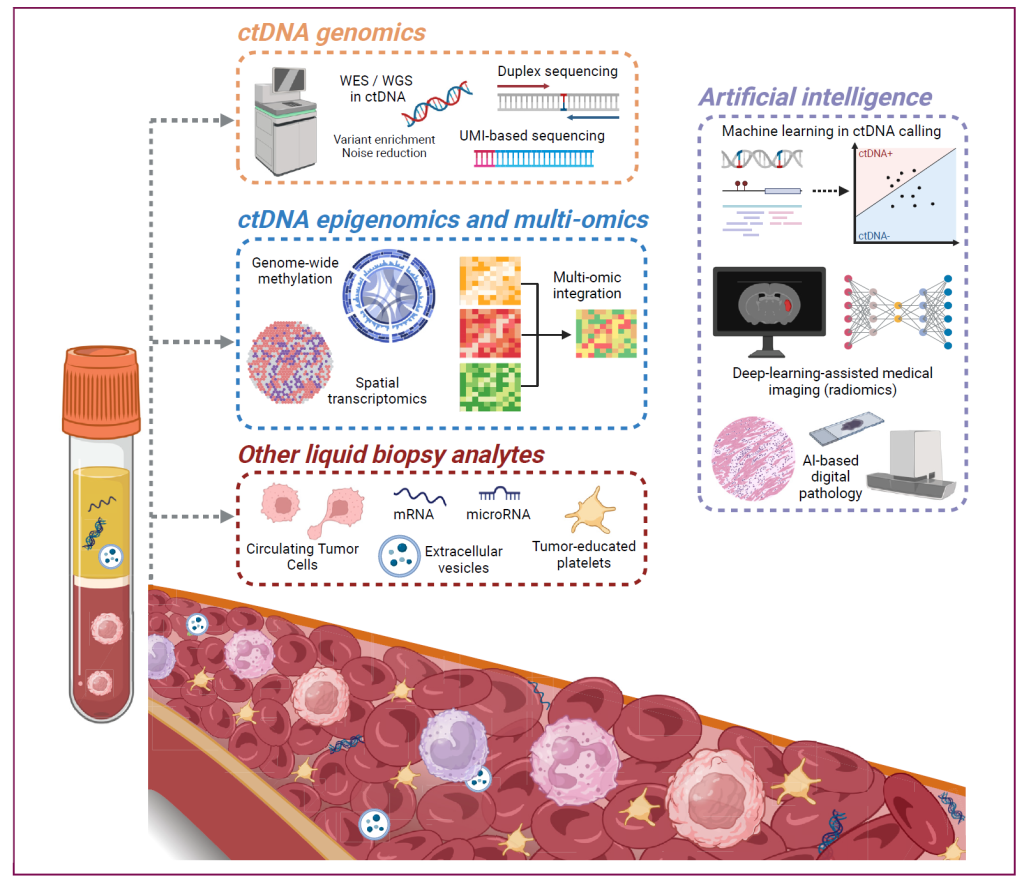
Figure 2. Summary of emerging technologies and future directions for ctDNA assessment.
四
伯科MRD个体化Panel表现
伯科生物全国产化高性能靶向捕获技术平台(TargetCap®)为MRD检测提供全面支撑,包括Tumor-Informed与Tumor-Agnostic技术策略中的不同类型MRD Gene Panel设计合成及配套试剂。在Tumor-Informed的半固定Panel检测方案中,伯科TargetCap® Core Exome Panel v3.0(WES Panel)是肿瘤组织的个体化变异发现筛选的强有力工具,在个体化变异监测环节,伯科也正为用户提供性能优异的Carrier Panel(基础模块)和极速MRD个体化Panel定制(个体变异跟踪模块),供货周期<7天。
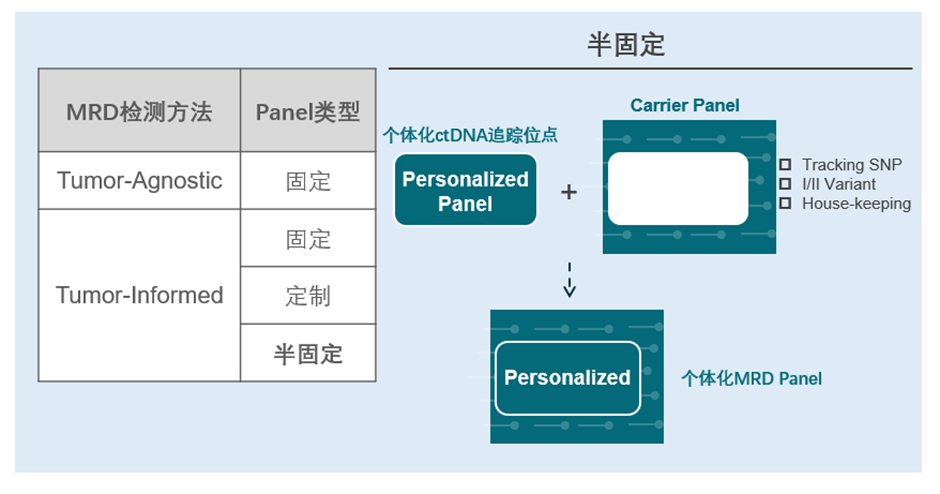
MRD检测Panel分类
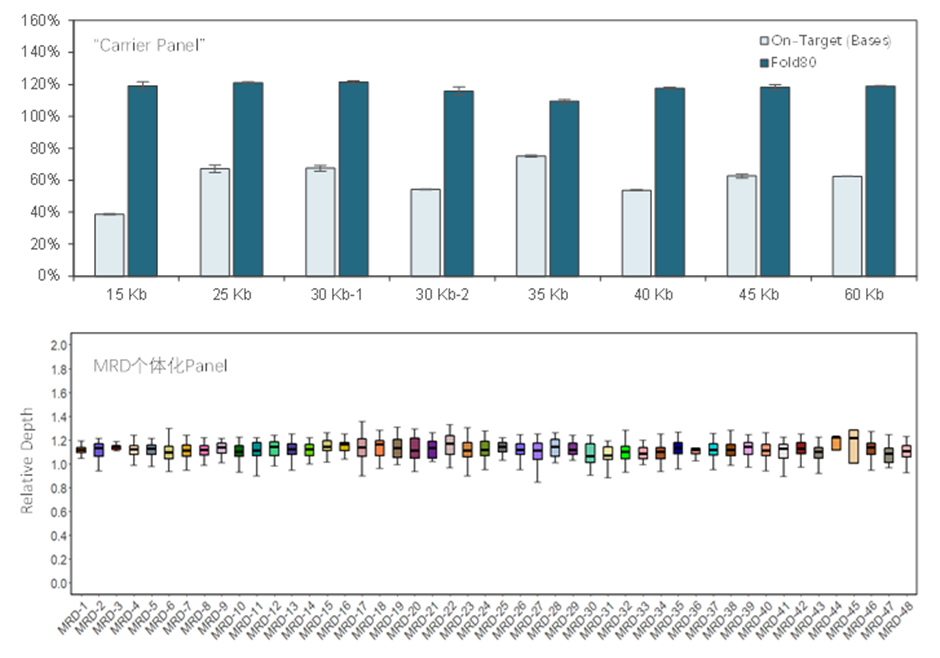
伯科 “Carrier Panel”与MRD个体化Panel表现
参考文献
[1]. Lemei Zhu, et al. Minimal residual disease (MRD) detection in solid tumors using circulating tumor DNA: a systematic review. Frontiers in Genetics 2023
[2]. Meiling Song, et al. Minimal Residual Disease Detection: Implications for Clinical Diagnosis and Cancer Patient Treatment. MedComm 2025
[3]. Martínez-Castedo B, et al. Minimal residual disease in colorectal cancer. Tumor-informed versus tumor-agnostic approaches: unraveling the optimal strategy[J]. Annals of Oncology, 2025, 36(3): 263-276.
[4]. Andreea-Iulia Ștefan, et al. The emerging role of next-generation sequencing in minimal residual disease assessment in acute lymphoblastic leukemia: a systematic review of current literature.Frontiers in Medicine 2025
[5]. Binbin Chen, et al. Advancing MRD Detection in Multiple Myeloma. American Journal of Clinical Oncology 2025
[6]. Federico Caroni, et al. Minimal Residual Disease Significance in Multiple Myeloma Patients Treated with Anti-CD38 Monoclonal Antibodies. Pharmaceuticals 2025
[7] Mohammed A. Aljama, et al. Are we maintaining minimal residual disease in myeloma? Leukemia and Lymphoma 2025
[8]. Xuefeng Li, et al. Minimal residual disease in systemic light chain amyloidosis: a systematic review and meta-analysis. Journal of Cancer Research and Clinical Oncology 2024
[9]. Mina Meseha, et al. Minimal Residual Disease-Adapted Therapy in Multiple Myeloma: Current Evidence and Opinions. Current Oncology Reports 2024
[10]. Junren Chen, et al. Measurable residual disease (MRD)-testing in haematological and solid cancers. Leukemia. 2024 Jun;38(6):1202-1212. doi: 10.1038/s41375-024-02252-4.
[11]. Song Dong, et al. Circulating Tumor DNA-Guided De-Escalation Targeted Therapy for Advanced Non-Small Cell Lung Cancer: A Nonrandomized Controlled Trial. JAMA Oncol. 2024 Jul 1;10(7):932-940.
[12]. S. Kobayashi, et al. Japan society of clinical oncology position paper on appropriate clinical use of molecular residual disease (MRD) testing. International Journal of Clinical Oncology 2025
[13]. Paiva B, et al. Opportunities and challenges for MRD assessment in the clinical management of multiple myeloma. Nat Rev Clin Oncol. 2025 Apr 7.
[14]. Aurore Perrot, et al. Measurable Residual Disease–Guided Therapy in Newly Diagnosed Myeloma. N Engl J Med 2025
[15]. Feng Y, et al. Have we been qualifying measurable residual disease correctly? Leukemia. 2023
[16]. Aristeidis E Boukouris, et al. A comprehensive overview of minimal residual disease in the management of early-stage and locally advanced non-small cell lung cancer. NPJ Precision Oncology 2025
[17].Short NJ, et al. Clinical use of measurable residual disease in adult ALL: recommendations from a panel of US experts. Blood Adv. 2025
[18]. James J. Sears, et al. Clinical Applications for Liquid Biopsy Assessment of Minimal Residual Disease in Breast Cancer. Current Breast Cancer Reports 2023
[19]. C. Charalampous, et al. Minimal Residual Disease Assessment in Multiple Myeloma Patients: Minimal Disease With Maximal Implications. Frontiers in Oncology 2022
[20]. B. Pellini, et al. Circulating Tumor DNA Minimal Residual Disease Detection of Non-Small-Cell Lung Cancer Treated With Curative Intent. Journal of Clinical Oncology 2022
[21]. Megan R Greenberg, et al. The Impact of Minimal Residual Disease Measurement in the Management of Chronic Lymphocytic Leukemia. Cancers (Basel). 2025
[22] Stelmach P, Trumpp A. Leukemic stem cells and therapy resistance in acute myeloid leukemia[J]. Haematologica, 2023.
[23] Gui G, Ravindra N, Hegde P S, et al. Measurable residual mutated IDH1 before allogeneic transplant for acute myeloid leukemia[J]. Bone Marrow Transplantation, 2025
[24]. S. Bernardi, et al. Digital PCR as a New Method for Minimal Residual Disease Monitoring and Treatment Free Remission Management in Chronic Myeloid Leukemia Patients: Is It Reliable? Hemato 2022
[25]. Paola Pacelli, et al. “Friends and foes” of multiple myeloma measurable/minimal residual disease evaluation by next generation flow. Frontiers in Oncology 2022
[26].Wang L-L, Zhao P, Liu J, et al. Peritransplant lysine methyltransferase 2a–rearranged measurable residual disease dynamics as a prognostic marker in adult acute myeloid leukemia. Cancer. 2025
[27]. Klaus Pantel, et al. Minimal residual disease as a target for liquid biopsy in patients with solid tumours. Nat Rev Clin Oncol. 2025
[28]. P. Merli, et al. Minimal Residual Disease Prior to and After Haematopoietic Stem Cell Transplantation in Children and Adolescents With Acute Lymphoblastic Leukaemia: What Level of Negativity Is Relevant? Frontiers in Pediatrics 2021
[29]. L. Mussolin, et al. Minimal Disease Monitoring in Pediatric Non-Hodgkin’s Lymphoma: Current Clinical Application and Future Challenges. Cancers 2021
[30] Garcia-Murillas I, Schiavon G, Weigelt B, et al.Mutation tracking in circulating tumor DNA predicts relapse in early breast cancer[J]. Science Translational Medicine, 2015
[31] Janni W, Rack B, Friedl T W P, et al.Detection of minimal residual disease and prediction of recurrence in breast cancer using a plasma-only circulating tumor DNA assay[J]. ESMO Open, 2025
[32]. Shaw JA, et al. Serial Postoperative Circulating Tumor DNA Assessment Has Strong Prognostic Value During Long-Term Follow-Up in Patients With Breast Cancer. JCO Precis Oncol. 2024
[33]. Jeanne Tie, et al. Circulating Tumor DNA Analysis Guiding Adjuvant Therapy in Stage II Colon Cancer. N Engl J Med. 2022
[34]. M. Ladetto, et al. Minimal residual disease (MRD) in mantle cell lymphoma: Methods and Clinical Significance. M. Ladetto, R. Tavarozzi, C. Pott
[35] Kataoka K, Mori K, Nakamura Y, et al.Survival benefit of adjuvant chemotherapy based on molecular residual disease detection in resected colorectal liver metastases: subgroup analysis from CIRCULATE-Japan GALAXY[J]. Annals of Oncology: Official Journal of the European Society for Medical Oncology, 2024
[36]. Hiroya Taniguchi , et al. CIRCULATE- Japan: Circulating tumor DNA– guided adaptive platform trials to refine adjuvant therapy for colorectal cancer. Cancer Science. 2021
[37]. 2025 EMSO GI. Dynamic Circulating Tumor DNA Methylation Monitoring Guiding Postoperative Surveillance in Non-Metastatic Colorectal Cancer: Interim Analysis of FIND Trial.
[38]. Roy S Herbst, et al. Herbst R S, John T, Grohé C, et al.Molecular residual disease analysis of adjuvant osimertinib in resected EGFR-mutated stage IB-IIIA non-small-cell lung cancer[J]. Nature Medicine, 2025
[39] ASCO 2025 3044. Impact of stereotactic ablative radiotherapy (SABR) on detection of ctDNA in patients with early-stage lung cancer: Interim findings from the prospective SABR-DETECT trial.
[40]. T. Robak, et al. Measurable residual disease in hairy cell leukemia: Technical considerations and clinical significance. 2022, Frontiers in Oncology
[41]. J. Bohn, et al. Treatment of Classic Hairy Cell Leukemia: Targeting Minimal Residual Disease beyond Cladribine. 2022, Cancers
[42]. Yu-Heng Zhou, Yaobin Lin, Bing-Yu Rao, et al. Investigation of the role of personalized molecular residual disease in the assessment of high-risk non-small cell lung cancer (NSCLC) post-operation. 2024 ASCO. Abstract 8027.
[43]. Perioperative ctDNA – Based Molecular Residual Disease Detection for Non – Small Cell Lung Cancer: A Prospective Multicenter Cohort Study (LUNGCA – 1). Clin Cancer Res.2022
[44]. Concordance of circulating tumor DNA and tissue genomic profiling in ovarian cancer: influencing factors and clinical significance. 2025 ASCO. Abstract 5548
[45]. A. Venditti, et al. Gimema AML1310 trial of risk-adapted, mrd-directed therapy for young adults with newly diagnosed Acute Myeloid Leukemia.2019,Blood


