2025 V5.0 NCCN指南 | 肛门癌的诊断与精准治疗
- boke
- 2026-01-07
- 3:05 下午
一
疾病概述
肛门癌是一种罕见的恶性肿瘤,在普通人群中,肛门肿瘤性病变少见,其中以肛门鳞状细胞癌(ASCC)为主,约占85%。数据显示,全球每年ASCC新发病例超过3.5万,且发病率以每年2%~3%速率增长,死亡率则每年上升3%左右。肛门癌与以下因素相关:HPV感染、性行为因素、免疫功能低下、血液系统恶性肿瘤、自身免疫性疾病以及不良的生活习惯(如吸烟等)。肛门癌患病风险降低策略包括针对高危人群(如HIV感染者、移植受者)进行肛门细胞学检查、HPV检测、肛门镜检查以及HPV疫苗接种。
肛门区域包括肛管和肛周区域,根据肿瘤发生的具体部位可将肛门癌分为肛管癌和肛周癌。NCCN指南基于最新证据,为肛门鳞状细胞癌(该病最常见的组织学类型)的预防、诊断、治疗及随访提供了系统且分层的管理策略,强调个体化治疗和多学科合作。
二
肛管癌诊疗路径
1
检查与评估
活检:确诊为鳞状细胞癌
肛门指诊(DRE);腹股沟淋巴结评估:如有可疑淋巴结,考虑活检或细针穿刺(FNA);影像学检查:胸部/腹部/盆腔CT或MRI;可考虑FDG-PET/CT或FDG-PET/MRI;肛门镜检查(Anoscopy);HIV检测(如HIV状态未知);妇科检查(如宫颈癌筛查);生育风险咨询。
2
临床分期
NCCN指南使用美国癌症联合委员会(AJCC)肛门癌TNM分期。
(1)T、N、M定义
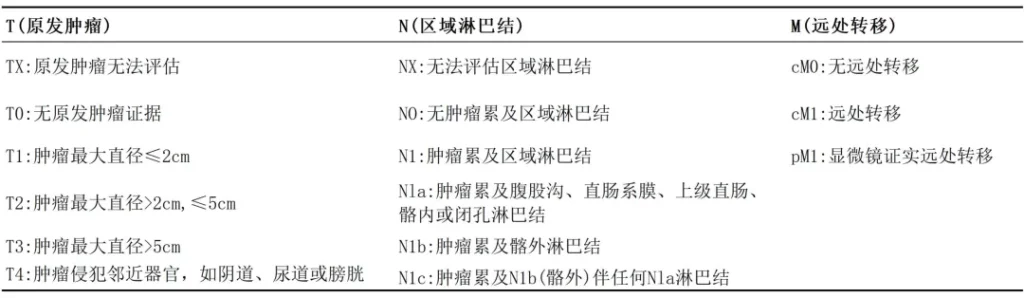
图1 T、N、M的定义
(2)AJCC解剖学分期/预后分组
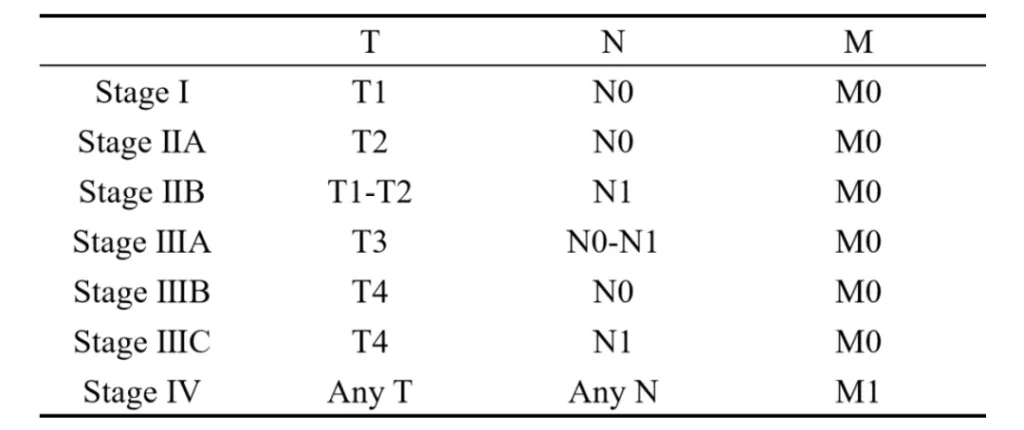
3
治疗方案
局部疾病治疗(±主动脉旁淋巴结阳性)
初始治疗:5-FU/丝裂霉素+放疗(RT)、卡培他滨/丝裂霉素+RT、5-FU/顺铂+RT。治疗完成之后,进入随访和监测。
转移性疾病治疗
首先进行一线全身治疗,治疗完成后重新评估并考虑对原发部位进行化疗/RT,使用5-FU或卡培他滨进行局部控制,最后进入二线和后续全身治疗。

图3 肛管癌诊疗路径
三
肛周癌诊疗路径
1
检查与评估
活检:确诊为鳞状细胞癌
肛门指诊(DRE);腹股沟淋巴结评估:如有可疑淋巴结,考虑活检或细针穿刺(FNA);影像学检查:胸部/腹部/盆腔CT或磁共振检查(MRI);可考虑FDG-PET/CT或FDG-PET/MRI;肛门镜检查(Anoscopy);HIV检测(如HIV状态未知);妇科检查(如宫颈癌筛查);生育风险咨询。
2
临床分期
NCCN指南对肛管癌和肛周癌均采用AJCC肛门癌分期系统,具体分期详见上述肛管癌临床分期(图1、图2)。
3
治疗方案
- T1,N0分化良好或中度分化或选择T2,N0(不涉及括约肌)
进行局部切除,若切缘充足,进入随访与监测阶段;若切缘不足,需再次切除(首选)或考虑放化疗(局部RT±5-FU/丝裂霉素或卡培他滨/丝裂霉素或5-FU/顺铂),后进入随访与监测阶段。
注:切缘充足:指手术切除的组织边缘距离肿瘤或病变组织足够远,经病理检查确认切缘处未发现肿瘤细胞或其他异常病变。这意味着手术成功切除了所有可见的病变组织,达到了根治性切除的标准,降低了肿瘤复发的风险。
切缘不足:指手术切除的组织边缘距离肿瘤或病变组织过近,或切缘处发现了肿瘤细胞、高级别上皮内瘤变等异常病变。这种情况表明手术未能完全切除病变组织,残留的肿瘤细胞可能增加术后复发的风险。
- T1,N0低分化或T2-T4,N0或任何T,N(±阳性主动脉旁淋巴结)
进行放化疗(5-FU/丝裂霉素+RT或卡培他滨/丝裂霉素+RT或5-FU/顺铂+RT),后进入随访与监测阶段。
- 转移性疾病
首先进行一线全身治疗,进行疗效评估,并考虑对原发部位进行化疗RT,使用5-FU或卡培他滨进行局部控制,随后进行二线和后续全身治疗。
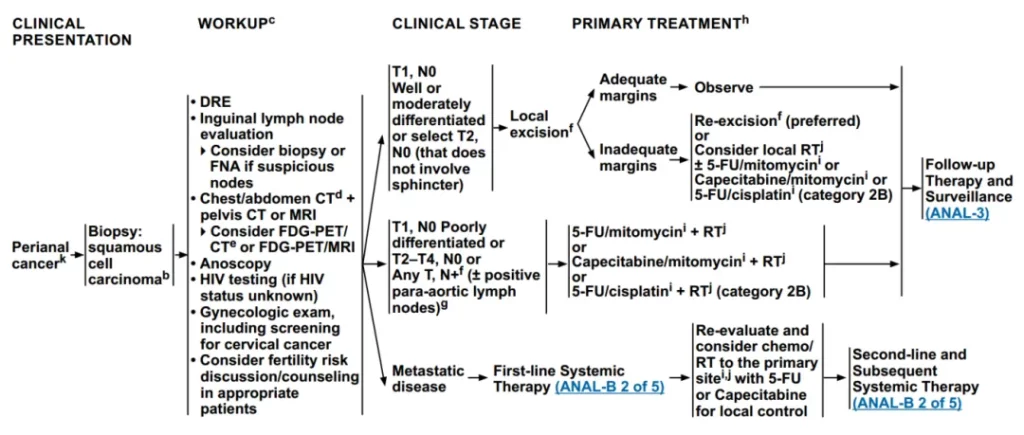
图4 肛周癌诊疗路径
4
随访和监测
首先在治疗后8-12周内通过检查+肛门指诊(DRE)进行评估。
评估结果若完全缓解,进行监测
DRE每3-6个月一次,持续5年;腹股沟淋巴结触诊每3-6个月一次,持续5年;肛门镜检查每6-12个月,持续3年;胸部/腹部/骨盆CT(有造影剂)或胸部CT(无造影剂)和腹部/骨盆MRI(有造影剂),每年一次,持续3年(II-III期)。
a.监测后续若出现局部复发,进行腹会阴切除术(APR),后续进行监测:腹股沟淋巴结触诊,每3-6个月一次,持续5年;胸部/腹部/骨盆CT(有造影剂)或胸部CT(无造影剂)和腹部/骨盆MRI(有造影剂),每年一次,持续3年。
b.若出现腹股沟淋巴结复发,进行腹股沟解剖;如果先前未接受腹股沟±5-FU/丝裂霉素或丝裂霉素/卡培他滨的RT,则考虑RT;如果先前接受RT,则卡铂/紫杉醇或5-FU/顺铂(类别2B);后续进行监测:DRE,每3-6个月一次,持续5年;腹股沟淋巴结触诊,每3-6个月一次,持续5年;肛门镜检查,每6-12个月一次,持续3年;胸部/腹部/骨盆CT(有造影剂)或胸部CT(无造影剂)和腹部/骨盆MRI(有造影剂),每年一次,持续3年。
c.后续若出现转移性疾病,首先进行一线全身治疗,随后进行二线和后续全身治疗。
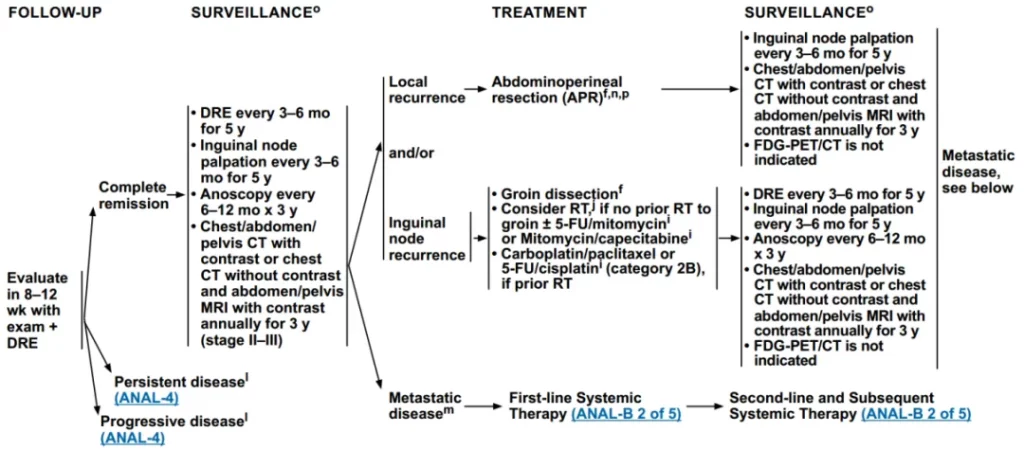
图5 随访治疗和监测—完全缓解
评估结果若为进行性疾病,活检证实,后重新进行分期
局部复发,如果是腹股沟淋巴结阳性,进行APR+腹股沟解剖;后进入监测阶段:腹股沟淋巴结触诊,每3-6个月一次,持续5年;胸部/腹部/骨盆CT(有造影剂)或胸部CT(无造影剂)和腹部/骨盆MRI(有造影剂),每年一次,持续3年;FDG-PET/CT不适用。
评估结果若为持续性疾病,4周内重新评估
在系列检查中出现进展,则按照上述进行性疾病治疗方案进行;若在系列检查中出现退化或无进展,继续观察并每隔3个月重新评价,出现进展或仍持续存在,按照上述进行性疾病治疗方案进行,若完全缓解,则进入监测阶段。
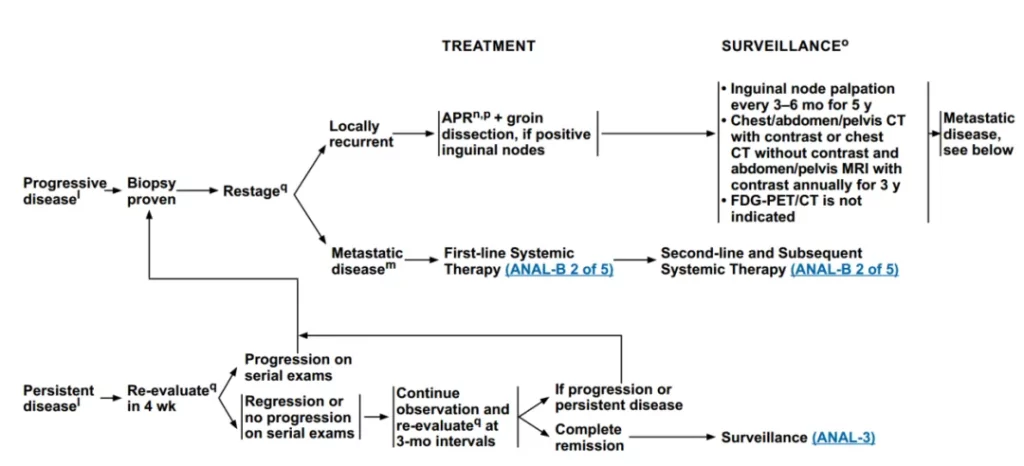
图6 随访治疗和监测—进行性/持续性
四
具体治疗方案
1
一线治疗方案

图7 一线治疗具体治疗方案
2
二线和后续治疗

图8 二线和后续治疗具体方案
基因组的变异检测在各种肿瘤类型中越来越多的用于诊断和治疗指导,基因靶向技术结合高通量测序在肛门鳞状细胞癌(ASCC)中,检测到多种变异,其中PIK3CA基因的激活突变和扩增是ASCC中最常见的遗传变异[2]。通过全外显子测序研究ASCC基因组特征,明确了ASCC中的HPV基因型、整合位点及反复出现的拷贝数变异(CNV),为疾病机制研究和临床干预提供了重要依据[3]。同时基因靶向技术结合高通量测序技术还用于免疫治疗预测标志物(TMB、MSI、PD-L1),辅助判断免疫治疗疗效[2,4]。
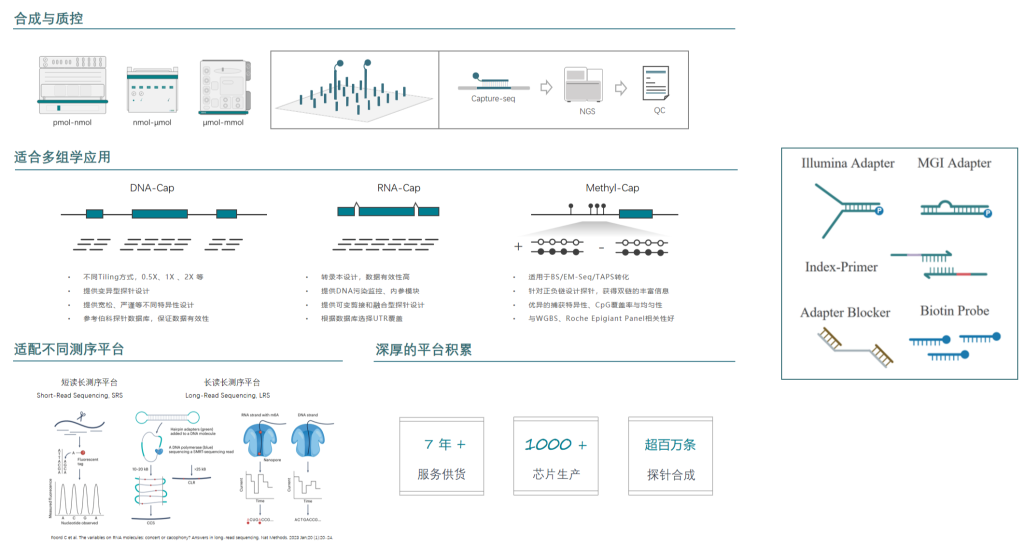
伯科生物在国内已经建设了全流程国产化的高通量核酸合成与应用技术转化中心,建立了GMP厂房和ISO9001、ISO13485质量体系。已经为国内外数百家知名医院、科学研究机构、临床检验所开发了上千款Gene Panel(液相基因芯片),并配套完整的检测试剂,各项性能参数均与国际竞品相当或优于(详见附表1),在基因组、转录组、甲基化组及病原体的检测应用方向均有成熟的产品管线。
附表1: 产品简介
血液肿瘤液相基因芯片
TargetCap® Haematological Disease Research Panel是一款用于血液肿瘤研究分析的基础型panel,覆盖407个血液病相关基因,探针覆盖约2Mb区间。探针浓度已知,可独立或进一步掺入其他探针使用。
性能表现
竞品评测
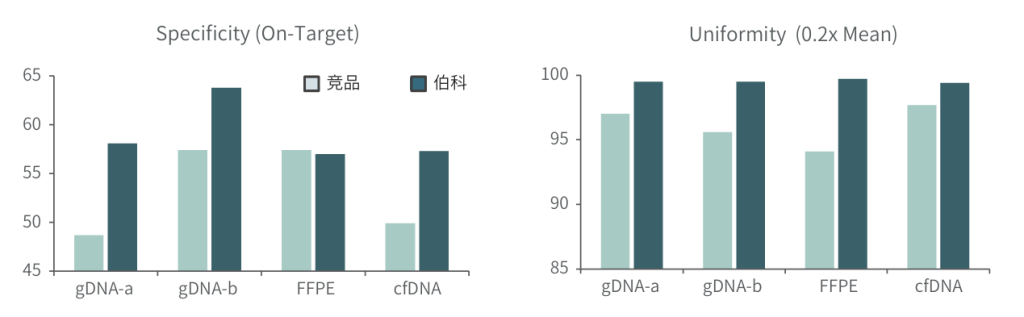
采用gDNA/cfDNA/FFPE/泛肿瘤800gDNA标准品文库,分别使用伯科商品化肿瘤大Panel-OncoGene Plus Research Panel与竞品肿瘤大Panel进行性能比较(二者大小相近),在捕获特异性上(On-Target)和覆盖均一性(0.2XMean)上,伯科均优于竞品。
对于gDNA标准品,竞品测序35.9Gb,伯科测序19.6Gb,虽然伯科测序数据少,深度低,但二者的突变频率检出无明显差异,伯科对EGFR的19号外显子缺失变异的检出优于竞品。
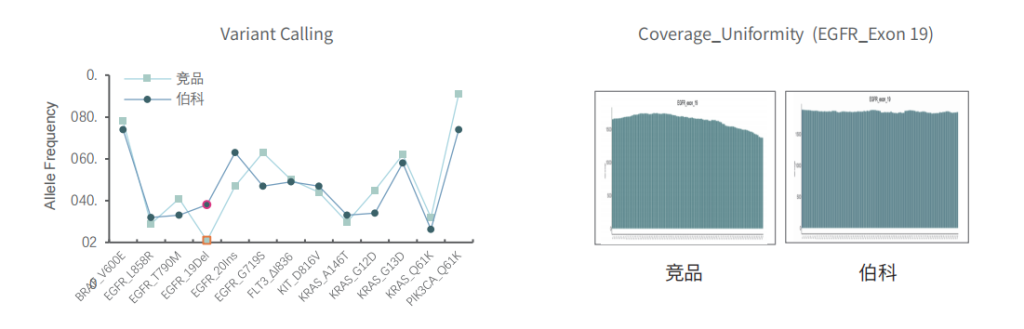
不同样本类型表现
对不同质量的gDNA样本 (WBC/FFPE, >150例),TargetCap® OncoGene Plus Research Panel表现稳定。
伯科HPV病毒捕获Panel
伯科生物设计合成的病原Panel延续了人类基因组Panel的性能优势,其富集效率高、均一性好。用户的测评结果显示,使用不同的捕获方式,对不同HPV亚型的阳性样本进行捕获测序,与mNGS相比,伯科HPVPanel的富集效率在4000倍/20000倍左右,HPV基因组覆盖均一性优异,同时,HPV亚型检测一致性好。
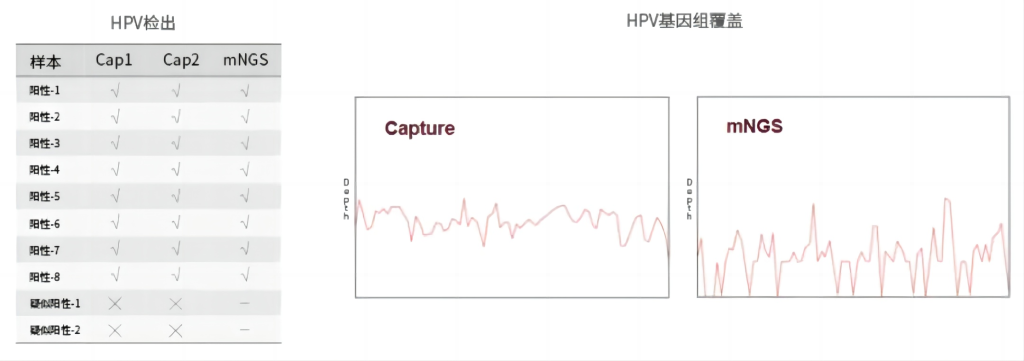
杂交与清洗试剂盒v2 简介
产品概述
伯科杂交与清洗试剂盒v2 (TargetCap® Hybridization and Wash Kit v2)简化了试剂组分和操作流程,同时仍保持优异的捕获性能。该试剂盒由4种缓冲液组成,分别为Hyb Buffer、Bingding Buffer、Wash Buffer 1和Wash Buffer 2,所有试剂均为1x缓冲液,可以直接使用,同时清洗步骤仅需3步,整个操作流程更加便捷。

基本捕获性能
使用NA12878和NA24694 DNA标准品,分别采用不同大小的Gene Panel对TargetCap® Hybridization and Wash Kit v1和v2进行比较。结果显示,在不同大小的 Gene Panel 中, v2试剂盒的中靶率和均一性与v1试剂盒表现基本一致,v2试剂盒表现略好。
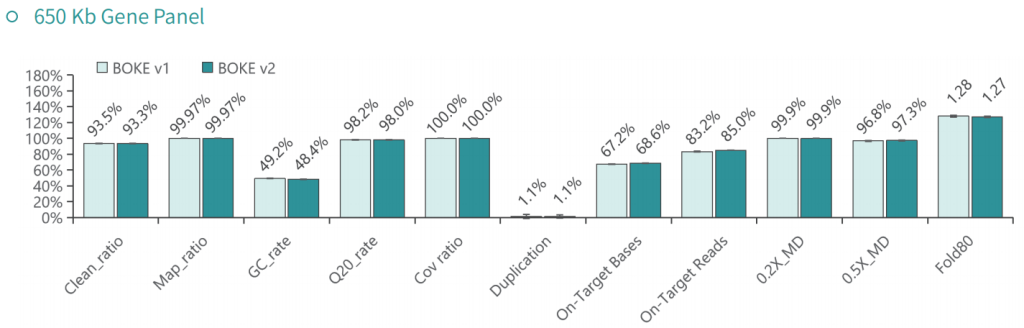
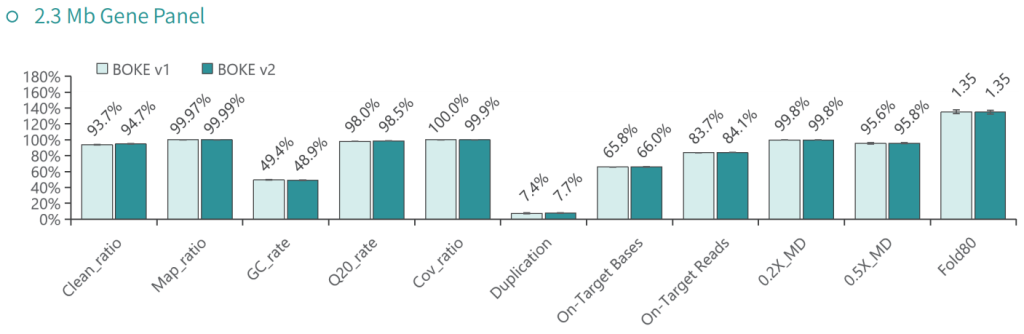
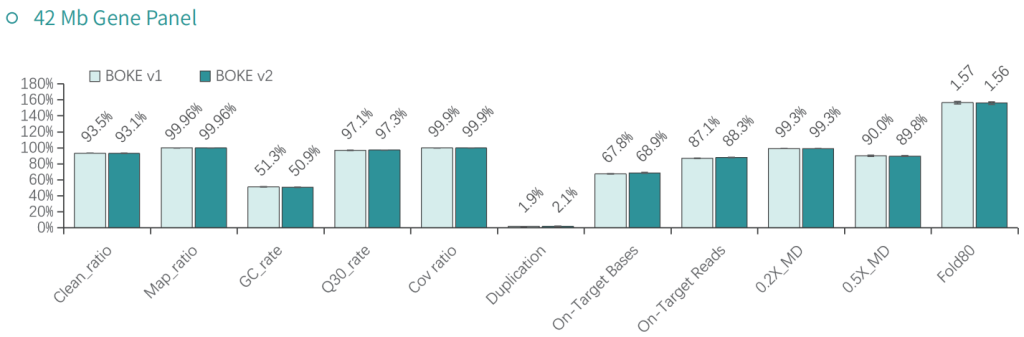
低频变异检测
使用肿瘤 SNV gDNA 标准品Ⅱ (GW-OGTM006) 对TargetCap® Hybridization and Wash Kit v1和 v2 进行验证。GW-OGTM006 DNA标准品包含 EGFR、KRAS、NRAS、BRAF、PIK3CA、FGFR3、Her2、MET 等多个常见伴随诊断基因及位点,包含点突变、插入和缺失等多种变异类型。
a. 基本QC
采用300Kb Gene Panel对该标准品进行捕获,捕获数据显示,v1与v2试剂盒的基本捕获性能表现相当,v2略优于v1。
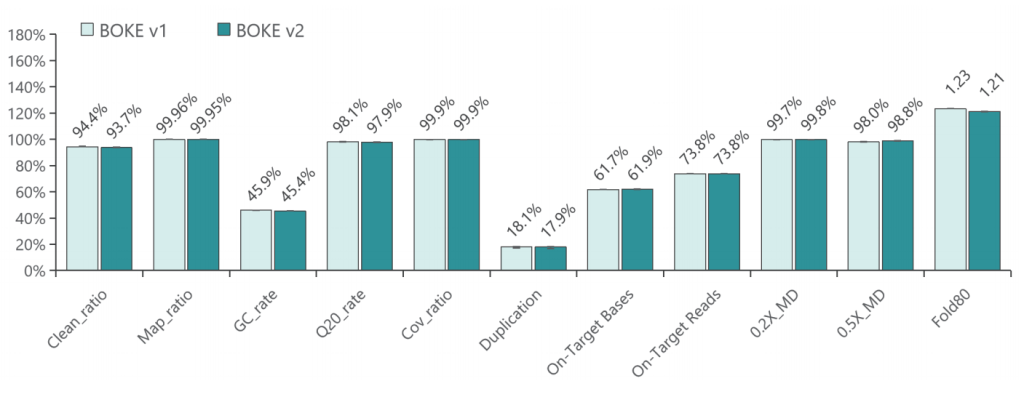
b. 变异检测
v1与v2试剂盒均能对12个已知变异准确检出。
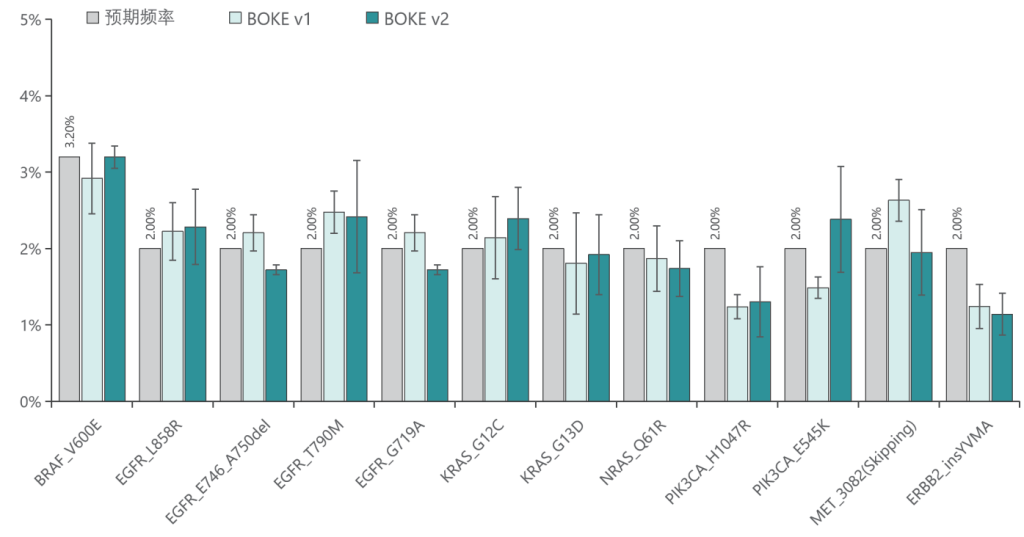
参考文献:
NCCN Clinical Practice Guidelines in Oncology-Anal Carcinoma(2025 Version 5). Rödel F, Fleischmann M, et al. Emerging advances and future opportunities in the molecular and therapeutic landscape of anal cancer. Nat Rev Clin Oncol. 2025 Jul;22(7):483-498. doi: 10.1038/s41571-025-01025-x. Aldersley J, Lorenz DR, et al. Genomic Landscape of Primary and Recurrent Anal Squamous Cell Carcinomas in Relation to HPV Integration, Copy-Number Variation, and DNA Damage Response Genes. Mol Cancer Res. 2021 Aug;19(8):1308-1321. doi: 10.1158/1541-7786.MCR-20-0884. Sharma G, Baca Y, et al. Uncovering PD-L1 among immune cell predictive biomarkers and actionable genetic alterations in anal squamous-cell carcinomas in the era of immunotherapy. ESMO Open. 2025 Jun;10(6):105315. doi: 10.1016/j.esmoop.2025.105315.


