2025 V1.0 NCCN指南 | 甲状腺癌的诊断与精准治疗
- boke
- 2026-02-27
- 3:34 下午
提到甲状腺癌,很多人会联想到“懒癌”——认为它进展慢、预后好,无需过度重视。但事实上,甲状腺癌并非单一疾病,不同病理类型、不同分期的患者,治疗方案和预后差异巨大。近年来甲状腺癌的发病率在许多国家和地区中都有所上升。甲状腺癌的发病率呈现出两个明显特点:
1)女性发病率明显高于男性;
2)发病人群的年轻化[1]。
甲状腺癌致病因素包括:
1.电离辐射:电离辐射是目前引起甲状腺癌最明确的危险因素。
2.碘摄入:目前关于碘与甲状腺癌发病的关系存在比较大的争议。
3.遗传因素:
基因突变:部分甲状腺癌与特定基因突变相关,如BRAF 基因突变在甲状腺乳头状癌中较为常见。
家族遗传:约5%的甲状腺癌患者有家族史,家族性甲状腺癌可能与遗传基因缺陷有关。(可见下文)
4.生活方式:不良生活习惯影响甲状腺细胞代谢,增加甲状腺癌发病风险。
一、甲状腺癌的诊断与分型
1
甲状腺癌的诊断
超声是评估甲状腺结节的基石。超声引导下细针穿刺活检(FNA)仍是评估可疑结节的首选方法。目前,临床广泛采用的美国放射学会甲状腺影像报告和数据系统(ACR TI-RADS)和美国甲状腺协会(ATA)指南,通过结节的成分、回声、形态、边界和钙化等特征,对结节进行风险分层。
然而,约20%-30%的结节细胞学结果属于“意义不明确的非典型病变”或“滤泡性肿瘤”。这部分结节的恶性风险难以仅凭形态学判断,基因检测便登上了舞台。基因检测(如BRAF V600 E、RET、RAS、PAX 8/PPAR γ)有助于评估不确定的FNA样本,以甲状腺癌的诊断。BRAF V600E突变发生在约45%的乳头状癌患者中,是最常见的突变。部分研究表明,BRAF V600E突变,尤其是当同时存在TERT启动子突变时,与不良预后相关。基因检测除用作诊断用途外,还有助于为晚期疾病制定靶向治疗方案。
2
甲状腺癌的组织学分型
甲状腺癌的主要组织学类型包括:
1)分化型(含乳头状癌、滤泡状癌、嗜酸细胞癌)
2)髓样癌
3)未分化癌(一种侵袭性极强的未分化肿瘤)
甲状腺癌的总体死亡率极低。分化型甲状腺癌预后通常良好,10年生存率超过90%-95%。相反,甲状腺未分化癌(ATC)几乎均为致命性疾病。
二、甲状腺癌的治疗路径
乳头状甲状腺癌(PTC)
甲状腺乳头状癌(PTC)是甲状腺癌中最常见的类型,占所有甲状腺癌的70%-80%。
1
诊断
甲状PTC的诊断通常需要综合临床症状、影像学检查、实验室检查和病理检查等多方面信息。
诊断流程:
影像学检查:进行甲状腺及颈部超声(包括中央区和侧方区)。若超声发现可疑淋巴结或存在声带麻痹,考虑行增强CT或MRI。
功能评估:考虑评估声带活动度(通过超声、喉镜等)。
病理确认:对侧颈可疑淋巴结进行FNA确认。
遗传风险:筛查个人及家族史,评估是否存在遗传性癌症风险。
2
治疗方案
(1)手术治疗
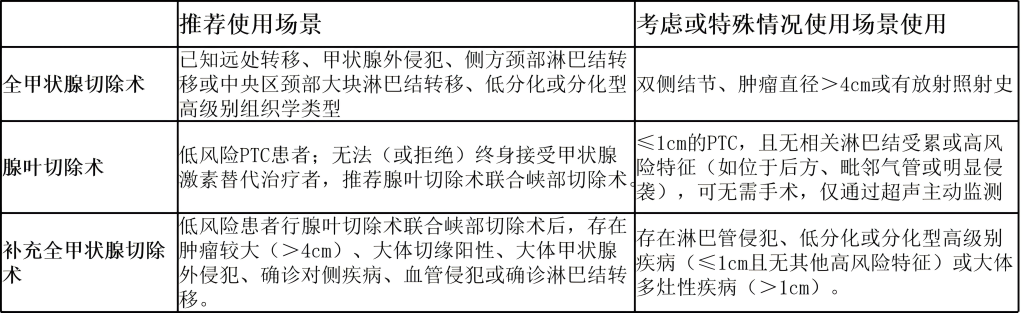
(2)放射性碘治疗(RAI)
1) 当多项临床因素预测复发、远处转移或疾病特异性死亡风险显著时,推荐术后进行RAI治疗。
不同场景下RAI的使用:
低复发/疾病特异性死亡风险患者通常不推荐术后RAI治疗;
无大体残留疾病的中风险或高风险患者可考虑RAI辅助治疗;
术后残留疾病或无法手术的远处转移患者,根据持续肿瘤是否摄取碘-131,常使用RAI治疗。然而,部分患者的转移灶可能对RAI治疗不敏感,即放射性碘难治性疾病。即使甲状腺床无摄取,也可考虑术后RAI治疗。
2) 对于放射性碘难治性患者,重建RAI摄取的再分化治疗是一种正在研究的治疗方案。
3) 对于颈部无法手术切除的大体残留疾病,若疾病威胁重要结构、存在内脏侵犯或进展迅速,可考虑EBRT;接受初始EBRT且无RAI摄取的无法手术切除大体残留疾病患者,应进行监测或考虑全身治疗。
(3)监测与维持治疗
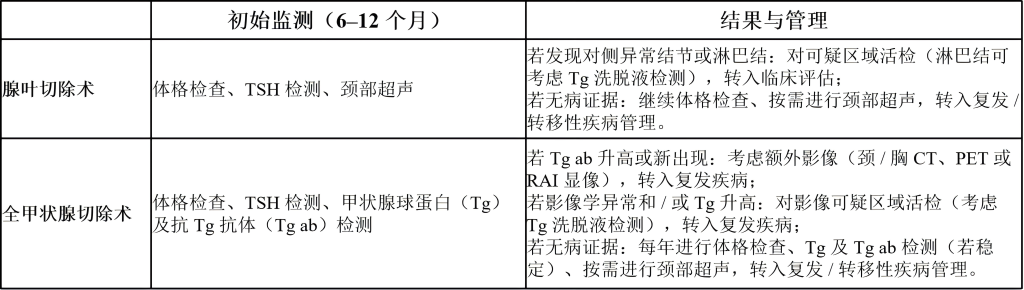
(4)复发或转移性疾病治疗
复发性疾病治疗方案:
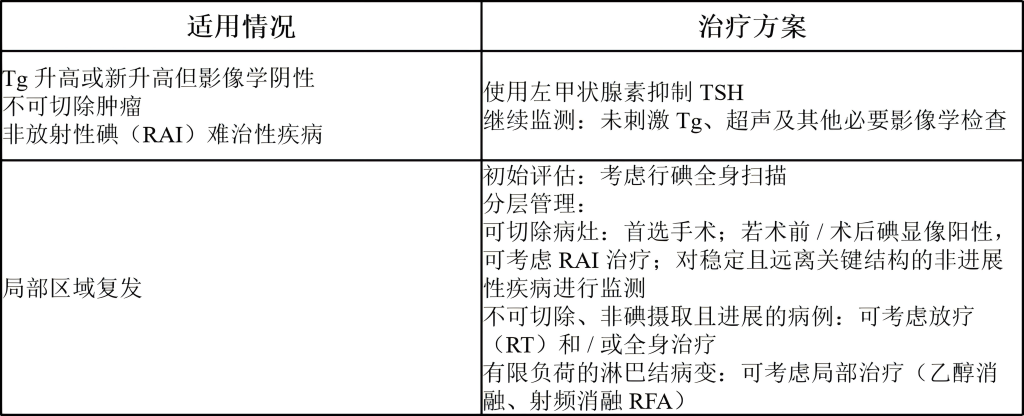
转移性疾病治疗方案:
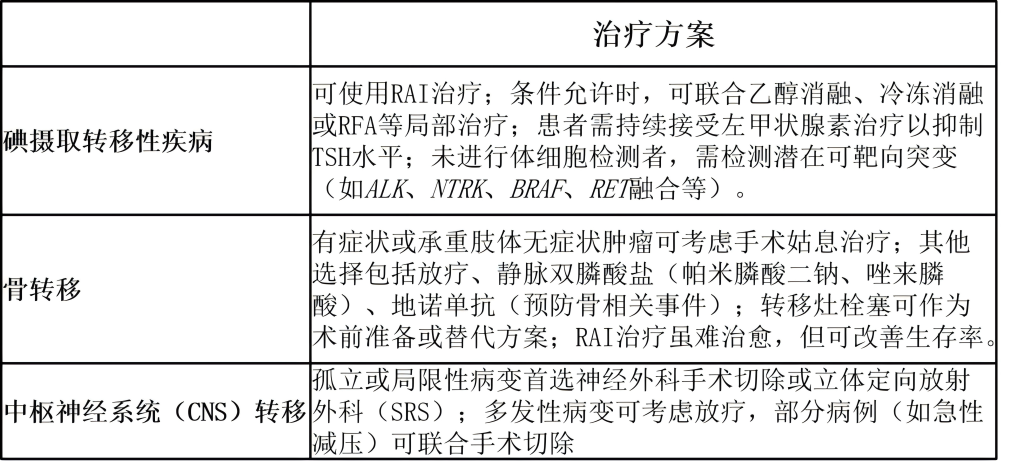
全身治疗方案:

滤泡状甲状腺癌(FTC)
乳头状甲状腺癌和滤泡状甲状腺癌的诊断和治疗相似。
1
诊断
确诊核心证据:需具备结节包膜侵犯或血管侵犯的病理证据,这是FTC确诊的关键。
细针穿刺(FNA)特点:FNA对FTC不具有特异性,这是其与PTC诊疗的主要差异。FNA诊断为“可疑滤泡性肿瘤”的病例中,80%为良性滤泡性腺瘤,仅20%最终确诊为FTC。
转移特点:通常不扩散至颈部淋巴结,若出现颈部淋巴结转移,需警惕PTC滤泡型变异型或混合性肿瘤的误诊可能;可扩散至颈部软组织。
辅助诊断:分子诊断检测可根据基因特征,辅助判断滤泡性病变或意义不明确病变(如滤泡性肿瘤、意义不明确的非典型病变)的恶性可能性。
2
治疗方案
(1)手术治疗
全甲状腺切除术:①手术时存在甲状腺外侵犯的影像学证据或术中发现;②患者选择全甲状腺切除术,以避免病理检查发现高风险癌症时需二次手术(补充甲状腺切除术)。
腺叶切除术联合峡部切除术:FNA诊断结果为滤泡性肿瘤患者的初始手术首选。
补充甲状腺切除术:叶切除术联合峡部切除术后,若最终病理证实为侵袭性FTC(广泛侵袭性或包膜血管侵袭性,且侵犯≥4个血管),推荐及时进行补充甲状腺切除术。
(2)放射性碘(RAI)治疗
术后RAI使用需结合临床病理因素决策,具体原则如下:
低复发/疾病特异性死亡风险患者:通常不推荐术后RAI治疗。
中、高复发风险患者:可考虑RAI辅助治疗,以降低复发风险。
已知或可疑远处转移患者:可使用RAI治疗。
嗜酸细胞性甲状腺癌(OTC)
嗜酸细胞癌的特征是RAS/RAF/MAPK和PI3K/AKT/mTOR通路以及EIF1AX、TERT 和DAXX基因的体细胞突变。与其他类型分化型甲状腺癌相比,嗜酸细胞性甲状腺癌通常发现时分期更晚,且预后更差。
FNA无法诊断嗜酸细胞性甲状腺癌。细胞学结果为嗜酸细胞性肿瘤时,鉴别诊断包括嗜酸细胞性甲状腺癌以及多种常见良性疾病,应考虑对嗜酸细胞性癌进行分子诊断检测。
嗜酸细胞性癌的手术管理与滤泡状甲状腺癌几乎相同,但有以下两点例外:
1)局部区域淋巴结转移更常见,因此对于临床明显且活检证实的疾病,需对受累区域进行治疗性淋巴结清扫;
2)与其他分化型甲状腺癌相比,嗜酸细胞性癌摄取碘-131的可能性更低。
髓样甲状腺癌(MTC)
髓样甲状腺癌(MTC)起源于甲状腺的神经内分泌滤泡旁C细胞。散发性MTC约占所有髓样甲状腺癌病例的80%。其余病例为遗传性肿瘤综合征。
1
诊断
MTC患者可通过FNA或基因检测进行确诊。
诊断流程:基础血清降钙素、癌胚抗原(CEA)检测、嗜铬细胞瘤筛查、血清钙检测、胚系RET 致病性突变筛查及遗传咨询、甲状腺及颈部超声(含中央区和侧颈淋巴结分区)、声带活动度评估(喉镜或超声)、进行胸部/颈部增强CT(降钙素>300 pg/mL)、肝脏MRI/三期CT、可选PET/CT/骨扫描/全身MRI排查转移性疾病。
2
治疗方案
手术是MTC主要治疗方式,碘-131对其无治疗作用;术后均需左甲状腺素治疗,维持TSH在正常范围(C细胞无TSH受体,无需TSH抑制)。术前需评估甲状旁腺功能亢进和嗜铬细胞瘤,所有患者需进行RET胚系变异检测。
(1)手术治疗
常规手术:
肿瘤≥1cm或双侧甲状腺疾病者,需进行全甲状腺切除术+双侧中央区(VI区)颈部清扫;肿瘤<1cm且单侧疾病者,推荐全甲状腺切除术,可考虑颈部清扫。
遗传性MTC的预防性手术:
MEN2A患者:诊断足够早时推荐预防性全甲状腺切除术(携带RET高风险致病性变异);携带低风险RET变异且无结构性疾病证据者,可每年监测降钙素和超声,延迟手术。
MEN2B患者:携带密码子883、918等RET致病性变异者,推荐出生后第一年或诊断时进行全甲状腺切除术(MTC风险极高)。
(2)术后监测
血清降钙素和CEA是术后残留疾病评估的核心:降钙素可检测或CEA升高者,推荐颈部超声;降钙素不可检测且CEA正常者,每年监测血清标志物即可。
降钙素≥150pg/mL者,需进行颈部、胸部、肝脏CT/MRI;部分患者可考虑骨扫描和全身MRI。无症状、标志物异常但影像学阴性者,每6-12个月监测标志物,根据倍增时间调整成像频。
MEN患者需每年筛查嗜铬细胞瘤(MEN2A/B)和甲状旁腺功能亢进(MEN2A)。
(3)复发或持续性疾病治疗
对于无法手术切除的复发或持续性MTC,部分患者可考虑激酶抑制剂治疗。
局部治疗:
无远处转移的局部区域复发者,推荐手术切除;无法手术切除且有症状/进展者,可考虑EBRT或全身治疗。有症状远处转移灶(如骨转移),可采用姑息性切除、消融、EBRT、静脉双膦酸盐/地诺单抗或全身治疗;无症状进展性远处转移灶,可监测或局部+全身治疗。
髓样癌全身治疗方案:
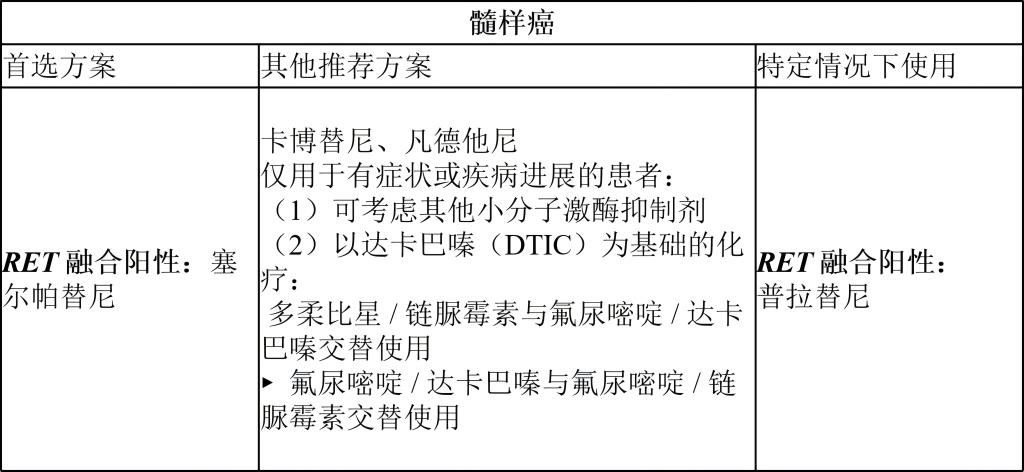
甲状腺未分化癌ATC
未分化甲状腺癌(ATC)是侵袭性极强的未分化肿瘤,疾病特异性死亡率接近100%,为最罕见的甲状腺癌类型(占所有甲状腺癌的0.8%)。约50%患者既往或同时患有分化型甲状腺癌,由分化程度更高的肿瘤经去分化发展而来(与p53肿瘤抑制蛋白缺失相关),但去分化机制尚未明确。
核心特征:与分化型甲状腺癌不同,ATC通常不具备碘摄取、TSH受体表达及Tg产生能力,因此碘-131成像和治疗不适用。
1
诊断
细针穿刺(FNA)检查难以与其他甲状腺恶性肿瘤或转移癌区分,怀疑ATC时诊断首选核心活检或手术活检。
诊断流程:
实验室检查:全血细胞计数(CBC)及分类计数、全面代谢组学检查、TSH水平检测;
内镜检查:喉镜直接检查,评估声带活动度;
影像学检查:颈部超声快速评估肿瘤范围及侵犯情况;头颈部、胸部、腹部和骨盆CT扫描明确肿瘤范围及对周围结构的侵犯;推荐PET/CT或MRI扫描用于准确分期;
分期与分子检测:所有ATC均视为IV期(A、B或C期);推荐进行可靶向突变检测(BRAF、NTRK、ALK、RET、微卫星不稳定性、DNA错配修复缺陷和肿瘤突变负荷),优先进行BRAF免疫组织化学(IHC)检测。
2
治疗方案
(1)手术治疗
仅少数肿瘤体积小、完全局限于甲状腺内或可轻松切除的患者,可行全甲状腺切除术联合治疗性淋巴结清扫术以延长患者生存期(进行全甲状腺切除术者需终身服用左甲状腺素)。
仅在有明确指征时,可ⅣC期患者行气管切开术。
(2)放射治疗
单发脑转移灶:神经外科手术切除或放疗;
肿瘤未切除/切除不彻底者,尽快启动放疗(通常联合同步化疗);
R0或R1切除):术后进行辅助外照射放疗(EBRT)+放射增敏化疗(在临床合适时);推荐采用调强放疗(IMRT)技术;吞咽困难患者可考虑肠内营养支持。

(3)全身治疗
靶向治疗为首选方案,具体根据分子检测结果选择,化疗及免疫治疗作为补充。

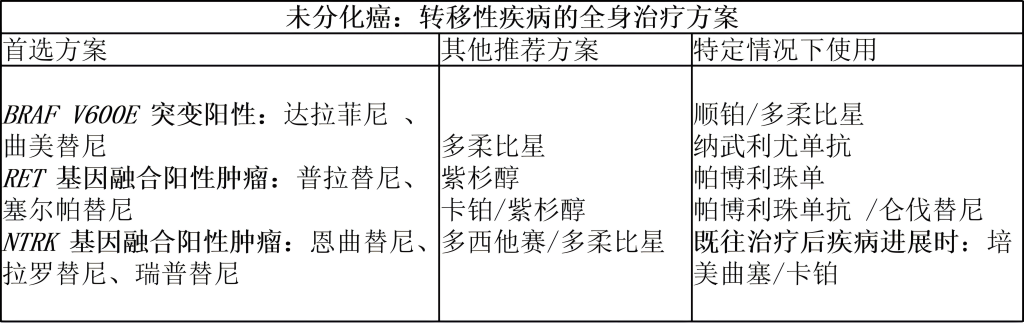
三、遗传性甲状腺癌
家族遗传性甲状腺癌包括遗传性甲状腺髓样癌(HMTC)和家族性甲状腺非髓样癌(FNMTC)。

基因检测包括胚系和体细胞变异检测,对于家族遗传性甲状腺癌主要进行胚系突变的检测,临床推荐对外周血进行检测。HMTC患者或高危人群主要检测RET基因胚系变异,临床常用的检测方法包括PCR、Sanger测序和NGS。不同的FNMTC家系基因变异位点可能不同,推荐FNMTC患者或高危人群采用NGS进行较为广泛的基因胚系突变筛查,先证者直系家属可采用Sanger测序进行验证[3]。
四、常用的靶向药物及适应证
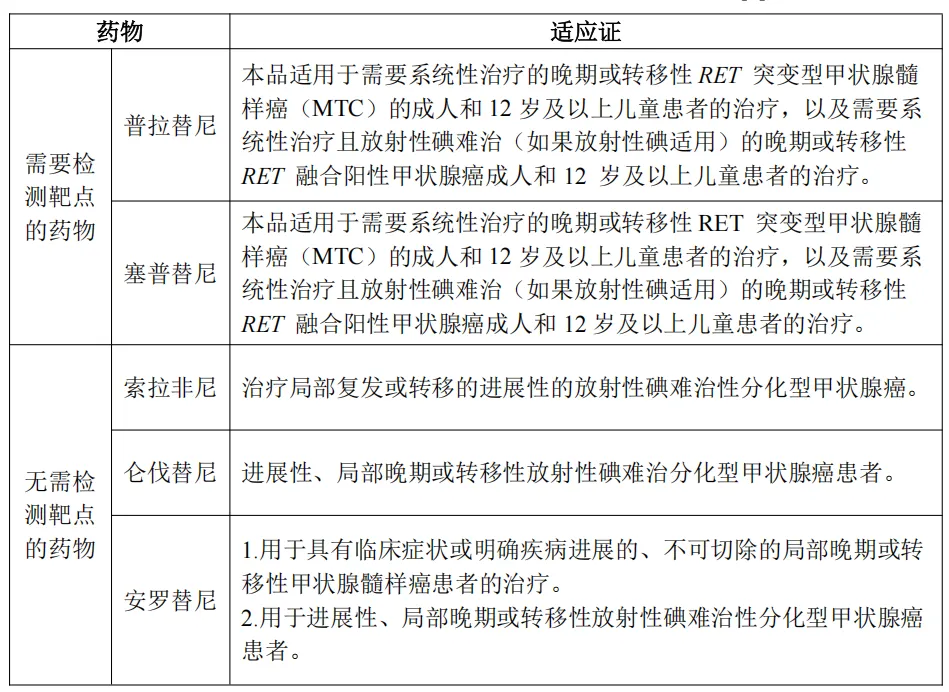
高通量测序(NGS)技术在甲状腺癌诊疗中发挥着关键的精准指导作用:它通过多基因联合检测,能有效辅助鉴别细针穿刺细胞学结果不明确的甲状腺结节良恶性;结合检测到的基因变异以指导靶向治疗;基因检测可预测RAI治疗敏感性与碘抵抗风险;通过肿瘤突变负荷(TMB)、微卫星不稳定性(MSI)等标志物助力免疫治疗患者的筛选;此外,基因变异信息还能与临床特征结合构建预后模型,精准预测复发风险并指导个体化随访方案,实现甲状腺癌的精准诊断与分层治疗。
伯科生物在国内已经建设了全流程国产化的高通量核酸合成与应用技术转化中心,建立了GMP厂房和ISO9001、ISO13485质量体系。已经为国内外数百家知名医院、科学研究机构、临床检验所开发了上千款Gene Panel(液相基因芯片),并配套完整的检测试剂,各项性能参数均与国际竞品相当或优于(详见附表1),在基因组、转录组、甲基化组及病原体的检测应用方向均有成熟的产品管线。
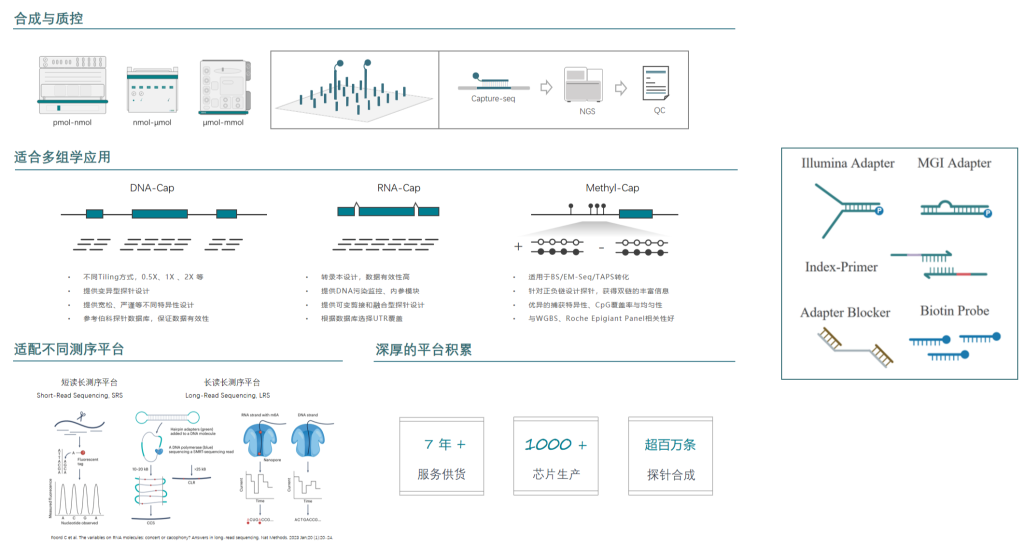
附表1: 产品简介
肿瘤液相基因芯片
伯科设计的TargetCap® OncoGene Plus Research Panel基于美国食品药品监督管理局(FDA)批准的用于肿瘤基因检测的FoundationOne CDxTM与MSK-IMPACTTM,其覆盖702个肿瘤相关基因编码区和34个基因的非编码区(融合基因),含有6个MSI和53个化药相关位点,探针覆盖2.32Mb区间。这些区域涵盖更多基因,检测范围更泛,涉及肿瘤高频突变、肿瘤易感、药物靶向、药物耐受等多种类型基因。
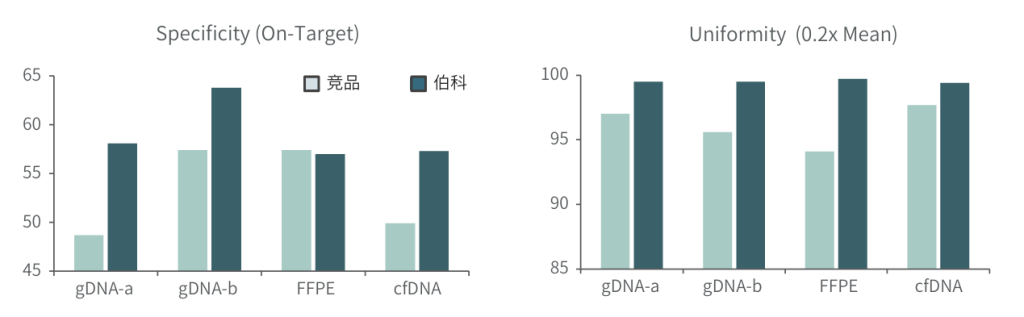
性能表现
竞品评测
采用gDNA/cfDNA/FFPE/泛肿瘤800gDNA标准品文库,分别使用伯科商品化肿瘤大Panel-OncoGene Plus Research Panel与竞品肿瘤大Panel进行性能比较(二者大小相近),在捕获特异性上(On-Target)和覆盖均一性(0.2XMean)上,伯科均优于竞品。
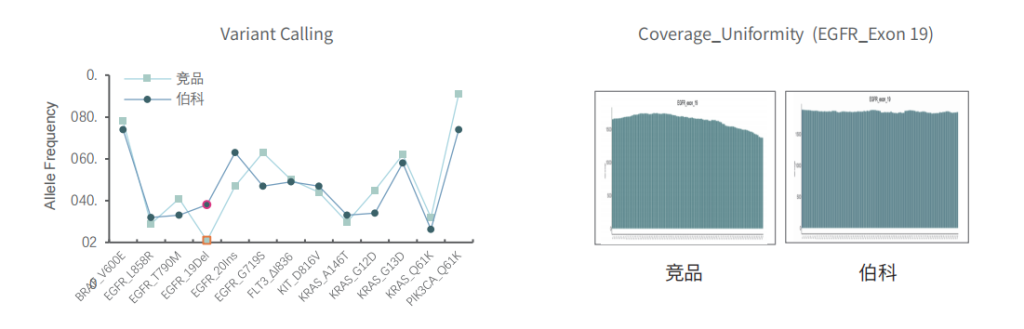
对于gDNA标准品,竞品测序35.9Gb,伯科测序19.6Gb,虽然伯科测序数据少,深度低,但二者的突变频率检出无明显差异,伯科对EGFR的19号外显子缺失变异的检出优于竞品。
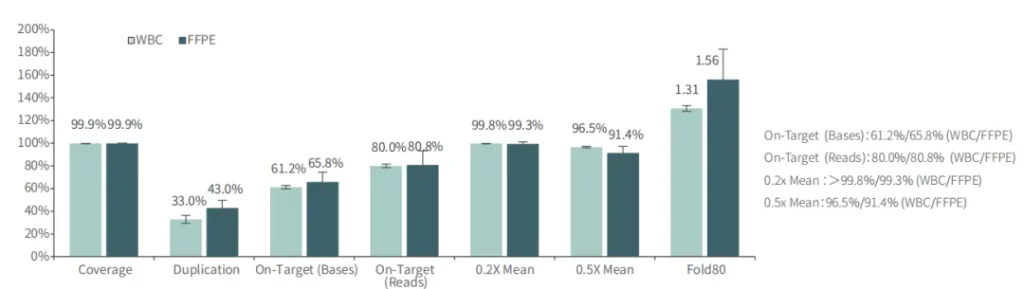
不同样本类型表现
对不同质量的gDNA样本 (WBC/FFPE, >150例),TargetCap® OncoGene Plus Research Panel表现稳定。
杂交与清洗试剂盒v2 简介
试剂盒概述
伯科杂交与清洗试剂盒v2 (TargetCap® Hybridization and Wash Kit v2,下文简称Hyb&Wash Kit v2)简化了试剂组分和操作流程,同时仍保持优异的捕获性能。Hyb&Wash Kit v2包含4种缓冲液组分,仅需3步清洗,操作流程更加便捷。
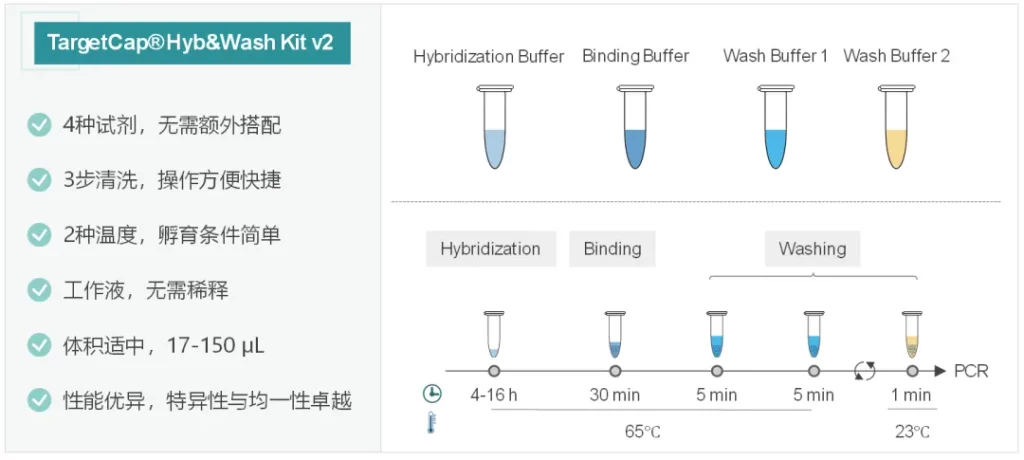
性能表现介绍
Ⅰ. 基本QC表现
使用NA12878和NA24694 gDNA标准品,采用三款不同大小的Gene Panel (650Kb、2.3Mb和42Mb) 对Hyb&Wash Kit v2 和 v1 进行比较测试。
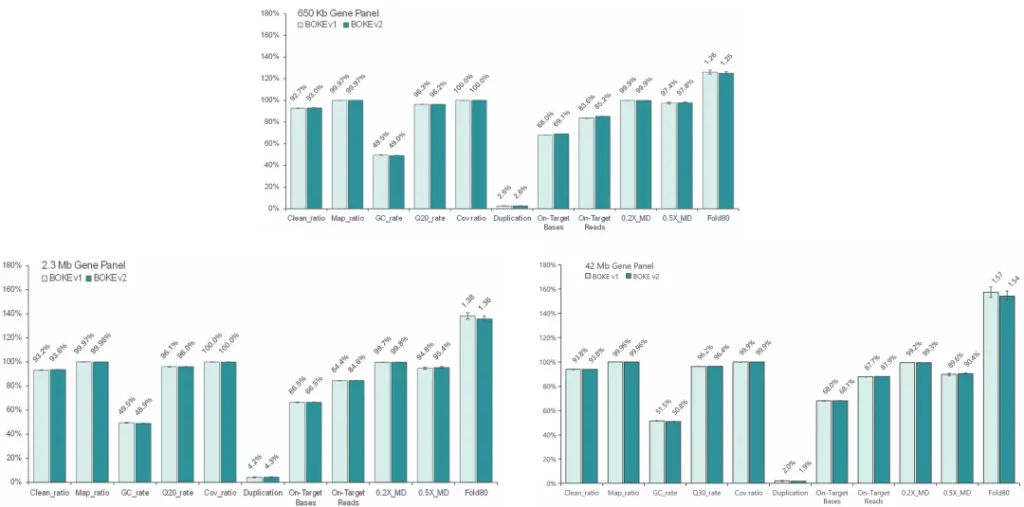
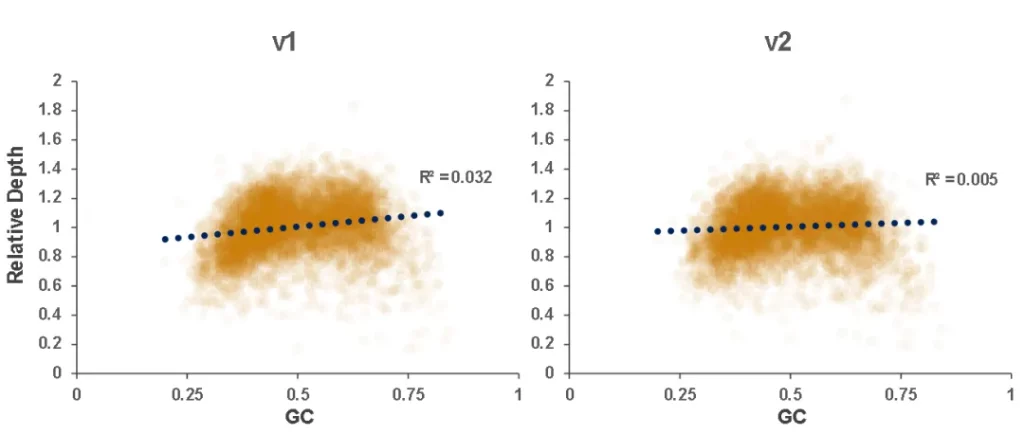
结果显示,在不同大小的Gene Panel中,对于杂交与清洗试剂盒的关键参数-中靶率和均一性,v2与v1试剂盒表现相当,v2试剂盒表现更好的均一性(0.2X_MD、0.5X_MD和Fold80)。
Clean_ratio、Map_ratio等基本参数两款试剂盒表现一致,由于v2试剂盒对低GC目标区域覆盖更佳,其GC_rate率略低于v1。
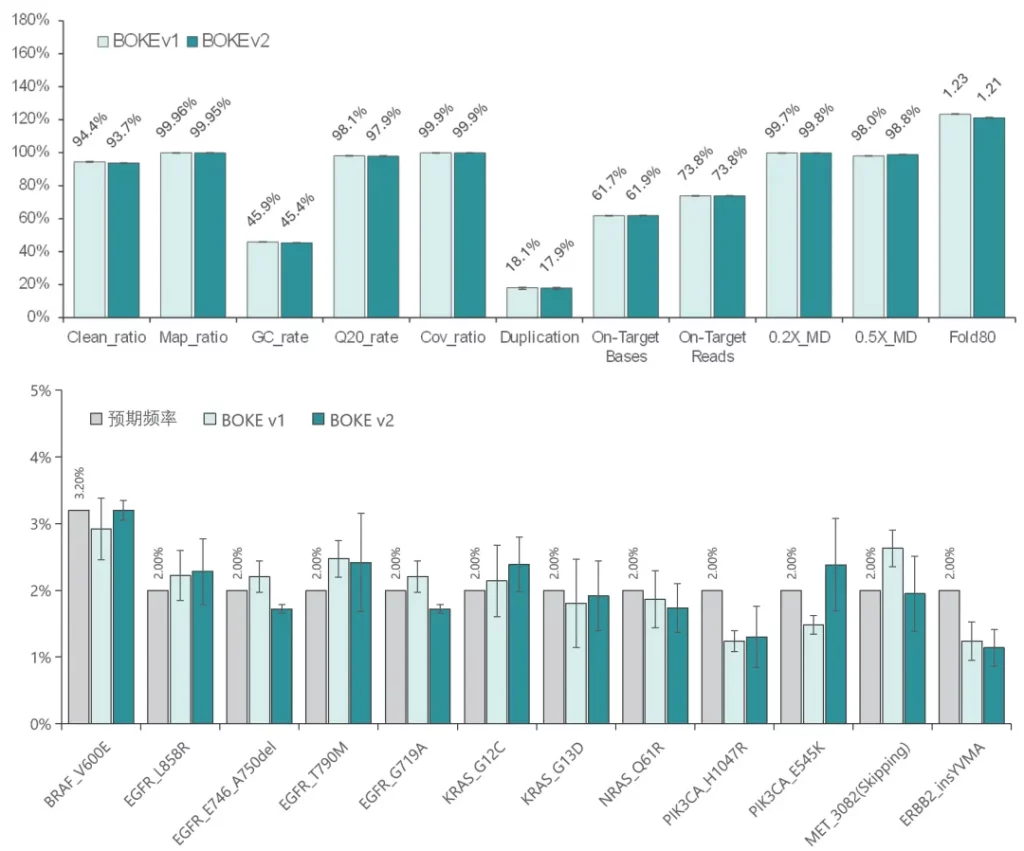
Ⅱ. 低频变异检测
使用肿瘤 SNV gDNA 标准品Ⅱ (GW-OGTM006) 对Hyb&Wash Kit v2的低频变异检测性能进行验证。GW-OGTM006 DNA标准品包含 EGFR、KRAS、NRAS、BRAF、PIK3CA、FGFR3、Her2、MET 等多个常见伴随诊断基因及位点,包含点突变、插入和缺失等多种变异类型。
采用300 Kb Gene Panel对该标准品进行捕获,捕获数据显示,v1与v2试剂盒的基本捕获性能表现相当,v2的中靶率与均一性略优于v1。同时,v1与v2试剂盒均能对12个已知变异准确检出。
参考文献:
1.Pizzato M, Li M, et,al. The epidemiological landscape of thyroid cancer worldwide: GLOBOCAN estimates for incidence and mortality rates in 2020. Lancet Diabetes Endocrinol. 2022 Apr;10(4):264-272.
2.NCCN Clinical Practice Guidelines in Thyroid Carcinoma (2025 Version 1).
3.中国家族遗传性肿瘤临床诊疗专家共识(2021年版)—家族遗传性甲状腺癌.
4.新型抗肿瘤药物临床应用指导原则(2025年版),国家卫生健康委


