2023NRG综述|回顾孟德尔遗传学:医学遗传学中的显性与隐性(二)
- boke
- 2023-04-28
- 7:07 上午
许多遗传疾病是由基因突变导致蛋白质功能改变造成的。在一项大型研究中发现,在发育障碍的de novo致病变异中,数量效应变异占57-59%,41-43%的变异属于质量效应变异。
本文讨论的质量效应包括:功能获得效应(gain of function,表1);显性负效应(dominant negative effects,图3);次级功能效应(sub function effects,图4a,b);多功能效应(Moonlighting-function effects图4c,d);以及组织特异性转录效应(tissue-specific transcript effects)。
功能获得(gain of function GoF)变异
功能获得(gain of function GoF)变异是一类导致编码蛋白质不受控地激活的变异。GoF机制通常与基因及所编码蛋白的氨基酸变化高度相关(表1)。例如,由于C1R或C1S中缺失或读码框内GoF变异引起的补体1亚单位C1s的不受控制剪切会导致常染色体显性牙周病性埃勒斯-丹洛斯综合征:正常被阻断的丝氨酸蛋白酶结构域的胞内自激活会导致结缔组织变化[4]。
相反,C1R或C1S的双等位基因LoF变异会引起一个与GoF表型无临床重叠的常染色体隐性系统性红斑狼疮样综合征。在KLF1基因中,GoF变异p.E325K改变被编码转录因子的DNA结合特异性,并导致先天性失调性造血细胞生成障碍IV[5]。
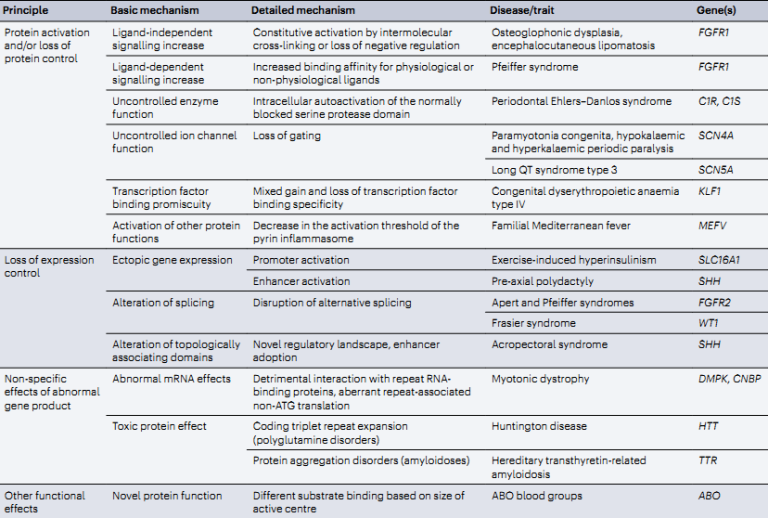
表1 功能获得(gain of function GoF)变异的几种示例
常染色体Gof变异通常与杂合子的临床表现有关,因为WT蛋白的正常功能或调节通常无法抵消异常变异的作用。一般来说,这种效应并不符合Mendel的显性定义,因为纯合基因型症状比杂合基因型更为严重。例如,由杂合FGFR3变异p.Gly380Arg引起的软骨发育不全症,纯合型通常导致产前或围产期死亡,而亨廷顿氏病杂合基因型和纯合基因型患者具有类似的临床表型[6,7]。
显性负效应(dominant negative effects,图3)
显性负效应(Dominant Negative, DN)是指单等位基因变异产生结构异常的蛋白质,异常蛋白会干扰正常蛋白的功能。表现为杂合个体可能比野生型或纯合基因型具有更不良的临床表现。
显性负效应的致病机制涉及变异对野生型蛋白功能的直接干扰或阻断,例如通过破坏同型或异型多聚体形成或功能,或者与野生型蛋白和其他分子之间的其他相互作用干扰(如图3a所示)。
先天性高胰岛素血症中p.Arg1353Pro变异属于LoF突变,在杂合状态下正常蛋白质数量减少但足以维持正常功能,而p.Arg1353His突变产生异常蛋白干扰野生型蛋白,表现为显性负效应。显性负效应在结构蛋白或多聚通道蛋白的变异中起着重要作用。
例如I型胶原蛋白,其中α1-链和α2-链的比例为2:1,每种Ⅰ型胶原基因的变异都导致骨发育不全症或脆性骨病(如图3b所示)。其中干扰三螺旋形成的错义突变通过显性负效应导致严重的表型。COL1A1序列中出现的胶氨酸(Gly)替换会导致致命的Ⅱ型骨发育不全症,而COL1A2中的Gly替换则产生中度的Ⅳ型骨发育不全症[8]。
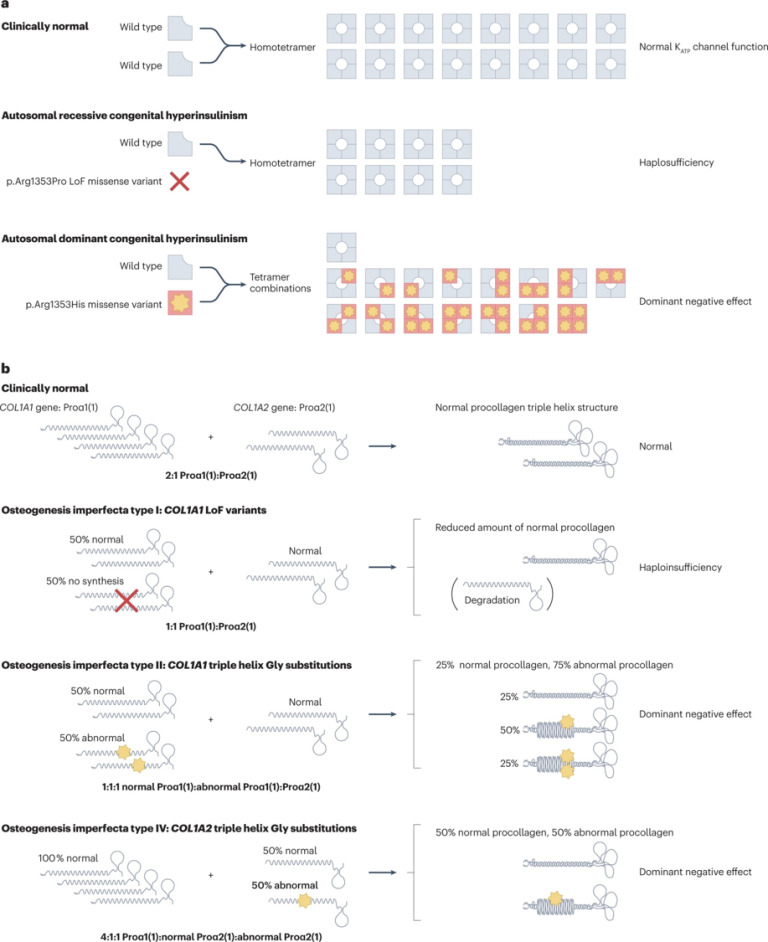
图3 显性负效应的表现形式
次级功能效应(sub function effects)
一些蛋白质在细胞过程中具有连续的功能,如酶促反应或运输过程中的连续步骤,这些功能可能会受到遗传变异影响(图4a)。例如载脂蛋白APOB基因中的变异抑制低密度脂蛋白(LDL)的产生导致血液中胆固醇浓度降低,而干扰LDL受体(LDLR)结合的变异则会导致家族性高胆固醇血症(图4b)。
APOB基因LoF变异导致脂蛋白不能形成,从而引起无脂蛋白血症。这种状态也可能由微粒体转移蛋白(MTP)基因的纯合型LoF变异引起。APOB杂合LoF变异导致自体半显性家族低β-lipoproteinaemia,血液中胆固醇、甘油三酯和ApoB浓度降低,多数情况下无症状。
多重功能效应(Moonlighting-function effects)
一些蛋白可以像多功能折叠刀一样组合不同的功能。蛋白质的功能丧失或质量效应变异产生的功能改变可能导致不同的疾病。例如线粒体蛋白17β-羟基甾体醇脱氢酶10(HSD10; SDR5C1)由HSD17B10基因编码。
HSD10作为线粒体3-甲基-2-羟基丁酸辅酶A脱氢酶(MHBD)参与缬氨酸分解,同时也是线粒体RNA酶P中一个组分,参与线粒体DNA的转录加工。HSD17B10变异可以分别影响两种功能[9],MHBD活性的缺陷引起尿中某些有机酸的积累,但RNaseP的缺陷导致了神经退行性症状。
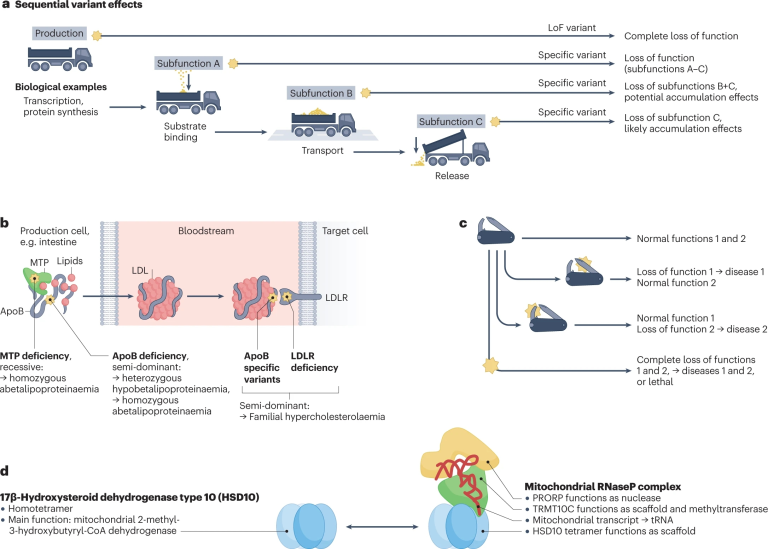
图4 蛋白质次级功能效应(sub function effects)和多重功能效应(Moonlighting-function effects)
转录差异会改变部分变异的影响
选择性剪接和不同起始密码子的使用允许从同一基因产生不同的蛋白质,并可以调节器官特有的基因功能。只影响某些转录本的致病变异可能会导致衰减或非典型的临床表型。例如,细胞骨架连接蛋白plectin的普遍缺陷会导致一种常染色体隐性遗传病,包括表皮水疱症和不定其他症状,如幽门闭锁和肌萎缩症,而在外显子1a中有致病变异的个体的临床特征仅限于皮肤。
等位基因型系列
由于基因改变对编码蛋白的影响通常多种多样,因此同一基因中的功能变异可能会表现出一系列非常不同(甚至相反)的表型,这种现象被称为等位基因型系列。有时不同变异会影响相同的细胞功能,导致细胞功能的降低或增加。例如,胰岛素分泌的减少或增加可以由葡萄糖激酶(GK)变异引起,分别导致显性或隐性单基因糖尿病和显性高胰岛素血症[10]。
相比之下,FAR1基因中的隐性LoF和显性GoF变异会引起相反的生化表型,但都具有发育迟缓、痉挛性麻痹、癫痫和白内障等相似临床表现[11]。参与发育调控的蛋白的杂合变异可能是致癌驱动因子,而LoF变异主要影响形态发生。
例如,RET原癌基因的遗传或体细胞活化变异会引发甲状腺癌和其他恶性肿瘤的发生[12],而LoF变异则是先天性巨结肠(Hirschsprung aganglionosis)的风险因素,同一家族中这两种变异同时出现被称为“Janus mutations”[13]。FGFR1基因中的变异对蛋白特性和信号功能产生不同的影响,显示出不同的表型(图5)。
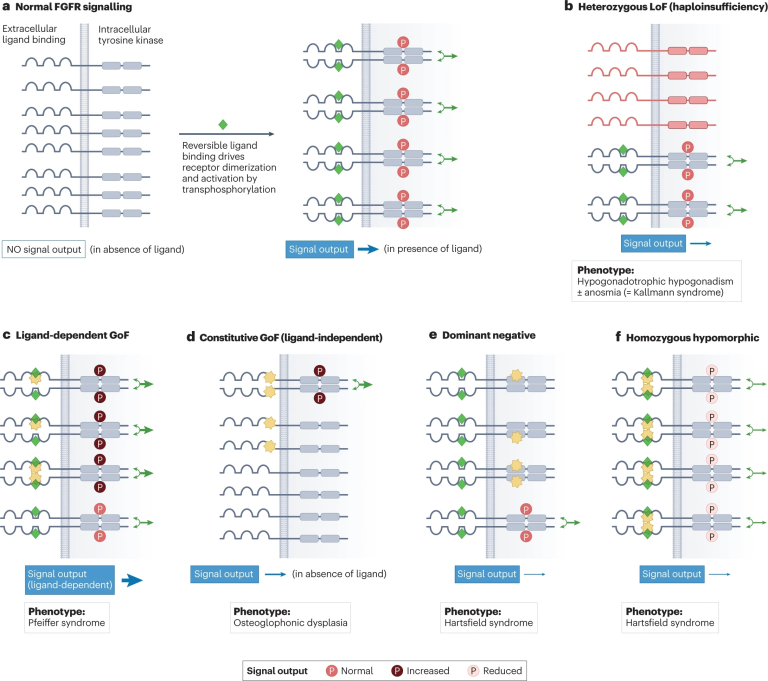
图5 FGFR1基因等位基因型系列突变与对应表型
杂合基因型可能具有选择性优势。隐性致病基因中的致病性变异可以与多个具有不同遗传模式和不同表现的特征相关,这些特征受到其他遗传和外源性因素的影响。杂合和纯合基因型的有利和不利影响之间的平衡促使人类适应不断变化的环境。
表观遗传因素也会干扰孟德尔遗传模式。有些疾病的单等位基因遗传规律并不遵循孟德尔的显性和隐性规律,而是与具有亲本特异性表达的印记基因相关。例如,15q11.2染色体上的UBE3A基因与安杰曼综合征相关,该基因在大脑中仅从母体等位基因表达。只有从母亲那里继承致病LoF变异才会引起疾病,并且可以在男性后代中隐性传递。





