预防猝死
- boke
- 2024-05-24
- 3:31 下午
载脂蛋白与疾病(APOB)
血脂是血清中的胆固醇、甘油三酯(Triglyceride,TG)和类脂(如磷脂)等的总称,与临床密切相关的血脂主要是胆固醇和 TG。由于血脂不溶于水,因此必须与特殊的蛋白质,即载脂蛋白(apoprotein,Apo),结合形成脂蛋白才能溶于血液,并被运输至组织进行代谢[1]。
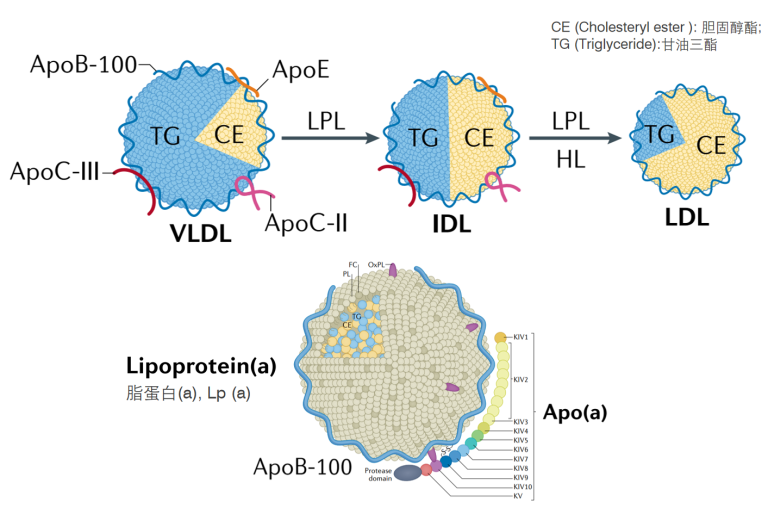
不同脂蛋白结合的载脂蛋白[2]
按照脂蛋白进行分类,包括乳糜微粒(chylomicron,CM)、极低密度脂蛋白(very low-density lipoprotein,VLDL)、中间密度脂蛋白(intermediate-density lipoprotein,IDL)、低密度脂蛋白(low-density lipoprotein,LDL)、高密度脂蛋白(high-density lipoprotein,HDL)和 脂蛋白(a)[ Lipoprotein(a), Lp(a)]。
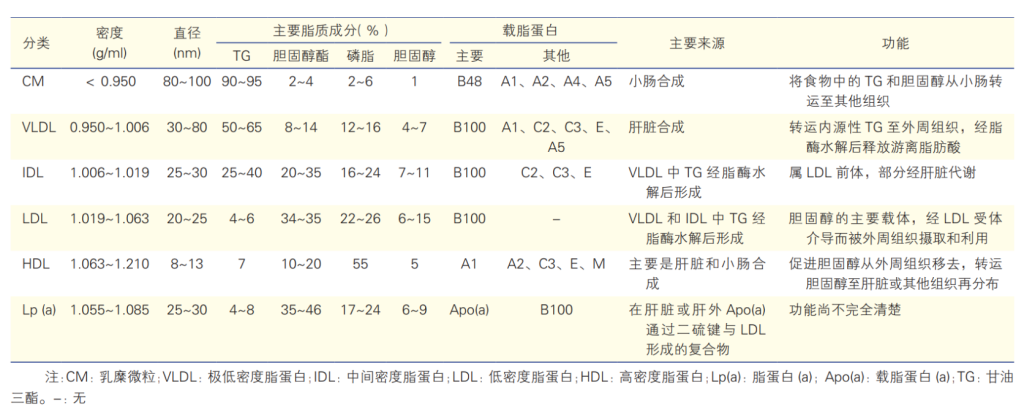
脂蛋白的物理及生物学特性和功能[1]
按照载脂蛋白进行分类包括载脂蛋白B-100 (ApoB-100)、载脂蛋白B-48 (ApoB-48)、载脂蛋白A-I (ApoA- I)、载脂蛋白C-II (ApoC-II)、载脂蛋白C-III (ApoC-I II)、载脂蛋白E (ApoE)、以及载脂蛋白(a)[Apo(a)]等。
不同的脂蛋白,其结合的载脂蛋白种类会存在差异。例如,极低密度脂蛋白(VLDL)除结合载脂蛋白ApoB-100外,还包括ApoC-II、ApoC-III和ApoE等载脂蛋白;低密度脂蛋白(LDL)由VLDL转化而来,但LDL中的载脂蛋白95% 以上为ApoB-100,而脂蛋白(a)[ Lipoprotein(a), Lp(a)]则包括Apo-B100和Apo(a)两种载脂蛋白。载脂蛋白在人体胆固醇稳态中发挥着重要作用,一旦发生功能变异,则会导致严重的疾病。
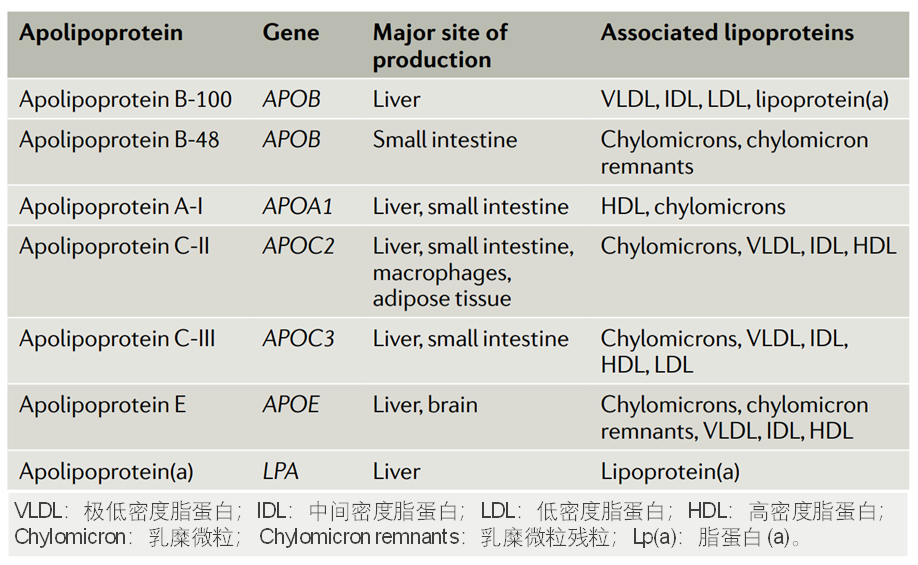
载脂蛋白的编码基因、合成组织和相关的脂蛋白[2]
APOB
正常人群中血清ApoB在0.80~1.10g/L范围内。正常情况下,每一个LDL、IDL、VLDL和Lp(a)颗粒中均含有1分子ApoB。ApoB有ApoB48和ApoB100两种亚类,前者主要存在于乳糜微粒中,后者主要存在于LDL中。除特殊说明外,临床常规测定的ApoB通常指的是ApoB100。血清ApoB主要反映LDL颗粒水平,与血清LDL-C水平呈明显正相关,两者的临床意义相似[1]。
载脂蛋白ApoB-100的羧基端含有LDLR(低密度脂蛋白受体)结合结构域,该结构域负责触发受体介导的LDL颗粒的内吞作用。肝脏是LDL清除的主要部位,apoB-100–LDLR相互作用在调节血液LDL水平方面具有重要作用,APOB基因变异将会导致血液LDL水平紊乱。
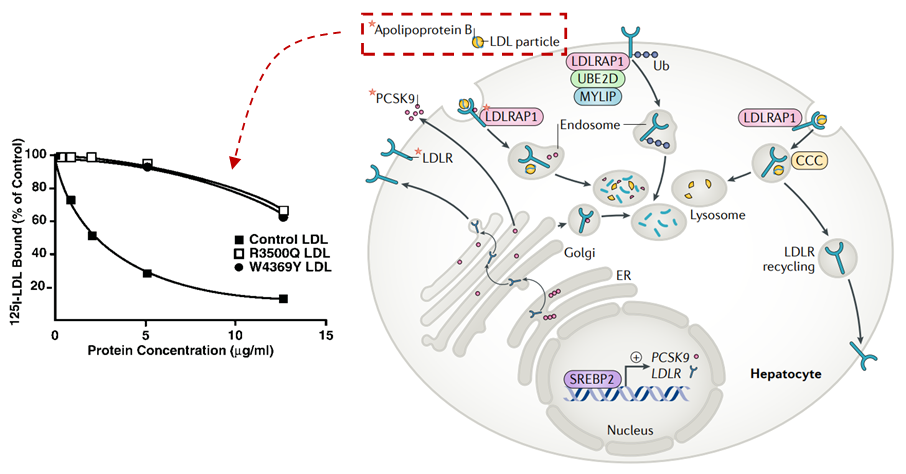
LDLR(低密度脂蛋白受体)代谢循环(APOB变异导致LDL与LDLR结合能力降低,左)[3、4]
家族性高胆固醇血症(Familial Hypercholesterolaemia, FH)是常见的常染色体单基因遗传性疾病,其临床特征为胆固醇和低密度脂蛋白胆固醇(LDC-C)水平显著升高、黄色瘤及早发和进展性动脉粥样硬化性心血管疾病,根据发病机制和临床表型可分为纯合子FH(HoFH)和杂合子FH (HeFH),。
基因检测证实,单基因致病的FH在社区人群中的患病率为1/(200-250)人,在高胆固醇血症和早发急性冠状动脉综合征患者中高达1/10。FH最常由LDLR(低密度脂蛋白受体)的遗传变异引起,APOB基因突变约占FH基因突变的5%[5]。
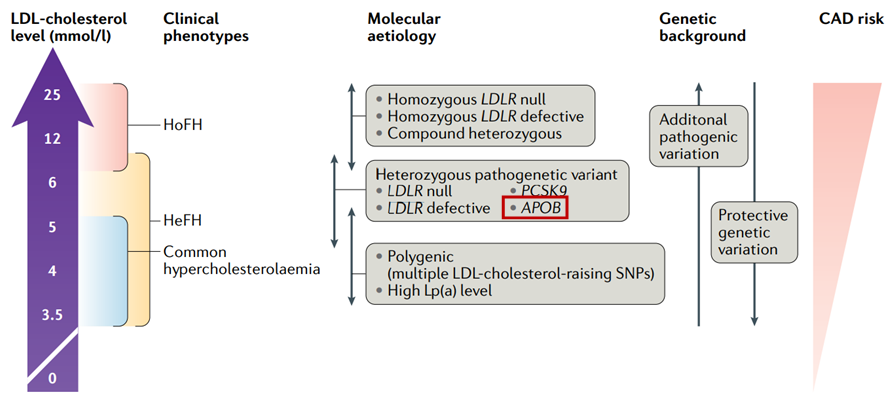
FH表型和遗传谱[5]
其中,家族性apoB-100缺陷症是一种罕见的家族性高胆固醇血症,由APOB的遗传变异引起,该变异降低了ApoB-100与LDLR之间的结合亲和力,最常见的致病性APOB变体是Arg3500Gln。其特征是血浆LDL-C水平升高(尽管其升高程度低于由LDLR变异引起的家族性高胆固醇血症患者)和早发动脉粥样硬化性心血管疾病(ASCVD)风险增加。
家族性低β脂蛋白血症由APOB的无义或移码变异引起,产生截短的ApoB载脂蛋白亚型,这些亚型通常无功能且被快速分解代谢。这种疾病的特征是致使ApoB载脂蛋白的合成异常,血浆中LDL-C和载脂蛋白ApoB水平显著降低(<5百分位)、肝脂肪变性,在一些患者中还有肝硬化。复合杂合子或纯合子患者有严重的低胆固醇血症和无法测量的LDL-C水平,其表型类似于糖尿病脂蛋白血症。
FH早期发现和降脂治疗可以预防青年和中年早期ASCVD事件,并降低患者一生的风险。2022年,在《Journal of the American Heart Association》发表的研究报告[6],通过结合临床标准和基因检测技术筛查FH,为加强FH患者的识别和早期治疗提供可能。该研究利用49738名参与者(UK Biobank)的临床特征和FH变异信息,建立回归模型来预测出现任何FH变异的概率。结果发现,将基因检测加入目标人群的临床筛查标准中可以提高FH筛查率,有助于进行早期预防治疗。
参考资料
1. 中国血脂管理指南(2023 年). 中国循环杂志 2023 年 3 月 第 38 卷 第 3 期(总第 297 期)
2. Mehta A, Shapiro M D. Apolipoproteins in vascular biology and atherosclerotic disease[J]. Nature Reviews Cardiology, 2022, 19(3): 168-179.
3. Berberich A J, Hegele R A. The complex molecular genetics of familial hypercholesterolaemia[J]. Nature Reviews Cardiology, 2019, 16(1): 9-20.
4. Borén J, Ekström U, Ågren B, et al. The molecular mechanism for the genetic disorder familial defective apolipoprotein B100[J]. Journal of Biological Chemistry, 2001, 276(12): 9214-9218.
5. Watts G F, Gidding S S, Mata P, et al. Familial hypercholesterolaemia: evolving knowledge for designing adaptive models of care[J]. Nature Reviews Cardiology, 2020, 17(6): 360-377.
6. Bellows BK, et al. Estimated Yield of Screening for Heterozygous Familial Hypercholesterolemia With and Without Genetic Testing in US Adults. J Am Heart Assoc. 2022 Jun 7;11(11):e025192. doi: 10.1161/JAHA.121.025192. Epub 2022 May 18. PMID: 35583136; PMCID: PMC9238728.


