新英格兰医学杂志|阐述冠状动脉疾病的多遗传因素基础,早期干预是高PRS风险人群预防冠心病的有效策略
- boke
- 2026-02-11
- 9:40 上午
摘要
对冠状动脉疾病遗传基础的研究已在机制认知、治疗、预防和风险预测方面取得进展。事实上,当代大多数冠状动脉疾病治疗药物均以基础遗传机制介导的动脉粥样硬化相关通路为靶点。冠状动脉疾病的单基因病因发生率约为1/250,且大多会导致血脂水平显著升高。在人群层面,数百种效应量较小的常见变异影响更为显著,可整合为多基因风险评分,用于评估个体相对于普通人群平均水平的遗传风险。评分处于前5%的人群,其患病风险是评分平均水平人群的3-5倍;多基因风险评分得出的相对风险可与临床风险评分得出的绝对风险相乘,以优化风险评估。目前,关于多基因风险评分应用于临床实践的临床价值、成本效益及实施策略,仍存在关键问题有待解决。
冠状动脉疾病的发生是行为、环境、遗传和随机因素共同作用的结果。吸烟、高血压、高脂血症和糖尿病是公认的可改变风险因素,一生中男性患病风险约为1/2,女性约为1/3。一个多世纪前,Osler观察到心绞痛常呈家族聚集性,提出遗传因素可能导致冠状动脉疾病。约30年前,双生子研究表明,致死性冠状动脉疾病的遗传率高达50%。2007年以来,大规模基因分型和基因测序研究已鉴定出数百种与冠状动脉疾病易感性增加相关的遗传变异(图1及互动图表)。部分相关基因的蛋白产物已成为有效治疗靶点,其他基因则指向目前尚未探索的疾病机制。
询问冠状动脉疾病家族史是胸痛综合征患者临床评估的常规项目。本文综述了冠状动脉粥样硬化分子遗传起源的最新发现,并探讨了该类信息当前及潜在的临床应用。
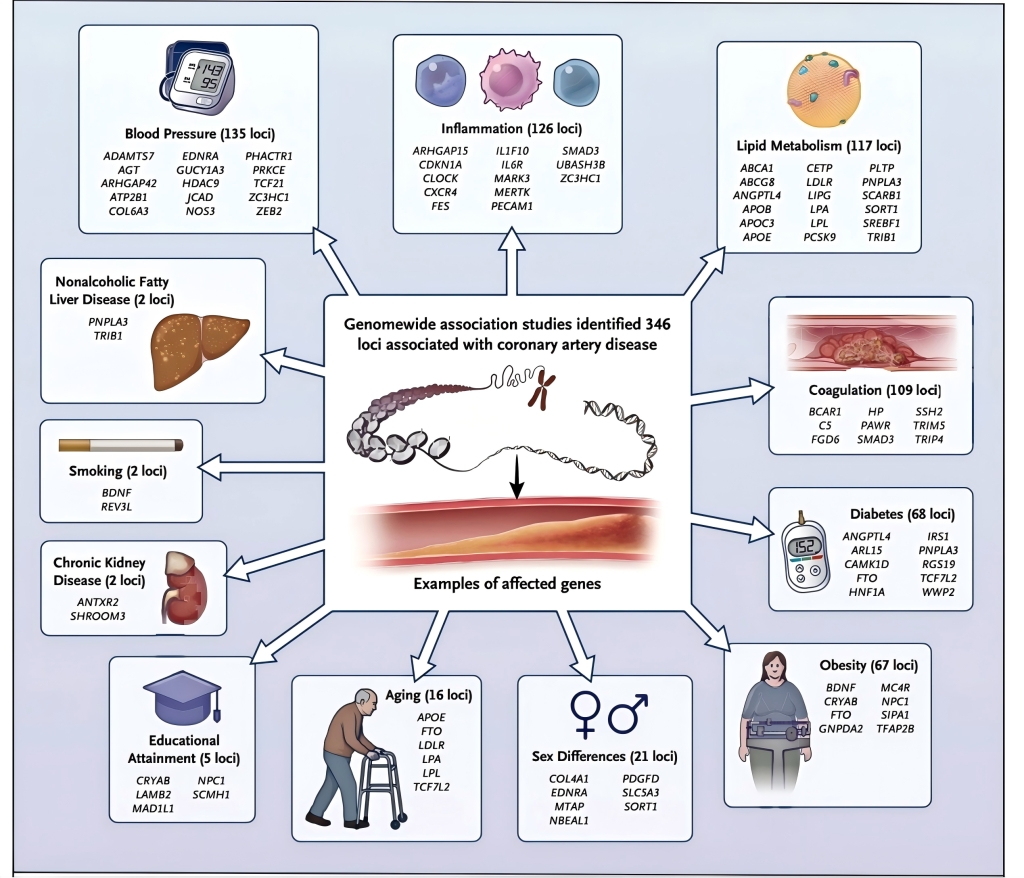
图1.与冠状动脉疾病相关的基因座
全基因组关联研究显示,346个基因座与冠状动脉疾病有显著关联。图中显示在部分基因座中,已被证实与该疾病已知危险因素、风险调节因素及临床状况显著相关的致病基因。括号内数字表示同时存在冠状动脉疾病及相应性状全基因组信号的基因座总数(部分基因座与多种性状显著相关)。共计76个风险基因座与上述性状无关联,其与冠状动脉疾病的关联机制有待探索。更多信息参见补充附录(补充附录随本文全文可在NEJM.org获取)
冠状动脉疾病的单基因遗传形式
冠状动脉疾病典型的分子遗传病因是家族性高胆固醇血症,这是一种不完全显性的单基因疾病。该疾病于1938年由米勒首次描述,在随后约70年里一直是唯一被证实的冠状动脉疾病遗传病因。到45岁左右,约20%的杂合子家族性高胆固醇血症患者会出现动脉粥样硬化相关疾病。家族性高胆固醇血症的致病遗传变异通常会导致低密度脂蛋白(LDL)受体功能减弱、载脂蛋白B功能改变,或前蛋白转化酶枯草溶菌素9(PCSK9)功能增强。
当LDL胆固醇水平显著升高时(成人>190 mg/dL[4.9 mmol/L];儿童>150 mg/dL[3.9 mmol/L]),应怀疑家族性高胆固醇血症。若同时存在LDL升高与早发性冠状动脉疾病、睑黄瘤或腱黄瘤,临床怀疑会显著提高;在家族性高胆固醇血症的临床评分系统中,除LDL胆固醇水平严重升高外,早发性冠状动脉疾病、睑黄瘤或腱黄瘤等疾病被赋予最大的权重。普通人群中致病性变异的患病率约为0.4%,而LDL胆固醇水平超过190 mg/dL的人群中,患病率约为3.5%。在其他检查提示可能或确诊家族性高胆固醇血症的人群中,变异检出率分别为5%和24%。
明确家族性高胆固醇血症的分子遗传诊断具有重要意义:即使LDL胆固醇水平相近,携带家族性高胆固醇血症特异性变异的人群,其冠状动脉疾病风险也是非携带者人群的2-3倍。此外,经基因证实的家族性高胆固醇血症患者,从LDL胆固醇降低治疗中获益更为显著;这一获益也体现在相关指南中 – 指南建议家族性高胆固醇血症患者的LDL目标值低于非家族性高胆固醇血症患者的一级预防目标值。遗憾的是,全球范围内家族性高胆固醇血症的基因检测利用率较低,导致错失对一级亲属进行指南推荐的级联筛查的机会。目前正在开展儿童家族性高胆固醇血症人群筛查相关研究,以期通过早期预防治疗降低冠状动脉疾病风险。
其他单基因形式的冠状动脉疾病极为罕见,仅占该病总高患病率的一小部分。常染色体隐性遗传病,如常染色体隐性高胆固醇血症(由LDLRAP1基因变异导致)、谷固醇血症(ABCG5和ABCG8基因变异)、弹性纤维假黄瘤(ABCC6基因变异),常与早发冠状动脉疾病相关。一氧化氮通路相关基因(GUCY1A1和PDE5A)、甘油三酯调节相关基因(APOA5)、胆固醇转运相关基因(SCARB1)中的罕见变异,也已被证实与早发冠状动脉疾病相关。在分子遗传评估的扩展检测panel中,除了家族性高胆固醇血症常见相关基因(LDLR、APOB和PCSK9)的变异,还可纳入这些基因的临床显著性变异。
冠状动脉疾病的多基因遗传贡献
尽管LDLR等基因的罕见致病性变异会对患者健康造成严重损害,但效应量较小的常见风险等位基因在人群层面的影响更为显著。20世纪50年代,Platt和Pickering就高血压是单基因遗传还是多基因遗传展开争论。随后的数学模型表明,多个效应量较小的常见风险等位基因导致的高血压病例数,多于效应量显著的罕见变异。
冠状动脉疾病全基因组关联研究已验证了这一假设。基因分型芯片可同时检测数十万个单核苷酸多态性(SNP)的等位基因,结合统计学推算的未分型SNP,能够高效完成常见变异的全基因组基因分型。全基因组关联研究通过比较患者与健康人群中每个SNP的等位基因频率,以P值<5×10⁻⁸作为全基因组显著性的严格标准。最新的全基因组关联研究荟萃分析纳入了超过18万名冠状动脉疾病患者,总样本量超过100万人,鉴定出346个具有全基因组显著性的风险区域(又称位点)(图1及互动图表)。据预测,仍有更多相关变异有待发现。具体而言,频率较低、全球分布差异显著或效应量更小的风险等位基因,需要更大规模、更多样化的队列研究来鉴定。大规模测序研究可能有助于填补这一空白。值得注意的是,这些遗传变异影响的基因在多种组织和细胞类型中表达,共同导致个体对冠状动脉疾病的易感性(图2)。这些发现主要应用于两个关键领域:心血管风险预测和治疗。
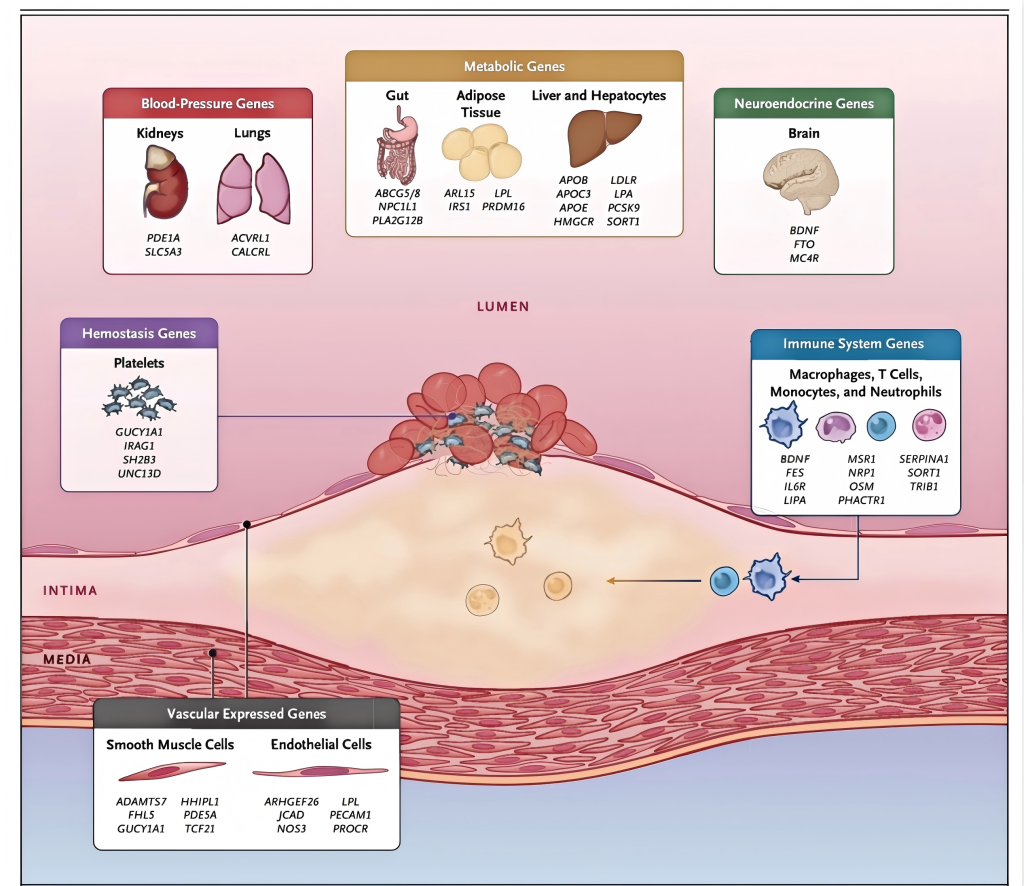
图2. 影响冠状动脉疾病风险的基因表达位置
图片显示了影响冠状动脉疾病风险的基因表达最丰富的组织与器官,同时显示了全基因组范围内与冠状动脉疾病显著相关的基因,这些基因具有高度组织特异性表达特征。动脉壁位于中心位置,其中动脉粥样硬化的关键细胞水平促进因素被突出标注。动脉壁上方显示与冠状动脉疾病病理生理学相关的其他器官和组织。基因表达通过人类蛋白质图谱进行识别,并通过基因型–组织表达(GTEx)项目、STARNET及文献数据进行交叉验证。更多信息参见补充附录。
心血管风险预测
1
临床风险评估
指南建议对无明确冠状动脉疾病的人群计算整合临床因素的风险评分,以识别动脉粥样硬化性心血管事件风险显著升高、值得接受预防治疗的个体。这些风险评估受实际年龄影响较大,导致年轻高风险人群的识别率较低。尽管冠状动脉疾病家族史被公认为主要风险因素,但由于其缺乏足够的额外鉴别价值,目前尚未纳入临床风险评分体系。
2
多基因风险评估
冠状动脉疾病风险等位基因的效应量较小,单独使用无法用于风险预测。然而,多基因风险评分整合的信息为优化风险预测提供了可能。由于多个常见风险等位基因独立遗传,普通人群中冠状动脉疾病多基因风险评分呈正态分布(图3A)。分布处于前5%的人群,其患病风险是人群中五分位数中间水平人群的3-5倍(图3B),且该结果独立于冠状动脉疾病家族史状态。由于全基因组显著性变异(图1及互动图表)仅占疾病相关变异总数的一小部分,当前的多基因风险评分纳入了所有具有信息价值的遗传变异——每个变异均与冠状动脉疾病或卒中存在微弱关联,以全面评估遗传易感性。随着全基因组关联研究规模扩大、多样性增加以及新方法的应用,多基因风险评分的性能持续提升。
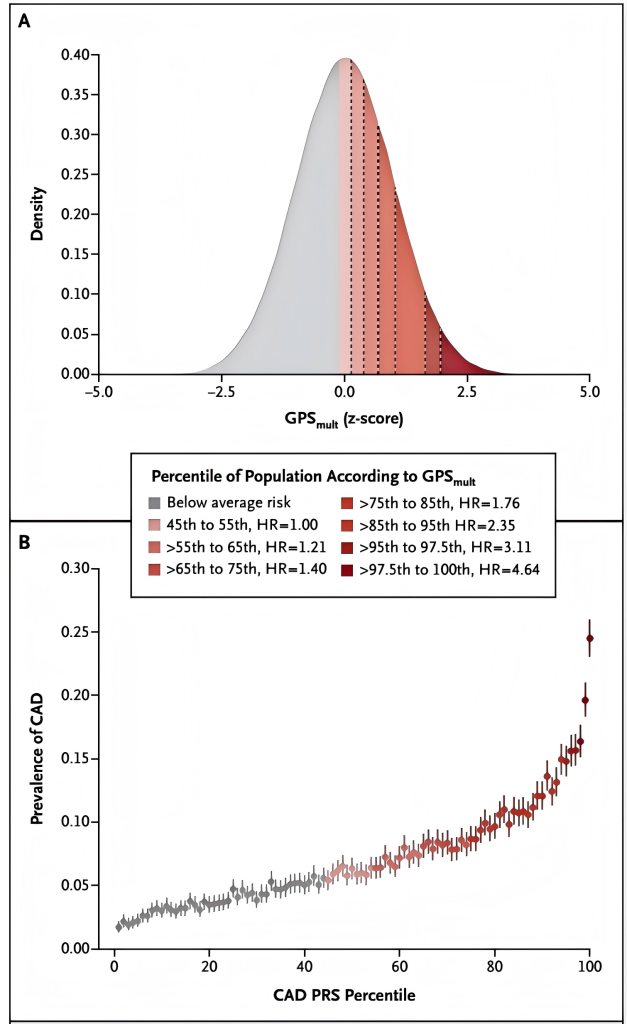
图3.冠状动脉疾病(CAD)的多基因风险评分(PRS)
每个人通过随机遗传机制继承数百个冠状动脉疾病风险等位基因。人群中个体携带的风险等位基因数量呈现高斯分布(如图A所示)。密度(y轴)对应每GPS mult标准差的观测值数量(经样本量校正),使总面积等于1。GPS mult指先前发表的冠状动脉疾病多基因风险评分。图B显示在PRS高于均值的人群中,冠状动脉疾病的风险比(HR)。图B显示尽管单个风险等位基因的效应较小,但它们具有乘数效应,导致风险呈指数级增长。两张图数据均来自英国生物样本库。
3
临床与多基因联合风险评估
完成基线临床风险评估后,冠状动脉疾病的多基因风险评分最具参考价值。多基因风险评分得出的相对风险可与临床风险评分得出的绝对风险相乘。因此,若临床风险较低,冠状动脉疾病多基因风险评分的影响也较小。在10年内心肌梗死或卒中临床概率为中等(5%-10%)的人群中,冠状动脉疾病多基因风险评分可将10%的个体归为高风险类别,其心血管疾病事件风险是多基因风险评分非高风险个体的两倍(图4A)。该策略每筛查340人可额外预防1例心血管疾病事件,约占所有事件的7%。
将多基因风险评分用于优化临床风险评估,与当前指南一致 – 指南建议结合额外因素进一步明确个体化风险。指南已为临床医生提供了相应行动指导,包括对高多基因风险评分等归为高风险类别的个体,进行进一步诊断检查(如冠状动脉钙化筛查)或预防性降脂治疗。随机试验的回顾性分析一致表明,冠状动脉疾病多基因风险评分高的人群,从降脂治疗中获得的绝对和相对获益均大于评分平均水平的人群(图5)。在一项针对中等冠状动脉疾病风险成人的单中心随机试验中,在一项针对冠状动脉疾病中等风险成人的单中心随机试验中,告知其多基因风险评分在近10年间降低了主要心血管不良事件发生率。
冠状动脉疾病多基因风险评分的另一适用人群是年轻成人——临床风险评分在该人群中校准效果不佳,仅能识别约1/4后续发生主要心血管疾病事件的个体。队列研究显示,40岁、无临床风险因素的男性中,多基因风险评分处于最高五分位数者,70岁前患冠状动脉疾病的风险为30%-40%,而最低五分位数者的风险仅为10%(图4B)。此类信息可能对临床诊疗具有重要意义,因为他汀类药物等预防治疗在疾病进展早期实施时,效果通常更为显著。此外,在传统风险因素患病率较低的生命早期,多基因风险对总体长期风险的贡献更大。基于多基因风险评分优先实施预防治疗的终身风险模型,仍需前瞻性研究继续验证。
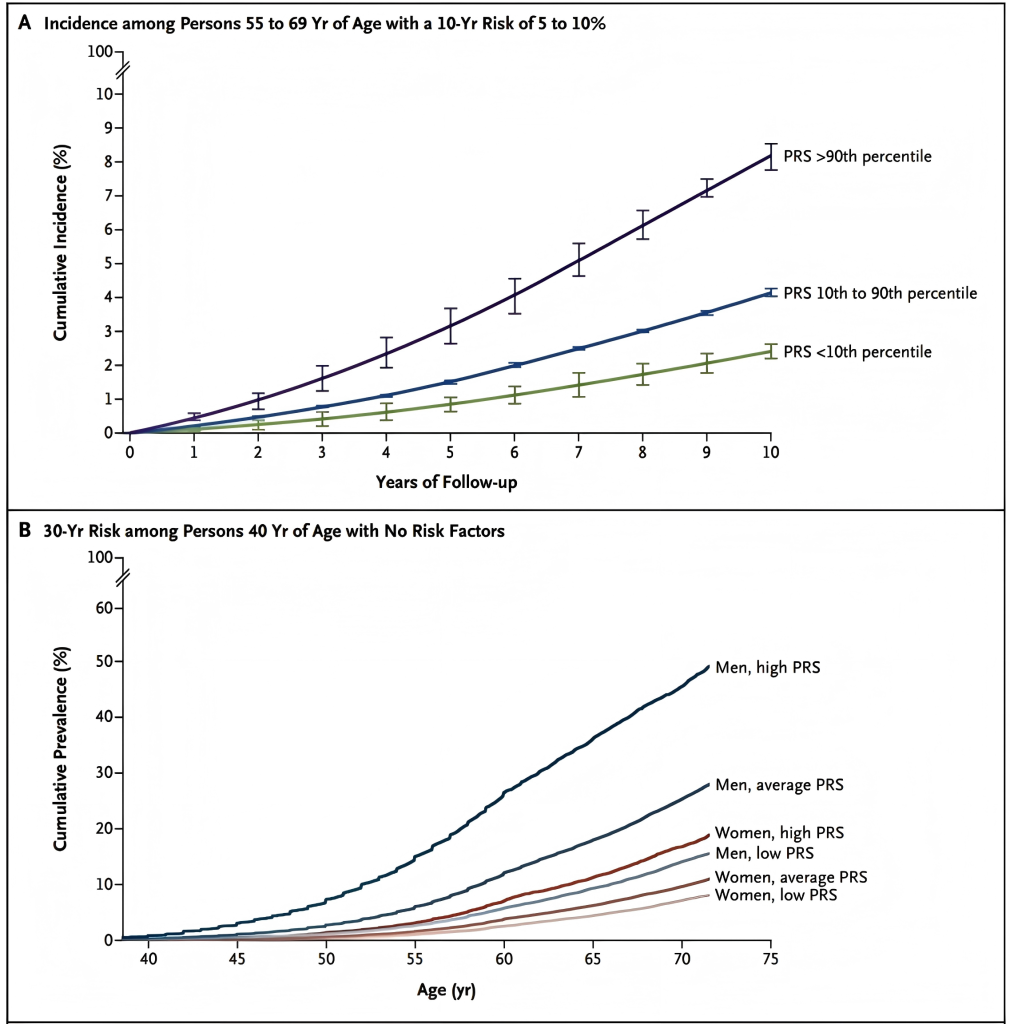
图4.根据多基因风险分类的动脉粥样硬化性心血管疾病事件的轨迹
根据英国生物样本库数据绘制的图A显示,在55~69岁人群中,使用SCORE2工具计算的动脉粥样硬化性心血管疾病事件风险为5%~10%。尽管SCORE2等风险预测工具对英国生物库人群的发病率存在高估,但观测到的发病率仍基本上随多基因风险变化而变化.研究将样本随机划分为10组,计算各组平均累积发病率及标准差。同样基于英国生物库数据的图B显示,在40岁且无临床危险因素的男性和女性中,冠状动脉疾病的长期风险也随多基因风险变化而变化。目前使用的临床风险评分无法充分预测年轻人群的冠状动脉疾病长期风险。在该亚群体中,冠状动脉疾病的多基因风险可能为预测未来风险提供有用信息。
第三类可能从多基因风险评估中获益的人群是早发冠状动脉疾病患者——高多基因风险可能是其疾病发生的原因之一,因此有助于明确病因。在这类患者中,高多基因风险评分可预测复发事件,但预测价值低于一级预防。尽管目前高多基因风险评分在确诊冠状动脉疾病患者中的临床应用价值尚不明确,但在治疗方案存在不确定性时,高评分可能提示需要强化治疗。
针对具有较高基因风险患冠状动脉疾病者的治疗措施
1
家族性高胆固醇血症
临床试验表明,与其他冠状动脉疾病风险人群相比,家族性高胆固醇血症患者从强化降脂治疗中获得的绝对获益更为显著。因此,指南建议对家族性高胆固醇血症患者,即使在成年早期,也应启动一级预防降脂治疗,目标LDL胆固醇值低于70 mg/dL(1.8 mmol/L)。根据欧洲指南,对于携带家族性高胆固醇血症致病遗传变异且持续存在临床显著性高胆固醇血症的儿童,可启动他汀类药物治疗,将LDL胆固醇水平降至135 mg/dL(3.5 mmol/L)以下。纯合子家族性高胆固醇血症是危及生命的疾病,冠状动脉疾病常在儿童期发病,显著升高的LDL胆固醇水平需要在专科中心接受强化治疗。
2
高多基因风险
与家族性高胆固醇血症等主要通过单一风险因素发挥作用的单基因疾病不同,冠状动脉疾病多基因风险评分代表了多种致病风险因素和未知风险通路的异质性组合。然而,冠状动脉疾病多基因风险同样可被显著改变。观察性研究表明,健康生活方式可能在很大程度上抵消高多基因风险评分的影响(图5)。此外,多项一级和二级预防随机试验的事后分析反复显示,他汀类药物或PCSK9抑制剂治疗,可使冠状动脉疾病高多基因风险评分人群获得更大的绝对和相对风险降低。这些研究支持以下观点:降脂治疗是降低高多基因风险评分人群冠状动脉疾病风险的特别有效策略(图5)。
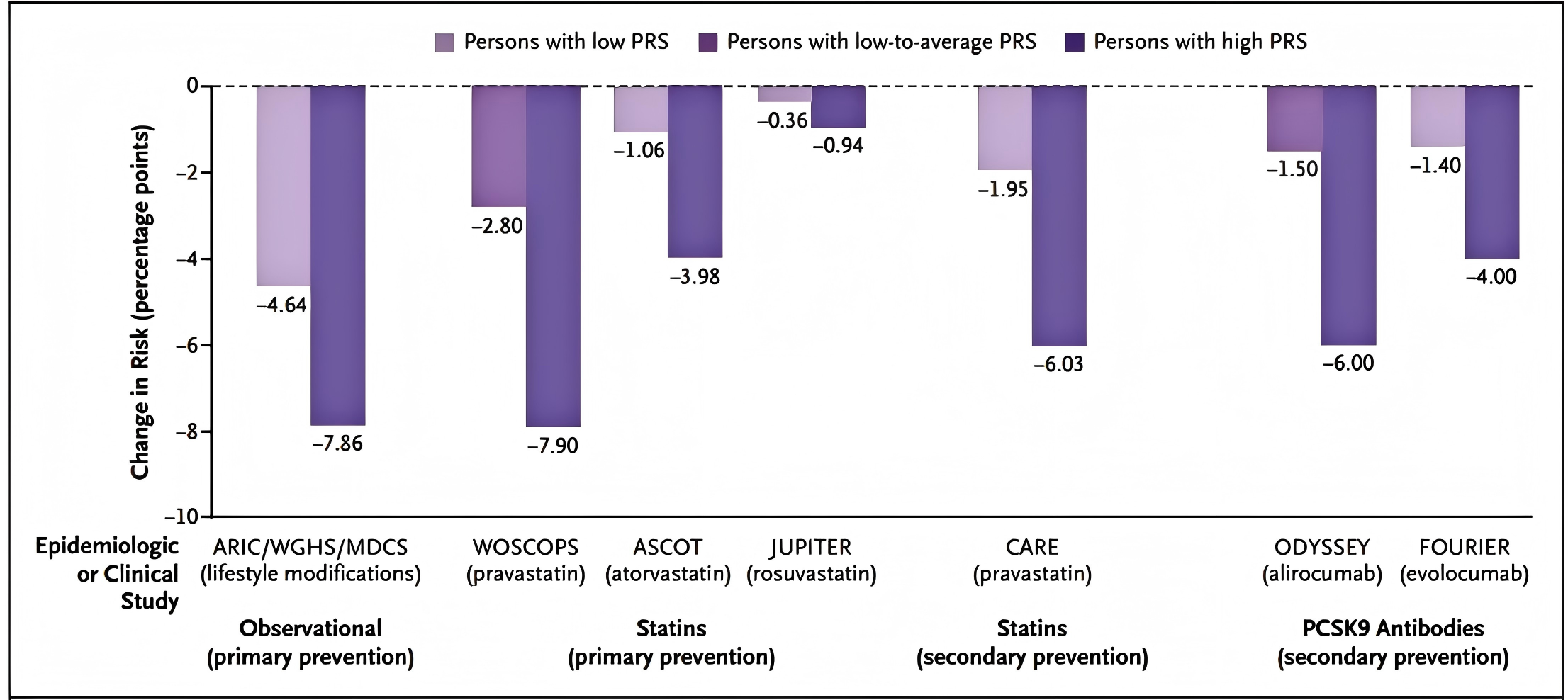
图5.根据PRS,通过改变生活方式或降脂治疗降低风险
流行病学研究和临床试验表明,在20年期间,生活方式干预与新发动脉粥样硬化性心血管疾病事件发生率降低相关,其中高PRS人群的风险降幅最大。生活方式干预数据源自以下流行病学研究:社区动脉粥样硬化风险研究(ARIC)、女性基因组健康研究(WGHS)及马尔默饮食与癌症研究(MDCS)。同样,他汀类药物及PCSK9抗体试验均显示,高PRS人群的绝对风险降幅超过低PRS人群。降脂治疗数据源自以下研究:苏格兰西部冠心病预防研究(WOSCOPS)、英格兰-斯堪的纳维亚心脏结局试验(ASCOT)、他汀预防应用论证:瑞舒伐他汀干预试验(JUPITER)、胆固醇与复发事件研究(CARE)、alirocumab治疗急性冠脉综合征后心血管结局评估(ODYSSEY OUTCOMES),以及高危人群PCSK9抑制剂心血管结局研究(FOURIER)。更多信息参见补充附录。
将遗传架构转化为新型治疗策略
利用冠状动脉疾病的遗传结构推进治疗发展是一项值得关注的策略。由于等位基因分配是随机的,且在个体一生中保持不变,风险等位基因可指向致病机制,为治疗靶点优先级排序提供依据。事实上,有人类遗传学证据支持的研究性药物,获得监管批准的可能性高于缺乏遗传支持的药物。
家族性高胆固醇血症致病性LDLR基因变异及冠状动脉疾病家族聚集现象的阐明,为开发上调肝脏LDL受体的药物(如他汀类药物)奠定了基础。PCSK9罕见破坏性变异可降低LDL胆固醇水平并减少冠状动脉疾病风险的观察结果,促成了PCSK9抑制剂的研发。NPC1L1和ACLY变异与冠状动脉疾病相关的发现,进一步验证了通过药物抑制这些蛋白可降低LDL胆固醇水平和冠状动脉疾病事件风险的结论。
全基因组关联研究中首个被鉴定且关联性最强的冠状动脉疾病位点,包含载脂蛋白(a)由LPA基因编码的载脂蛋白(a)是一种高度可遗传的类LDL胆固醇大分子,也是潜在的新可改变的冠状动脉疾病风险因素。基于LPA基因变异与冠状动脉疾病相关的有力遗传学证据,目前正在开展针对其产物(载脂蛋白a)转录或功能阻断剂的心血管结局临床试验。其他正在研究的药物靶点还包括ANGPTL3、ANGPTL4和APOC3-遗传学研究表明,这些基因可升高甘油三酯水平并增加冠状动脉疾病风险。
部分影响一氧化氮信号通路的罕见和常见变异(如NOS3、GUCY1A1和PDE5),与冠状动脉疾病风险增加和血压升高相关。一项观察性研究显示,磷酸二酯酶5抑制剂治疗与冠状动脉疾病事件发生率降低相关,但后续试验数据仍缺乏。SVEP1基因的一个氨基酸替换变异可增强其功能,进而增加血管平滑肌细胞炎症和冠状动脉疾病风险。
此外,实验研究表明,使用抗体或疫苗阻断ADAMTS7具有治疗潜力。相关炎症分子的遗传分析已明确NLRP3炎症小体的潜在致病特征,后续临床试验也证实了这一点。SH2B3基因的一个常见氨基酸替换变异,可通过增加中性粒细胞胞外诱捕网和动脉血栓形成,升高冠状动脉疾病风险。全基因组关联研究信号还集中于细胞特异性信号通路,如影响内皮细胞抗动脉粥样硬化过程的CCM2和TLNRD1。
阐明冠状动脉疾病的遗传基础,有助于区分潜在的致病性生物标志物与混杂生物标志物。这种常被称为孟德尔随机化的方法,利用仅与目标暴露相关的遗传变异(称为工具变量);若暴露与疾病的关联具有因果关系,则遗传变异应在其影响暴露的范围内与疾病相关。该方法已用于验证冠状动脉疾病风险因素,如LDL胆固醇和甘油三酯水平升高、高血压、肥胖、脂蛋白(a)水平升高和2型糖尿病。如前所述,多种针对这些风险因素的药物,其作用靶点基因均已通过全基因组关联研究证实与冠状动脉疾病显著相关,这进一步证实这些药物可作用于相关致病机制。这些研究还帮助排除了部分风险标志物的致病性,如高密度脂蛋白胆固醇水平降低、维生素D水平降低、C反应蛋白水平升高和尿酸水平升高。尽管这些生物标志物与冠状动脉疾病存在强烈的流行病学相关性,但调节其血浆水平的遗传变异与冠状动脉疾病风险并无令人信服的关联。
在随机试验难以开展的情况下,孟德尔随机化研究也为理解冠状动脉疾病风险提供了宝贵证据。例如,随机化研究表明,身高较矮与冠状动脉疾病风险升高存在因果关系,而习惯性饮酒可能增加冠状动脉疾病风险。
结论
全球范围内更大规模的全基因组关联研究和测序研究,将提供关于相关DNA变异、致病基因和下游机制的更精确信息,也将有助于进一步优化和标准化冠状动脉疾病多基因风险评分。自2007年以来,全基因组扫描产生的大量遗传发现,持续改变着人们对冠状动脉疾病发病机制的认知。每个人都携带数百种影响多种疾病机制的常见遗传变异,携带数量越多,冠状动脉疾病风险越高。多项已确立的治疗方法已通过这些数据得到验证,目前正对多个基因驱动的疾病通路进行治疗潜力研究。冠状动脉疾病的全部遗传信息(包括家族性高胆固醇血症变异或整合的多基因风险评分),正持续为早期风险预测、预防和治疗开辟新的机会。
要点
全球范围内更大规模的全基因组关联研究和测序研究,将提供关于相关DNA变异、致病基因和下游机制的更精确信息,也将有助于进一步优化和标准化冠状动脉疾病多基因风险评分。自2007年以来,全基因组扫描产生的大量遗传发现,持续改变着人们对冠状动脉疾病发病机制的认知。每个人都携带数百种影响多种疾病机制的常见遗传变异,携带数量越多,冠状动脉疾病风险越高。多项已确立的治疗方法已通过这些数据得到验证,目前正对多个基因驱动的疾病通路进行治疗潜力研究。冠状动脉疾病的全部遗传信息(包括家族性高胆固醇血症变异或整合的多基因风险评分),正持续为早期风险预测、预防和治疗开辟新的机会。
要点
1
冠状动脉疾病的遗传基础
罕见的功能丧失变体具有较大的影响,直接涉及特定基因作为治疗靶点,这为药物开发提供了强有力的人类遗传学验证。
全基因组关联研究表明,常见的遗传变异占冠状动脉疾病遗传风险的很大比例。
与冠状动脉疾病风险相关的变异表现出对器官和组织的影响。其中许多变异通过已知的冠状动脉疾病发展的核心途径介导风险,但目前仍不清楚几种变异的潜在机制。
遗传关联数据通过孟德尔随机化进行因果推断研究,这为区分冠状动脉疾病的因果风险因素和相关风险标志物提供了一个框架。
多基因风险评分将常见变异的累积效应整合到遗传性冠状动脉疾病风险的单一指标中,具有连续的人群分布和显著的上限事件富集。
多基因风险评分提供的信息在很大程度上独立于传统的临床风险因素,包括家族史,并细化了事件和复发性冠状动脉疾病的风险分层。
虽然遗传风险等位基因在受孕时是固定的,但其临床后果是可以改变的,有证据表明生活方式干预和降脂治疗可以降低多基因风险评分高的人的风险,特别是在早期应用时。
关于冠状动脉疾病多基因风险评分的临床应用尚未达成共识,关于人群的稳健性,增量价值,成本效益和实施的问题仍然存在。
相关阅读:
晓芯甘—心脑血管健康评估:https://cvd.xin/
参考文献:
Schunkert H, Natarajan P, and Samani NJ.The inherited basis of coronary artery disease. N Engl J Med 2026;394:576-87.


