天生“护心符”:您拥有PCSK9的钻石变异吗?
- boke
- 2026-03-04
- 10:43 上午
有些人天生就拥有“护心符”,想知道您是不是其中之一吗?
引言:一个基因的传奇故事
在人类基因组中,有一个名为PCSK9的基因,它的故事堪称医学史上最精彩的发现之一。这个基因的某些“错误”版本,反而成为了保护心血管的“钻石”突变,让携带者终生受益。今天,就让我们一起走进PCSK9的奇妙世界。
一、PCSK9:从基因发现到重磅药物
1
PCSK9 的生物学角色
PCSK9(前蛋白转化酶枯草溶菌素9)是调节胆固醇代谢的关键蛋白。它主要作用于肝细胞表面的低密度脂蛋白受体(LDLR),促使这些受体降解。简单来说,PCSK9就像一个“破坏者”,拥有抵抗肝脏清除血液中“坏胆固醇”(LDL-C)的能力 [1]。
2
关键的遗传学发现
2003年,科学家首次发现PCSK9基因的功能获得型突变会导致家族性高胆固醇血症——一种让LDL-C极度升高的遗传病。但真正改变医学历史的,是随后在2005年的一项重要发现。
在一项里程碑式的研究中,Cohen等人在非洲裔美国人中发现了两个PCSK9 无义突变,这些突变携带者的LDL-C水平极低,而且冠心病风险惊人地降低了88% [2]。这一发现揭示了一个革命性的理念:天生低LDL-C的人,心血管系统仿佛被施了保护魔法。
3
从基因到药物:转化医学的典范
这个遗传学发现迅速转化为药物研发的巨大动力。科学家们意识到,如果能用药物模拟这些“钻石”突变的效果,就能为无数心血管疾病患者带来福音。
2015年,首批PCSK9抑制剂(单克隆抗体)获批上市,它们通过阻断PCSK9的功能,使肝脏LDL受体得以保留,从而大幅降低血液中的LDL-C水平 [3]。更令人振奋的是,近年来开发的siRNA疗法(如Inclisiran)只需每半年给药一次,就能使LDL-C降低45-60%,被誉为心血管治疗的革命性突破 [4]。
二、欧美人群中的PCSK9 降脂变异
1
常见的功能丧失型变异
在欧美人群中,PCSK9功能丧失型变异的分布呈现明显的种族差异:
欧洲裔白人中最著名的变异是R46L(p.Arg46Leu)。一项纳入31,469名白人的研究发现,约3.1%的人群携带这一变异,携带者的LDL-C平均降低13 mg/dL(约0.34 mmol/L),冠心病风险降低18%(虽然未达统计学显著性)[5]。
2
非洲裔人群的强效变异
相比之下,非洲裔人群携带的PCSK9 变异效果更为惊人。在17,459名非洲裔美国人中,约2.1%的人群携带Y142X或C679X无义突变 [6]。这些变异的效应极其显著:
LDL-C平均降低36 mg/dL(约0.93 mmol/L)
冠心病风险降低49%(OR=0.51,统计学显著)
这一发现完美诠释了“终生低LDL-C带来极大心血管获益”的核心理念。正如Grejtakova等人在综述中指出的,PCSK9 功能丧失型突变携带者的LDL-C降幅可达28%,同时伴随88%的冠心病风险降低 [1]。
三、中国人群中的PCSK9降脂变异
1
中国人群的独特遗传背景
百里挑一
中国人群的遗传背景与欧美人群存在显著差异。2024年发表的一项基于中国慢性病前瞻性研究(China Kadoorie Biobank)的大规模研究,对超过10万名中国成年人进行了基因分析。研究发现,一个位于PCSK9 基因的功能丧失型变异与LDL-C水平显著相关 [7]。
这个变异就是rs151193009(c.277C>T, p.Arg93Cys)。该变异在东亚人群中的携带率约为1.3-2.8%,是中国人群中最主要的PCSK9 降脂变异之一 [8]。
该研究还通过构建PCSK9 遗传评分(PCSK9-GS)发现,携带LDL-C降低变异的中国人群:
颈动脉斑块风险降低39%(OR=0.61)
主要闭塞性血管事件风险降低20%(OR=0.80)
缺血性卒中风险降低20%(OR=0.80)
值得注意的是,Tang等(2015)的研究单独分析了rs151193009(p.Arg93Cys)的降脂效应,发现该变异可使LDL-C降低约0.64 mmol/L(Beta = -0.64,P = 7.9×10⁻³²)[15]。进一步证实了p.Arg93Cys作为中国人群主要降脂变异的重要地位。
2
中国人群中的强效降脂变异
除了p.Arg93Cys外,中国人群中还发现了多个功能或流行病学研究表明的强效降脂位点:
千里挑一
p.Cys378Trp是一个机制明确的强效降脂变异。该变异在中国台湾地区人群中的携带率约为0.12%,携带者PCSK9水平降低56.4%,LDL-C降低30.5% (降至2.1 mmol/L) [9]。功能研究证实,该变异损害PCSK9蛋白的成熟和分泌过程,导致循环PCSK9水平显著降低,从而带来强大的降脂效应 [10]。
万里挑一
p.Glu144Lys则是在新疆维吾尔族人群中首次报道的功能丧失型变异 [10]。功能实验证实,该变异损害PCSK9蛋白的成熟过程,导致其无法正常分泌。表达E144K突变体的小鼠表现出血清PCSK9分泌受阻、肝脏LDL受体水平升高,以及血清LDL-C降低 [10]。
这些变异的发现,揭示了中国人群PCSK9 降脂变异的多样性和独特性,也为精准医学指导下的血脂管理提供了重要依据。
四、这些“钻石”突变的临床意义
1
自然界的“基因编辑”
PCSK9 功能丧失型变异堪称大自然馈赠的“基因编辑”范例。携带这些变异的人群终生享有低LDL-C的益处,而且无需服用任何降脂药物。这种自然保护机制为药物研发提供了完美的蓝图。
2
需要关注的其他影响
尽管PCSK9 功能丧失型变异本身通常被认为是良性的,但科学家们仍在持续关注极低LDL-C水平可能带来的其他影响。
来自中国人群的重要发现
基于中国慢性病前瞻性研究的最新数据显示,PCSK9遗传评分的LDL-C降低效应与某些呼吸系统疾病的风险存在关联 [7]:
慢性阻塞性肺病住院风险增加38%
急性上呼吸道感染风险增加118%
自报哮喘风险增加17%
这些发现提示,临床医生在使用PCSK9抑制剂时,可能需要关注患者的呼吸系统状况。
脂溶性维生素的相关顾虑
另一个长期关注的问题是:极低的LDL-C水平是否会影响脂溶性维生素(维生素A、D、E、K)的转运?这些维生素在血液中主要通过脂蛋白(尤其是LDL)运输。
来自PCSK9抑制剂药物研究的数据提供了令人安心的答案。一项针对evolocumab的52周临床研究专门分析了其对维生素E水平的影响。结果显示,尽管evolocumab使LDL-C降低了57%,但红细胞膜中的维生素E水平未见改变——而红细胞膜中的维生素E水平是组织水平的一个可靠替代指标 [11]。即使在LDL-C降至25 mg/dL(约0.65 mmol/L)以下的患者中,结果也未见差异。
一篇发表于《Safety of PCSK9 inhibitors》的综述也明确指出:PCSK9抑制剂不影响组织维生素E水平或类固醇激素合成 [12]。另一篇综述同样强调,大量研究检验了PCSK9抑制剂长期给药对维生素E和其他脂溶性维生素水平的影响,结果令人鼓舞 [13]。
需要强调的是,某些由APOB 基因突变引起的遗传性低脂蛋白血症(如无β脂蛋白血症)确实可导致严重的维生素E缺乏,表现为视网膜变性、周围神经病变、共济失调等严重症状,需要大剂量维生素E治疗。但这些疾病是由于载脂蛋白B本身缺陷导致LDL颗粒几乎完全缺失,与PCSK9 功能丧失型变异的机制完全不同。
PCSK9功能丧失与糖尿病风险的关联
除了呼吸系统疾病外,PCSK9 功能丧失与糖代谢的关系也备受关注。2024年发表的一项纳入744,466人的大型荟萃分析显示,PCSK9经典功能丧失型变异R46L(p.Arg46Leu)携带者的糖尿病风险较非携带者轻微增加9%(OR=1.09,95%CI 1.04-1.14,P<0.01)[16]。值得注意的是,Meta回归分析表明,这种糖尿病风险的升高与LDL-C的降低程度呈显著正相关(P=0.004),提示该效应可能主要由极低的LDL-C水平本身所介导,而非PCSK9变异的脱靶效应 。
来自中国新疆维吾尔族人群的遗传学研究也为这一关联提供了独立证据。Zhao等(2022)发现,PCSK9 基因rs2483205和rs2495477的多态性与2型糖尿病风险显著相关(OR=1.30-1.32),其中rs2495477正是PCSK9遗传评分(PCSK9-GS)的组成位点之一 [7、17]。
需要强调的是,PCSK9 功能丧失的心血管保护效应(冠心病风险降低17-50%)远超其带来的糖尿病风险(增加约9%),临床净获益明确。对于因PCSK9功能丧失变异而享有终生低LDL-C的个体,无需为此过度担忧,但保持健康的生活方式和定期体检依然是必要的。
3
药物研发的启示
从遗传学到药物的转化,PCSK9的故事已成为精准医学的典范。正如Perera在《Nature Reviews Genetics》中指出的:“基于PCSK9基因发现开发的单克隆抗体,为那些对他汀类药物耐受的患者带来了显著的LDL-C降低效果。这是人类基因组研究在现代医学中价值的胜利巡游。” [14]
结语:您想知道自己是否携带“钻石”突变吗?
PCSK9的遗传发现告诉我们一个简单而深刻的道理:有时候,上天赐予的“缺陷”,反而可能是最珍贵的礼物。那些天生携带PCSK9功能丧失型变异的人,就像是得到了一张心血管系统的“终身VIP卡”。
目前,通过基因检测可以很好地发现是否携带这些保护性变异。虽然大规模人群筛查尚未普及,但随着测序成本的下降和精准医学的发展,未来每个人或许都能了解自己的“基因护心符”。
如果您有早发冠心病家族史,或者对常规降脂治疗效果不佳,不妨咨询医生是否需要进行PCSK9等相关基因的检测。毕竟,了解自己的遗传密码,就是掌握健康的第一步。
精准筛查
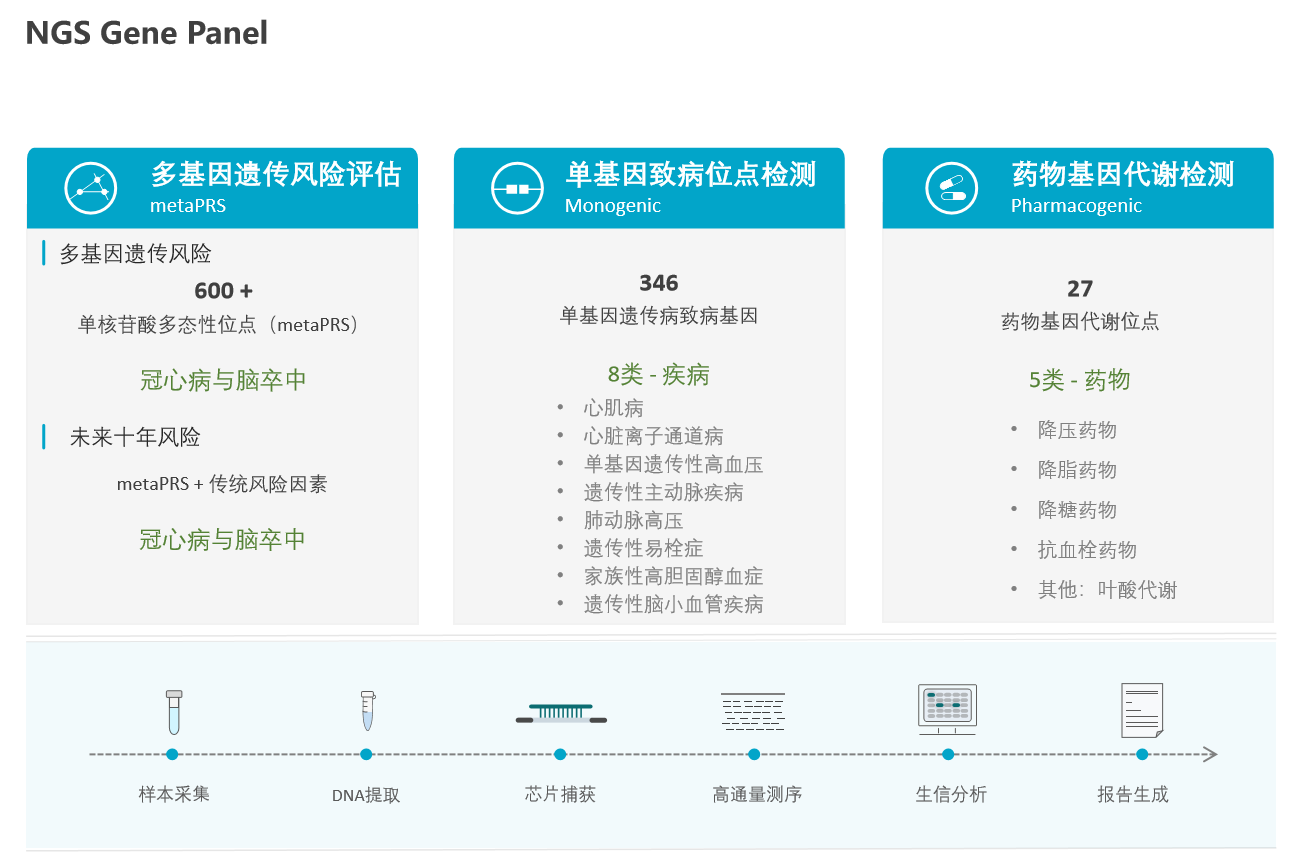
伯科生物开发的心脑血管健康评估芯片( 晓芯甘TM),涵盖了528个基因,661个单核苷酸多态性位点,27个药物基因代谢位点;其中多基因风险评估检测包括冠心病与脑卒中,单基因检测涵盖8大类心血管疾病,如心肌病、心脏离子通道病(包括QT综合征)、单基因遗传性高血压、遗传性主动脉疾病、肺动脉高压、遗传性易栓症、家族性高胆固醇血症、遗传性脑小血管疾病。
晓芯甘TM检测以多基因遗传风险为基础,加上单基因致病位点的检测,可以全面评估心脑血管疾病的遗传风险(Genetic Risk),实现精准筛查;利用多遗传因素风险和临床风险的综合模型能够更加精细化的进行风险分层;结合药物基因代谢的检测,针对高风险人群进行个性化干预以及有效治疗。
晓芯甘TM检测应用的研发与转化是基于过去二十年顾东风院士带领的国家心血管病中心研究团队的中国人群大队列基因组学研究,近十多年研究团队协调组织了中国、新加坡、马来西亚、日本、菲律宾等东亚人群以及欧美人群,涉及到全球近100余个队列,开展了50万人群心脑血管疾病基因组学研究,系统地解码了影响中国人群冠心病、脑卒中以及血脂异常、高血压等主要危险因素的遗传信息,相关研究成果发表在Nature Genetics、European Heart Journal等世界顶尖的学术期刊。
检测方法
一、检测方法:采用靶向基因高通量测序技术(Gene Panel/基因芯片)。
二、检测内容:
(1)PRS,600多个SNP单核苷酸多态性位点;
(2)单基因致病变异检测,包括八大类的单基因遗传性心血管病致病基因;
(3)药物基因组涵盖降血压、降脂等药物代谢多态性位点近30个。
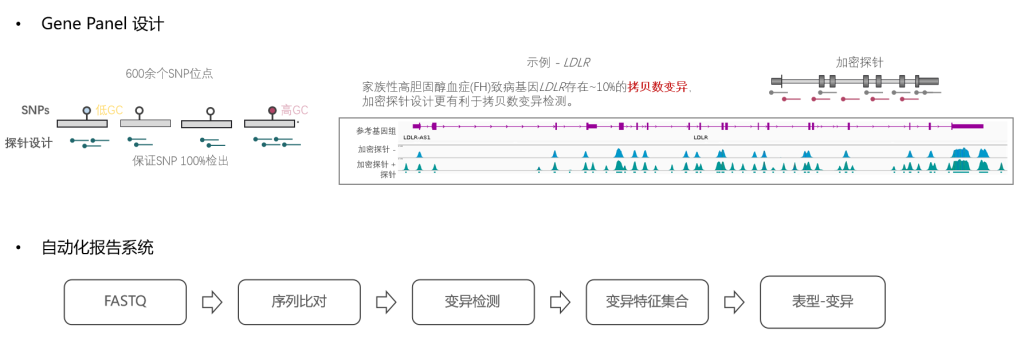
三、Gene Panel设计:对于不同基因变异类型采取针对性的探针设计策略。PRS模块采用多重叠瓦设计,保证覆盖深度均一性,单基因覆盖UTR与外显子,特殊变异类型也进行相应设计,例如具有VNTR的LPA基因以及含有深度内含子变异的MYBPC3采用全基因覆盖、具有CNV变异的LDLR基因对内含子部分进行加密设计。
参考文献:
GBD 2019 Diseases and Injuries Collaborators. Global burden of 369 diseases and injuries in 204 countries and territories, 1990-2019: a systematic analysis for the Global Burden of Disease Study 2019 [published correction appears in Lancet. 2020 Nov 14;396(10262):1562.
The Lancet Commission on rethinking coronary artery disease: moving from ischaemia to atheroma. DOI: 10.1016/S0140-6736(25)00055-8
Cloud G C, Williamson J D, Thao L T P, et al. Low-dose aspirin and the risk of stroke and intracerebral bleeding in healthy older people: Secondary analysis of a randomized clinical trial[J]. JAMA Netw Open,2023, 6(7): 571-580.
Liu C F, Rokavec M, Huang Z K,et al. Salicylate induces AMPK and inhibits c-MYC to activate a NRF2/ARE/miR-34a/b/c cascade resulting in suppression of colorectal cancer metastasis[J]. Cell Death Disease, 2023, 14(10): 707-716.
Ana Laura S A M , Ashley J O, Emil Jakobsen , Diego I G,et al. Salicylate-elicited activation of amp-activated protein kinase directly triggers degradation of c-myc in colorectal cancer cells[J]. Cells,2025,14(4):294-302.
Lee T Y, Hsu Y C, Tseng H C,et al. Daily aspirin associated with a reduced risk of hepatocellular carcinoma in patients with non-alcoholic fatty liver disease: A population-based cohort study[J]. eClin Med, 2023,61(6):323-331.
Gaziano JM, Brotons C, et al. Use of aspirin to reduce risk of initial vascular events in patients at moderate risk of cardiovascular disease (ARRIVE): a randomised, double-blind, placebo-controlled trial. Lancet. 2018 Sep 22;392(10152):1036-1046.
ASCEND Study Collaborative Group;et al. Effects of Aspirin for Primary Prevention in Persons with Diabetes Mellitus. N Engl J Med. 2018 Oct 18;379(16):1529-1539.
McNeil JJ, Nelson MR, Woods RL, Lockery JE, Wolfe R, Reid CM, et al. Effect of Aspirin on All-Cause Mortality in the Healthy Elderly. N Engl J Med. 2018;379(16):1519-1528
Zoungas S, Zhou Z, Owen AJ, Curtis AJ, Espinoza SE, Ernst ME, et al. Daily low-dose aspirin and incident type 2 diabetes in community-dwelling healthy older adults: a post-hoc analysis of efficacy and safety in the ASPREE randomised placebo-controlled trial. Lancet Diabetes Endocrinol. 2024;12(2):98-106
Wolfe R, Broder JC, Zhou Z, Murray AM, Ryan J, Chan AT, et al. Aspirin, cardiovascular events, and major bleeding in older adults: extended follow-up of the ASPREE trial. Eur Heart J. 2025;46(42):4410-4422
Zhou Z, Webb KL, Nelson MR, Woods RL, Ernst ME, Murray AM, et al. Short- and long-term impact of aspirin cessation in older adults: a target trial emulation. BMC Med. 2024;22(1):306
Li CX, Sun LC,et al. The associations of candidate gene polymorphisms with aspirin resistance in patients with ischemic disease: a meta-analysis. Hum Genomics. 2024 Dec 2;18(1):135.
Shorbaji A, Pushparaj PN, et al. A narrative review of research advancements in pharmacogenetics of cardiovascular disease and impact on clinical implications. NPJ Genom Med. 2025 Jul 10;10(1):54. .
Wang Y, Zhao X, et al. Association Between CYP2C19 Loss-of-Function Allele Status and Efficacy of Clopidogrel for Risk Reduction Among Patients With Minor Stroke or Transient Ischemic Attack. JAMA. 2016 Jul 5;316(1):70-8.
Pan Y, Chen W, et al. Association Between ABCB1 Polymorphisms and Outcomes of Clopidogrel Treatment in Patients With Minor Stroke or Transient Ischemic Attack: Secondary Analysis of a Randomized Clinical Trial. JAMA Neurol. 2019 May 1;76(5):552-560.参考文献:
1. Grejtakova D, Boronova I, Bernasovska J, Bellosta S. PCSK9 and Lipid Metabolism: Genetic Variants, Current Therapies, and Cardiovascular Outcomes. Cardiovasc Drugs Ther. 2024;39(6):1439-1451. doi:10.1007/s10557-024-07599-5
2.Cohen JC, Boerwinkle E, Mosley TH Jr, Hobbs HH. Sequence variations in PCSK9, low LDL, and protection against coronary heart disease. N Engl J Med. 2006;354(12):1264-1272. doi:10.1056/NEJMoa054013
3.Schwartz GG, Steg PG, Szarek M, et al. Alirocumab and Cardiovascular Outcomes after Acute Coronary Syndrome. N Engl J Med. 2018;379(22):2097-2107. doi:10.1056/NEJMoa1801174
4.Wright RS, Ray KK, Raal FJ, et al. Pooled Patient-Level Analysis of Inclisiran Trials in Patients With Familial Hypercholesterolemia or Atherosclerotic Cardiovascular Disease. J Am Coll Cardiol. 2021;77(9):1182-1193. doi:10.1016/j.jacc.2020.12.058
5.Benn M, Nordestgaard BG, Grande P, Schnohr P, Tybjaerg-Hansen A. PCSK9 R46L, low-density lipoprotein cholesterol levels, and risk of ischemic heart disease: 3 independent studies and meta-analyses. J Am Coll Cardiol. 2010;55(25):2833-2842. doi:10.1016/j.jacc.2010.02.044
6.Mefford MT, Marcovina SM, Bittner V, et al. PCSK9 loss-of-function variants and Lp(a) phenotypes among black US adults. J Lipid Res. 2019;60(11):1946-1952. doi:10.1194/jlr.P119000173
7.Holmes MV, Kartsonaki C, Boxall R, et al. PCSK9 genetic variants and risk of vascular and non-vascular diseases in Chinese and UK populations. Eur J Prev Cardiol. 2024;31(1):e9-e11. doi:10.1093/eurjpc/zwae009
8.Yang L, Pu T, Zhang Y, et al. The R93C Variant of PCSK9 Reduces the Risk of Premature MI in a Chinese Han Population. Front Genet. 2022;13:903579. doi:10.3389/fgene.2022.903579
9.Wu, Semon et al. “Effects of the PCSK9 C378W Mutation on PCSK9 Levels and Lipid Profiles in Taiwanese Individuals: A Loss-of-Function Mutation with Potential Cardiovascular Benefits.” Genes vol. 16,9 1113. 19 Sep. 2025, doi:10.3390/genes16091113
10.Meng FH, Liu S, Xiao J, et al. New Loss-of-Function Mutations in PCSK9 Reduce Plasma LDL Cholesterol. Arterioscler Thromb Vasc Biol. 2023;43(7):1219-1233. doi:10.1161/ATVBAHA.122.318839
11.Blom D, Monsalvo ML, Tsirtsonis K, et al. Effects of Evolocumab (AMG 145) Treatment on Vitamin E Levels: Results from the 52-Week Phase 3 Double-Blind, Randomized, Placebo-Controlled DESCARTES Study. J Am Coll Cardiol. 2015;65(10_Supplement):A1367. doi:10.1016/S0735-1097(15)61367-5
12.Safety of PCSK9 inhibitors. Biomed Pharmacother. 2022;156:113908. doi:10.1016/j.biopha.2022.113908
13.Kosmas CE, Skavdis A, Sourlas A, et al. Safety and Tolerability of PCSK9 Inhibitors: Current Insights. Clin Pharmacol. 2020;12:191-202. doi:10.2147/CPAA.S288831
14.Perera M. From genome to drug: the hidden story of diversity. Nat Rev Genet. 2025;26:296. doi:10.1038/s41576-025-00833-2
15.Tang CS, Zhang H, Cheung CY, et al. Exome-wide association analysis reveals novel coding sequence variants associated with lipid traits in Chinese. Nat Commun. 2015;6:10206. doi:10.1038/ncomms10206
16.Liu S, Wan J, Wang D, et al. Effect of the PCSK9 R46L genetic variant on plasma insulin and glucose levels, risk of diabetes mellitus and cardiovascular disease: A meta-analysis. Nutr Metab Cardiovasc Dis. 2024;34(6):1339-1351. doi:10.1016/j.numecd.2024.04.007
17.Zhao F, Wang Y, Liu R, et al. Association of genetic polymorphisms of PCSK9 with type 2 diabetes in Uygur Chinese population. BMC Cardiovasc Disord. 2022;22(1):284. doi:10.1186/s12872-022-02710-w


