反义寡核苷酸疗法对18%的神经发育障碍患者具有治疗潜力
- boke
- 2025-08-05
- 9:58 上午

神经发育障碍(Neurodevelopmental disorders,NDDs)
NDDs是一组难以治疗的疾病,许多NDDs在发育早期就表现出来,但NDDs相关的临床特征尚未阐明,如大脑结构异常,在症状出现后儿童和成人能否逆转等。
反义寡核苷酸疗法(AON/ASO)
在过去的十年中,基于反义寡核苷酸(AntiSense OligoNucleotide,AON/ASO)的治疗方法已经出现,也成为NDDs的有希望的治疗方法。
AON/ASO药物-Milasen代表了个性化医学的一个重大里程碑,用于治疗超罕见突变引起的巴顿氏病。Milasen也是第一种成功的个体化AON药物,它是只针对一个患者的致病变异设计AON药物,并以唯一服用的患者进行了命名。Milasen展示了AONs纠正剪接破坏变异的潜力,可能更广泛地应用于NDDs。目前,已经超过10种RNAi和ASO疗法获得了监管批准。
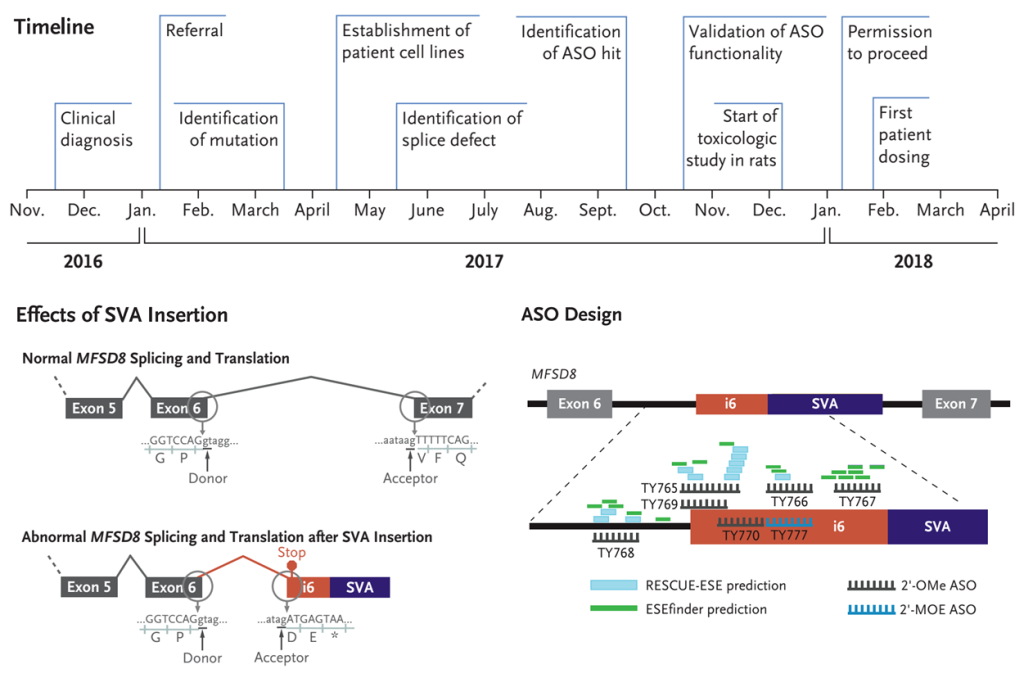
研究团队在1年内完成了致病变异发现(NGS测序),ASO/AON设计,细胞和动物实验筛选验证和第一剂用药;3个月后,患者症状明显改善。
AONs是短链寡核苷酸,能与(mRNA)结合,可用于影响剪接、稳定性和翻译过程。
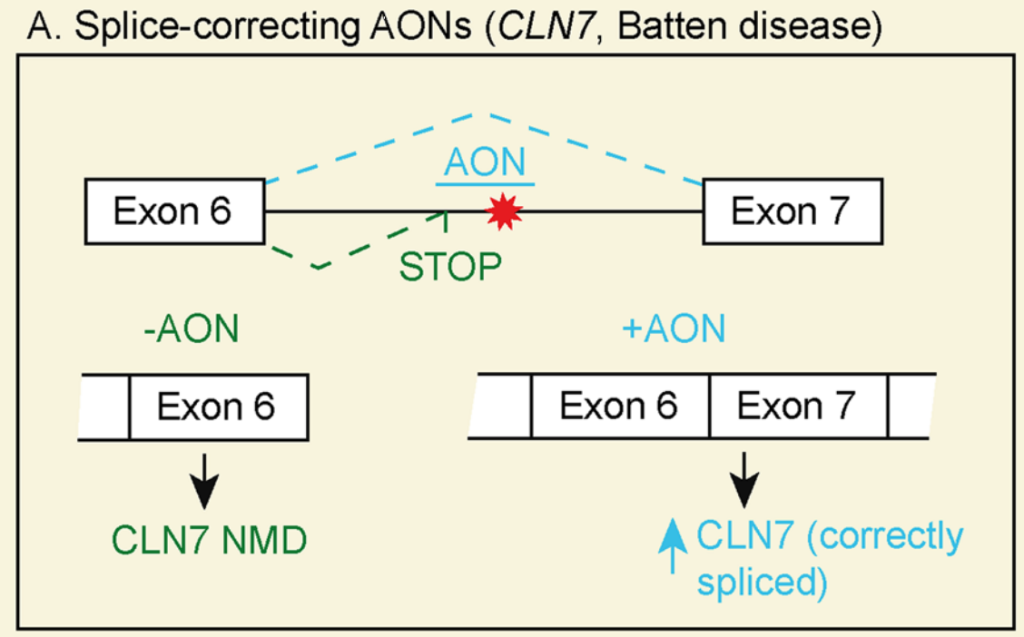
剪接转换AONs可以通过拯救剪接破坏的变异(图A)或外显子跳跃来防止无义介导的降解(Nonsense-Mediated Decay,NMD),通过跳跃包含截断变异的外显子来允许缩短转录本的表达(外显子跳跃用于变异排除)。
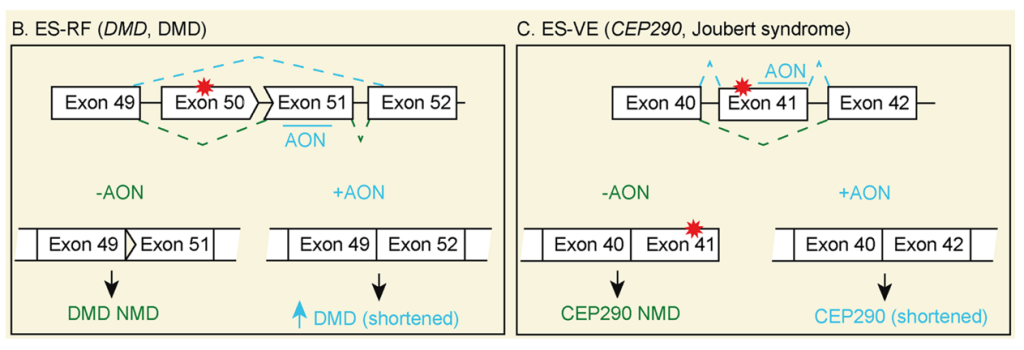
或通过跳跃移位外显子来恢复移位缺失的阅读框(外显子跳跃用于阅读框恢复)(图B,C)。
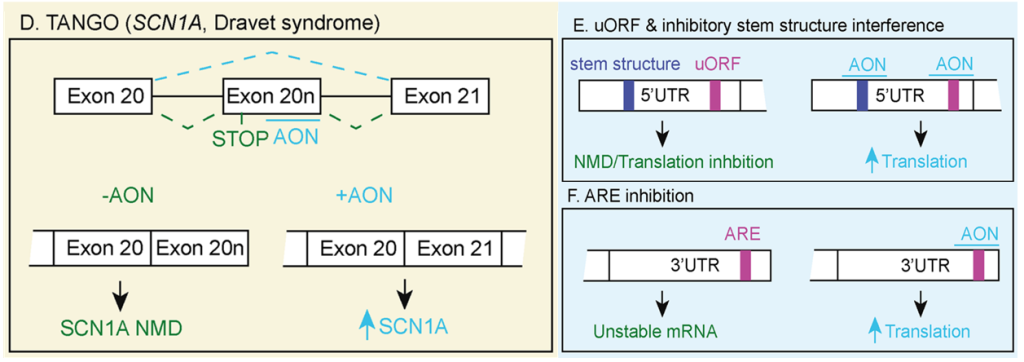
此外,空间阻碍AONs被用于提高由单倍体不足或印记引起的疾病中野生型等位基因的翻译效率。例如靶向NMD敏感事件来上调表达,或通过结合上游AUGs、5’UTR中的茎结构以及3’UTR中的AU丰富元件(AU-Rich Element,ARE)(图D-F)。
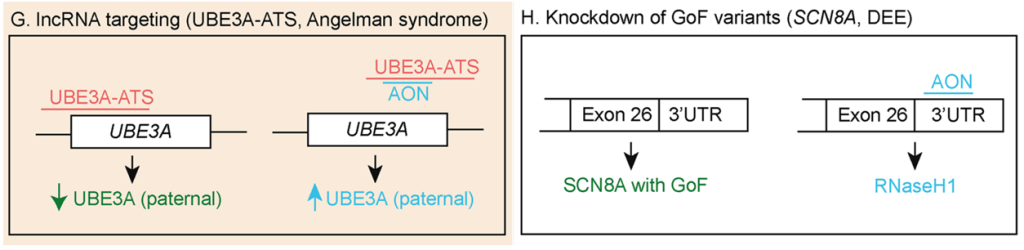
另一种提高野生型等位基因翻译效率的方法是通过RNAseH1激活AONs,促进调节因子的降解,例如作用于长链非编码RNA(IncRNA)(图G)。最后,RNAseH1激活的AONs还可以用于降解过表达、过于活跃或有毒的基因产物(图H)。
由于AONs通过互补碱基配对与细胞RNA结合,因此这是一种高度可编程的方法,可以针对通路、疾病或问题的根本原因进行靶向。此外,AONs的椎管内或脑室内给药允许靶向中枢神经系统,而不需要穿过血脑屏障。这些特性使AONs成为治疗神经功能障碍(包括NDDs)的有希望的疗法选择。
然而,AON疗法在NDDs中的适用性取决于遗传和表型特征。在本研究中,我们系统地评估了AON疗法在NDDs中的关键特征,以估计整体治疗潜力并确定那些可靶向的NDDs。
研究方法
创建并评估了一个NDD数据集,以识别7种AON策略可能可靶向的NDD。这包括检查包括疾病-基因特性(如调控元件、致病变异的影响)和疾病相关表型特征在内的关键因素组合的存在。如果一个变异具有可靶向的变异类型,并且注释到其上的疾病和基因包含对应AON策略的可靶向特性组合,则该变异被视为可靶向。
研究结果
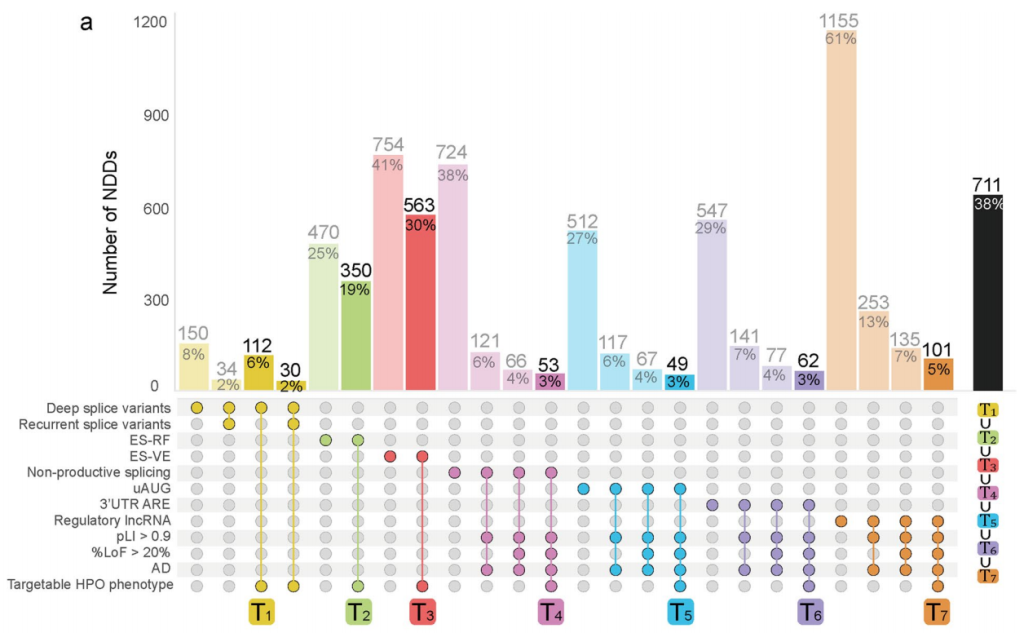
对1885种NDD及其致病基因的可靶向表型特征、预测的潜在变异后果和基因特性进行分析,用以评估AON疗法对NDDs的影响,并确定未来AON疗法的有希望候选者。我们发现基于AON的治疗策略可能适用于约18%的个体,涉及711种不同的NDD(占总数的38%),这表明AON疗法在NDDs中的应用潜力可能比迄今为止预期的更为广泛。
7种AON治疗策略:
T1:Splice-correction;
T2:Exon-skipping for reading frame restoration;
T3:Exon-skipping for variant exclusion;
T4:Targeting NMD-sensitive events(TANGO);
T5:uAUG targeting; T6:3’ ARE targeting;
T6:3’ ARE targeting;
T7:AON-mediated degradation of lncRNAs.
研究结论
我们分析的结果表明,AON疗法在NDDs中的应用潜力可能比迄今为止预期的更为广泛,同时强调了AON疗法作为NDDs的有希望的疗法选择,并有助于治疗选择的知情决策。
参考资料
1. Wijnant et al. Systematic analysis of genetic and phenotypic characteristics reveals antisense oligonucleotide therapy potential for one-third of neurodevelopmental disorders. Genome Medicine (2025) 17:59
2. Kim J, Hu C, Moufawad El Achkar C, Black LE, Douville J, Larson A, et al. Patient-customized oligonucleotide therapy for a rare genetic disease. N Engl J Med. 2019;381(17):1644–52.


