再谈基因检测在携带者筛查的意义与技术实施方案
- boke
- 2025-06-19
- 10:10 上午
新一代基因测序技术(NGS)已经在携带者筛查应用取得了非常大的进步,随着机器学习与人工智能技术在生物信息学分析的实施,将为人类疾病的精准筛查与诊治带来实质且有效的个性化解决方案。现在,基因检测用于携带者筛查的意义从卫生经济学角度获益将越来越高。
近期国际生殖遗传学会2025年会上,沈亦平教授阐释:
“综合性携带者筛查是阻断遗传病代际传递的第一道防线”;“携带者的定义对无明显症状的个体进行与某些遗传病相关基因的致病变异检测,每个人都可以做携带者筛查”。
如何设计更适用携带者筛查、更科学合理的Gene Panel?
两篇经典文献采用了类似的方法进行基因筛选。
一、《Nationwide, Couple-Based Geneti Carrier Screening》

覆盖至少1,277个基因,对应750余种严重遗传病(常染色体隐性或X连锁遗传病),包括致死性、致残性及儿童期发病疾病。
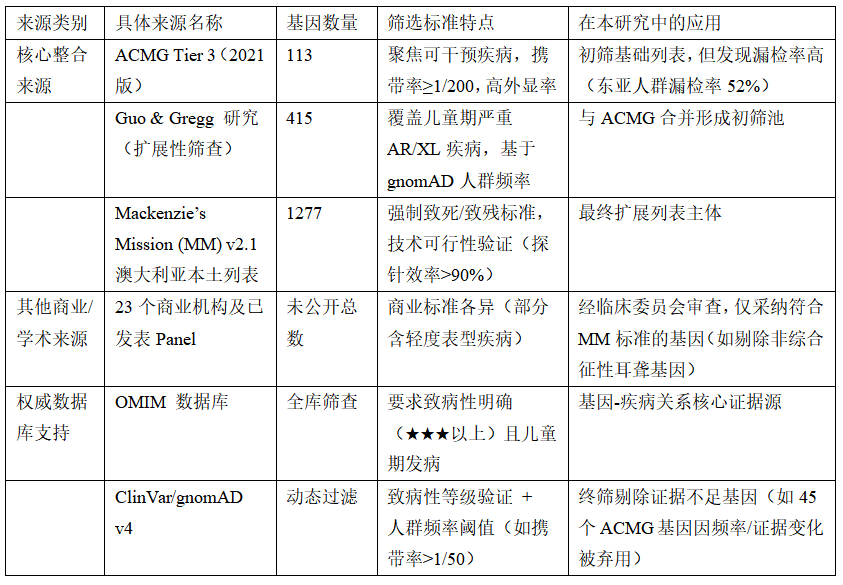
整合流程:
-
合并三大核心列表(113+415+1277)→ 初筛池共1350基因; -
去重+数据库验证 → 保留1310个基因(通过OMIM/gnomAD标准; -
技术可行性过滤 → 剔除31个低捕获效率基因 → 最终至少1277基因纳入MM Panel。
二、《Optimizing Gene Panels for Equiable Reproductive Carrier Screening: the “Goldilocks” Approach》

当前携带者筛查(如ACMG推荐的113基因Panel)存在显著公平性缺陷:
-
人群差异大:ACMG Tier 3 Panel在不同族裔中阳性率差异悬殊(48%–84%),东亚人群漏检率高达52%。
-
数据滞后性:ACMG原始列表基于旧版gnomAD数据,部分基因已不符合纳入标准(如致病性证据不足或人群频率变化)。
-
技术局限:固定基因数量难以平衡“覆盖全面性”与“成本效益”,亟需动态优化策略。
基因选择逻辑:三步构建Goldilocks Points模型
第一步:多源基因池整合(广度优先)
研究者合并三大权威来源:
-
ACMG Tier 3基因(113个) -
Guo & Gregg研究(415个) -
澳大利亚Mackenzie’s Mission项目(MM v2.1,1277个)
剔除重复项后形成 1350个候选基因,最终 1310个 通过gnomAD v4标准验证。
第二步:基于人群频率的动态建模(公平性导向)
-
利用 gnomAD v4.1.0(覆盖10个族裔群体,如非洲/东亚/中东等)和 ClinVar 数据库,计算每个基因在特定人群中的:
– 等位基因频率(AF)
– 夫妇携带风险概率
-
通过建模不同基因数量Panel的 阳性率(Positive Yield),发现关键规律:
基因数量 vs. 阳性率呈非线性增长,边际收益随基因数增加递减。
第三步:确定Goldilocks Points
基于临床决策需求,锁定四个关键阳性率阈值对应的最优基因数量:

避免过少(如ACMG 113基因):漏检率高(尤其非欧人群)❌。
避免过多(如>1000基因):边际收益骤降,成本效益低❌ 。
从定制化Panel到人全外显子Panel(WES),伯科可以为携带者筛查提供成熟的全国产化解决方案。Panel设计可全覆盖双文献(NEJM + Genetic in Medcine)中涉及的、更具价值的基因,可以根据临床需要快速添加新增基因,更新迭代。伯科的人全外显子Panel(WES)通过增强基因组hg19传统研究区域的覆盖,兼顾 hg19 & hg38 双版本基因组研究需求;同时,增加线粒体与高证据等级的非编码区致病和疑似致病位点模块;基于完整的基因组核心模块、单基因全覆盖等个性化定制模块,将为人类基因组全外显子的研究与转化,提供更加全面高效的解决方案。
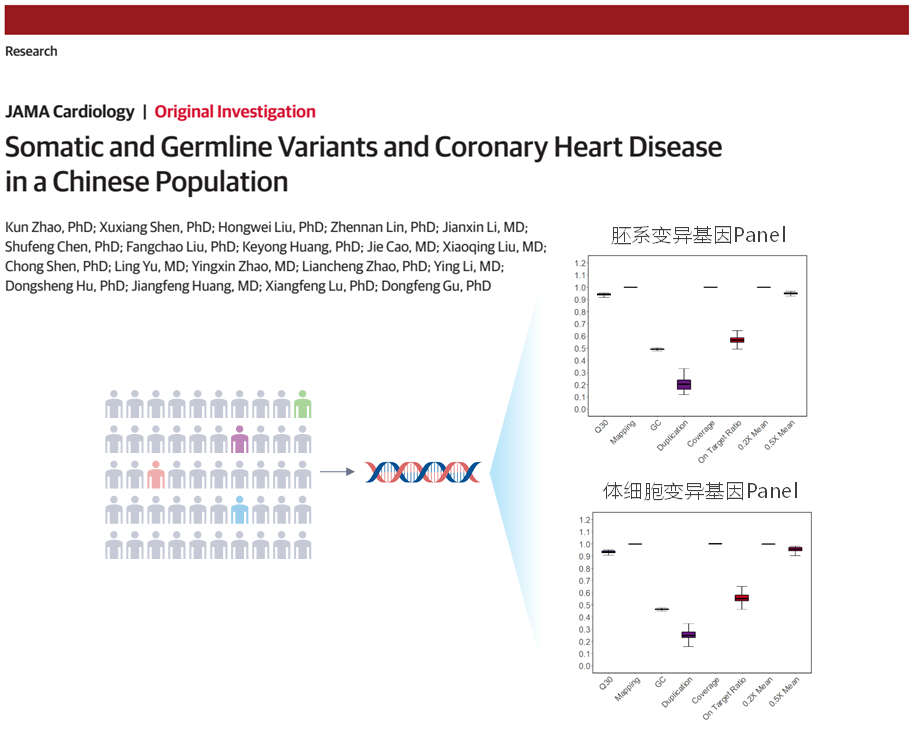
伯科胚系和体细胞变异检测提供的定制化Panel助力中国人群克隆性造血研究
参考资料
1. Kirk EP, Delatycki MB, Archibald AD, et al. Nationwide, Couple-Based Genetic Carrier Screening. N Engl J Med 2024;391:1877-1889
2. Optimizing Gene Panels for Equitable Reproductive Carrier Screening: the “Goldilocks” Approach. Genetics in Medicine. 2025
3. Zhao K, Shen X, Liu H, et al. Somatic and Germline Variants and Coronary Heart Disease in a Chinese Population[J]. JAMA cardiology, 2024.


