全长转录组图谱揭示ERBB2可变剪接介导的曲妥珠单抗耐药性
- boke
- 2025-12-19
- 5:45 下午
一、研究背景
胆囊癌(GBC)是消化系统常见恶性肿瘤,早期症状不明显,多数患者确诊时已失去手术机会,依赖化疗和靶向治疗。但由于对GBC的基础研究匮乏,导致有效的靶向治疗策略严重不足。研究表明ErbB通路突变是GBC的基因组特征性标志,能推动肿瘤生长、转移和免疫逃逸,因此ERBB2成为GBC最有前景的治疗靶点。靶向ERBB2的曲妥珠单抗,是FDA批准的首款用于癌症治疗的单克隆抗体,但耐药问题较为普遍。
除了基因组变异,RNA的选择性剪接已被证实在肿瘤发生、进展和耐药中发挥关键作用,可产生具有新功能的蛋白质异构体。构建全面的全长转录组图谱是研究肿瘤生物学中RNA改变的一种高效方法。主流短读长测序技术对于解析全长转录本的结构有一定的局限性,无法呈现完整转录本中各种异常的组合情况,这限制了人们对转录组复杂性的全面认识。而长读长测序技术能够直接获得完整、准确的全长转录本序列为系统发现和鉴定新的剪接异构体提供工具。
本研究旨在利用先进的长读长测序技术,构建胆囊癌的全长转录组图谱,揭示新的治疗靶点和耐药机制。
二、主要结论
该研究构建了GBC全长转录组图谱,揭示了丰富的全新转录本异构体与基因。鉴定出ERBB2新异构体ERBB2 i14e,该异构体在GBC中表达升高,与不良预后相关,并能通过激活增强与ERBB3的互作激活AKT信号通路促进肿瘤增殖。发现了曲妥珠单抗耐药性产生原因是由于ERBB2 i14e额外肽段造成的空间位阻效应,使药物无法与该ERBB2结合。提出了剪接因子ESRP1/2调控ERBB2 i14e的产生,使用ASOs靶向 ERBB2 i14e剪接过程可恢复曲妥珠单抗敏感性,为改善胆囊癌及可能的其他癌症的治疗带来了新的方案。
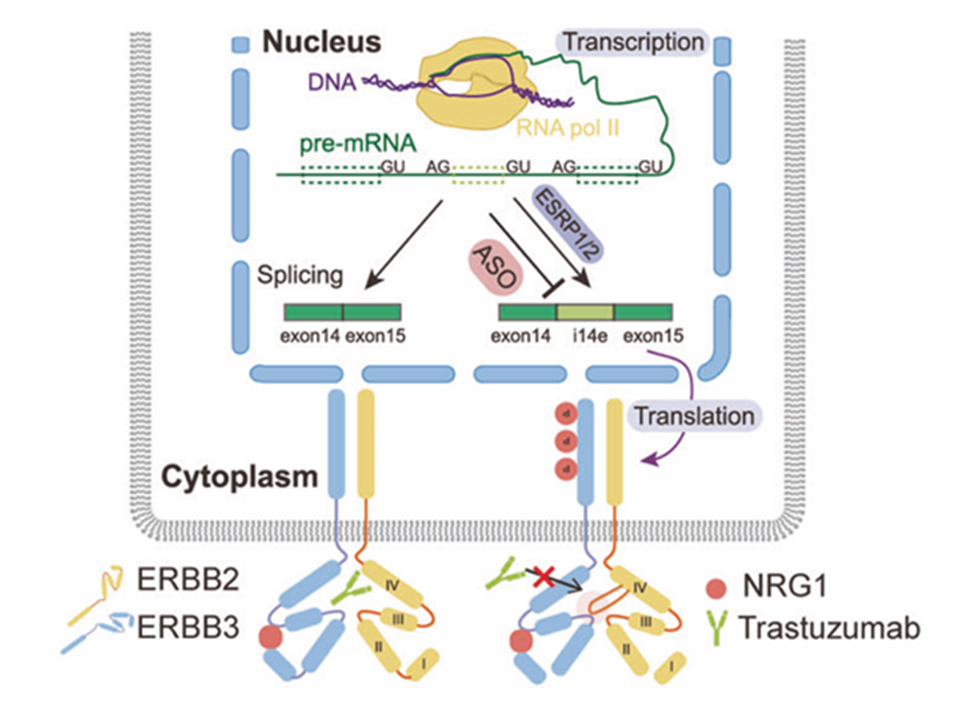
图1 ERBB2可变剪接介导的曲妥珠单抗耐药性及ASO靶向治疗示意图
三、详细结果
1.胆囊癌全长转录组图谱构建
对4例正常胆囊组织、8例GBC组织、4个GBC细胞系和1个永生化胆囊上皮细胞系进行PacBio长读长测序,整合了61,676个全长转录本异构体的注释与表达数据,构建了GBC转录组图谱。该研究还通过短读长测序验证了长读长测序结果,证实其成功构建了胆囊系统的高质量、全面的全长转录本表达数据集。图谱发现了大量新的转录本亚型,其中受体酪氨酸激酶(RTK)家族的转录本具有高度的多样性,尤其是ERBB2基因存在多种可变剪接形式。
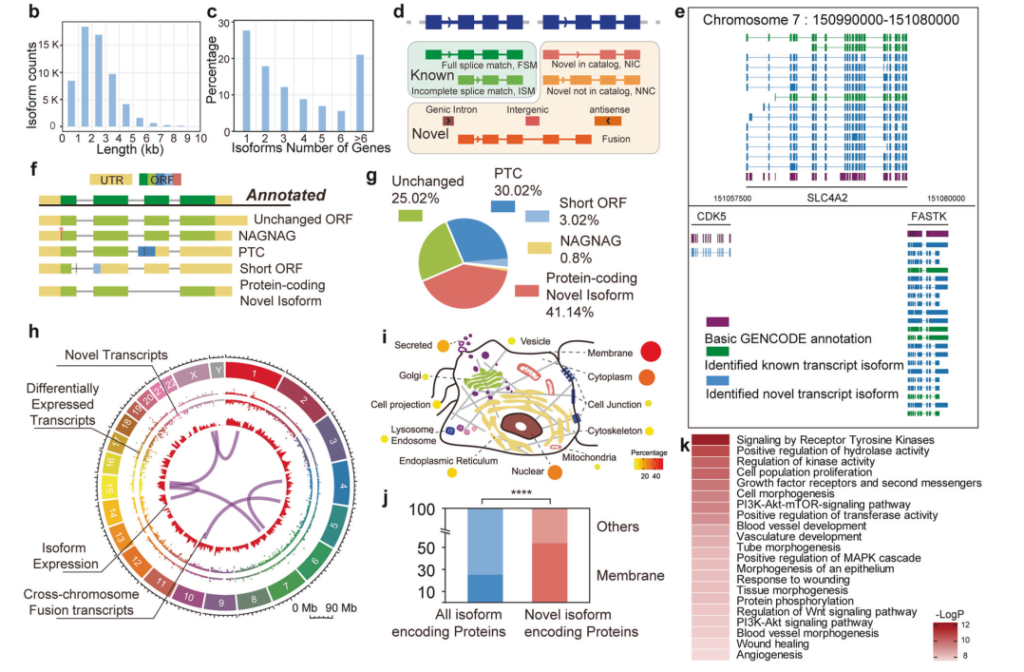
图2 胆囊癌全长转录组图谱构建
2. ERBB2 i14e的鉴定与功能确认
研究在约25.5%的胆囊癌样本中可检测到一个新的转录本—ERBB2 i14e(ERBB2 i14e在第14内含子中插入一个102 bp的新外显子,编码34个氨基酸的肽段,位于ERBB2胞外IV结构域)与患者总生存期缩短显著相关。
研究结果显示与ERBB3共表达且存在NRG1的情况下,过表达ERBB2 i14e能够激活AKT通路,促进细胞增殖和肿瘤生长。研究结果还显示与野生型ERBB2相比,ERBB2 i14e与ERBB3的相互作用更强。以上结果说明ERBB2 i14e具有更强的与ERBB3相互作用的能力,从而可能激活下游信号级联反应,促进GBC细胞增殖。
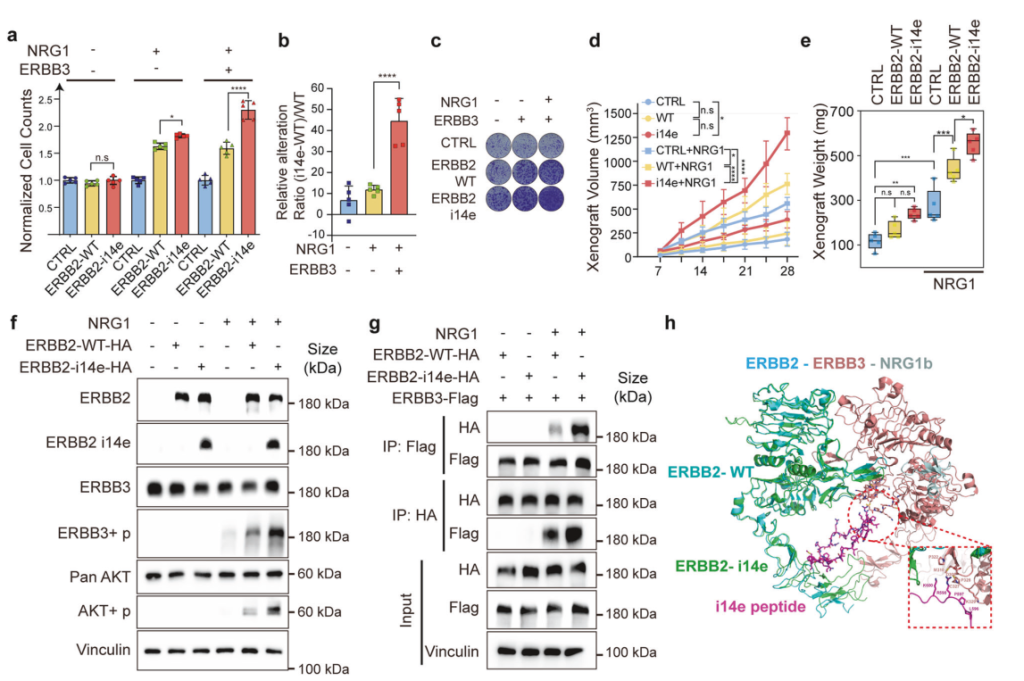
图3 ERBB 2 114 e促进细胞增殖并与ERBB 3相互作用
3. ERBB2 i14e介导的曲妥珠单抗耐药机制
体外细胞实验结果表明,与表达野生型ERBB2相比,表达ERBB2 i14e的细胞对曲妥珠单抗不敏感,且其AKT磷酸化不受抑制,体内异种移植模型也产生了相同的实验结果。
流式细胞术分析表明,相比野生型ERBB2,曲妥珠单抗与ERBB2 i14e的结合能力显著降低。蛋白质结构进一步分析发现ERBB2 i14e额外肽段在结构上阻碍曲妥珠单抗与ERBB2结合。表明ERBB2 i14e保护癌细胞免受曲妥珠单抗结合,从而产生对曲妥珠单抗治疗的耐药性。
在患者来源异种移植模型中,曲妥珠单抗处理后ERBB2 i14e表达上调,同时在乳腺癌与胃癌中有相同的结果。以上结果表明ERBB2 i14e在曲妥珠单抗适应过程中可被诱导表达,从而赋予肿瘤耐药性。
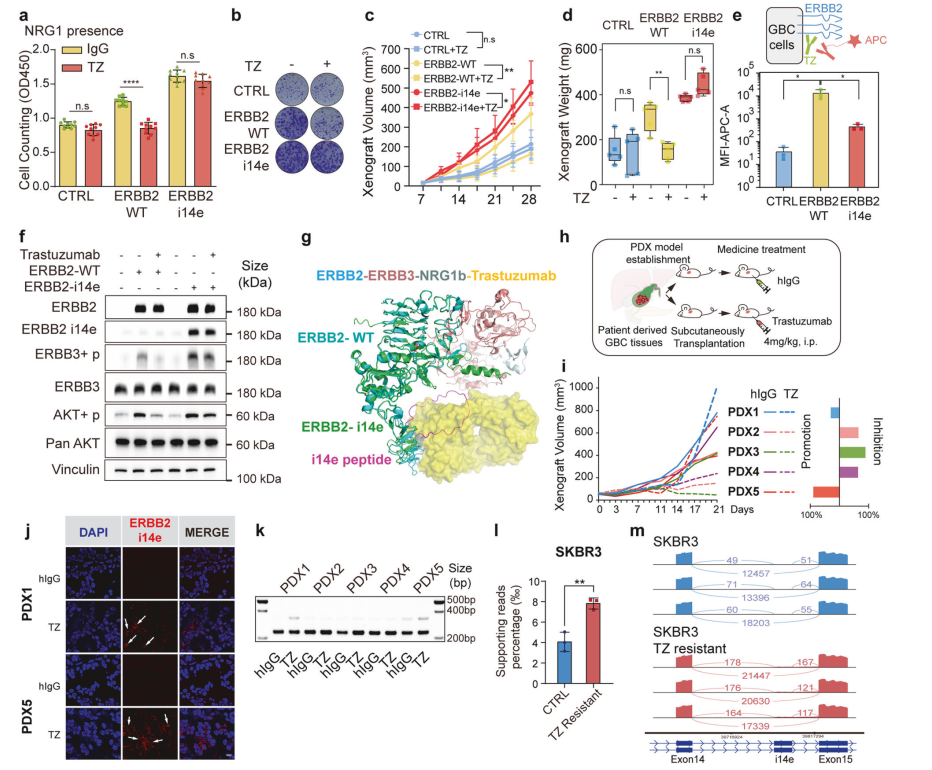
图4 表达ERBB 2 i14 e的细胞或肿瘤对曲妥珠单抗治疗耐药
4. 抑制ERBB2 i14e表达可增强曲妥珠单抗敏感性
利用GBC RNA数据集所获得的439个剪接因子进行差异基因表达分析,发现ESRP1/2可能是ERBB2 i14e剪接的潜在调节因子。同时,确定了 i14e 外显子附近的富含UGG的结构域对 ESRP1 结合至关重要。
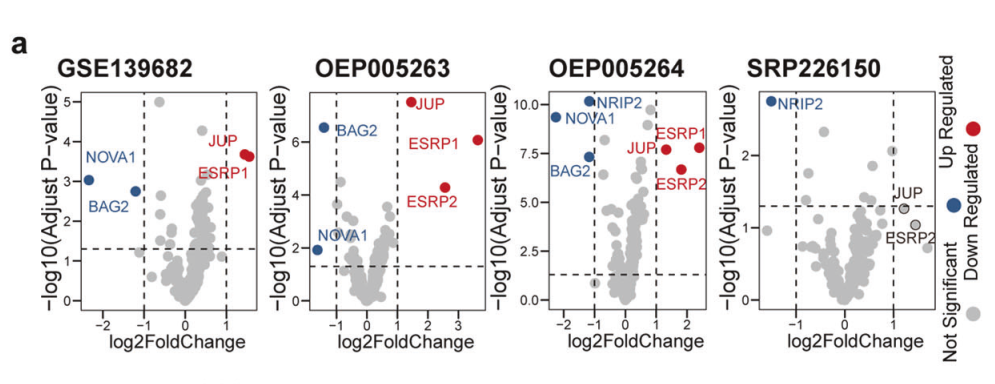
图5 四个独立GBC RNAseq数据库RNA剪接因子的差异表达分析
该研究还设计了靶向ERBB2 i14e不同剪接位点的反义寡核苷酸(ASO),靶向5’剪接位点的ASO1对ERBB2 i14e表达抑制效果最强。ASO联合曲妥珠单抗或其偶联药物T-DXd,在体外和体内模型中均能显著抑制肿瘤生长。表明ERBB2 i14e反义寡核苷酸与曲妥珠或曲妥珠-药物偶联物联合治疗,对表达ERBB2 i14e的癌症患者具有巨大的潜在益处。
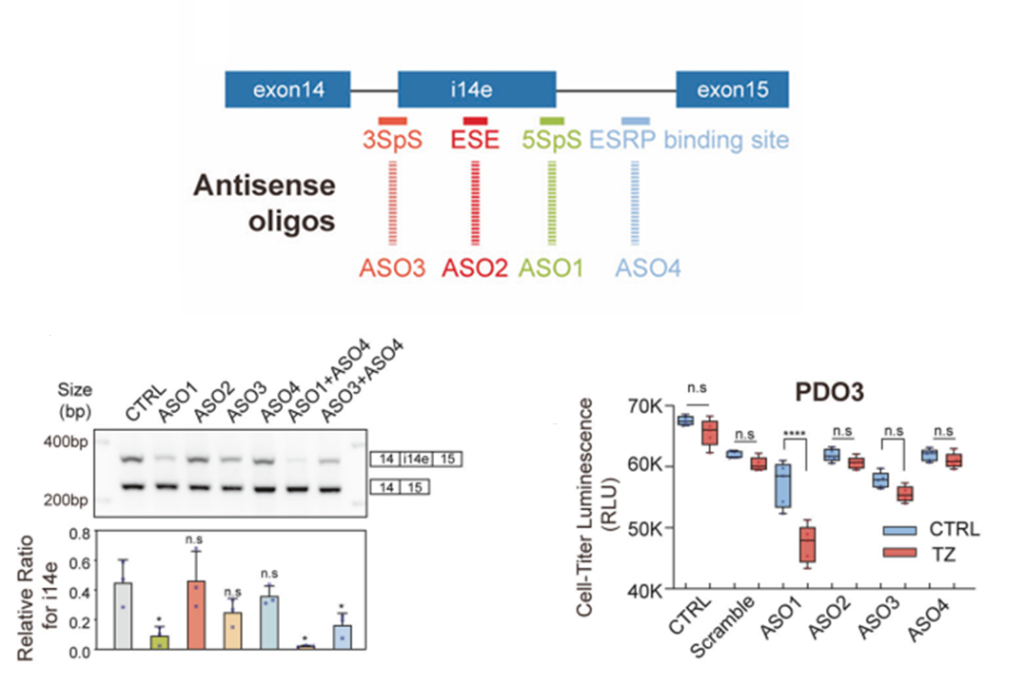
图6 ASO的设计及对ASO效果检测
参考文献;
Wang Z, Gao L, Jia Z, et al. Full-length transcriptome atlas of gallbladder cancer reveals trastuzumab resistance conferred by ERBB2 alternative splicing. Signal Transduct Target Ther. 2025 Feb 14;10(1):54. doi: 10.1038/s41392-025-02150-w.


