心血管病中的表观遗传学:分子机制与临床治疗进展
- boke
- 2023-04-11
- 7:07 上午
在全世界范围内,心血管疾病已逐渐升至为威胁人类健康的“第一杀手”。心血管疾病的发病率逐年上升,且发病年龄逐渐年轻化。心血管疾病的早期检测和诊断对于改善心血管疾病的治疗和预后至关重要。
表观遗传学修饰在心血管疾病的发生和发展中起着重要作用,它可以作为心血管疾病的生物标志物用于心血管疾病的诊断、治疗反应预测和评估。2022年发表的一篇综述,总结了表观遗传学的研究历史和一般机制、心血管疾病中的表观遗传调节机制以及利用表观遗传学治疗心血管疾病的潜在策略[1]。
英国生物学家C.H.Waddington在1942年首次提出“表观遗传学”一词[5],英国分子生物学家R Holliday在20世纪80年代重新系统地阐述了这个术语[6]。1996年,美国遗传学家Athur D. Riggs等人将表观遗传学定义为有丝分裂或减数分裂在不改变基因序列的情况下对基因功能造成的遗传变化[8,9]。表观遗传学是研究基因DNA序列不变而RNA的表达发生变化的现象。它是可逆的、动态调节的基因表达调控机制,可能在生物学中发挥重要的作用。
表观遗传学调控机制
表观遗传学调控主要有三大类:DNA甲基化、组蛋白修饰和非编码RNA。
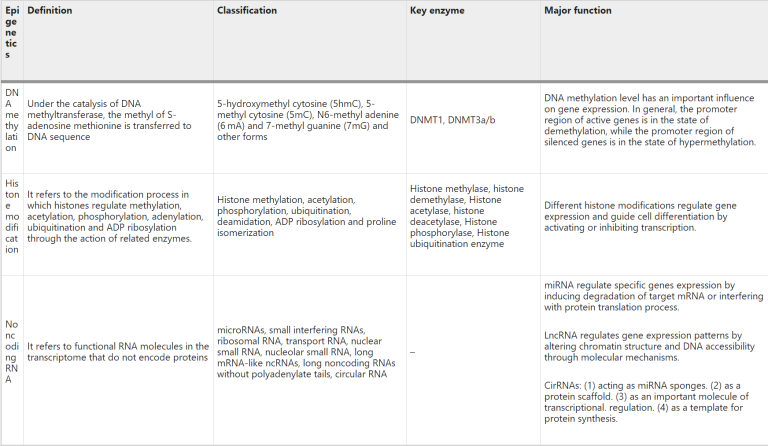
表1 三类表观遗传学调控类型:DNA甲基化、组蛋白修饰和非编码RNA
DNA甲基化是真核细胞中普遍存在的修饰方式,也是哺乳动物基因表达调控的主要表观遗传形式。DNA甲基化通过调节DNA甲基转移酶(DNMT)将遗传信息传递给后代DNA。DNMT根据作用可分为三类:写入酶、擦除酶和读取酶(图1)。写入酶将甲基基团添加到胞嘧啶残基上,擦除酶可以修改和去除甲基基团,而阅读酶则是识别并结合甲基基团以影响基因表达。

图1 DNA甲基化及三类DNMT酶(读取酶、写入酶和擦除酶)的作用
组蛋白修饰可以改变组蛋白和DNA双链之间的亲和力,也可以影响其他转录因子和结构基因启动子之间的亲和力。组蛋白精氨酸甲基化是一个相对动态的标记,它与基因的激活和沉默有关。组蛋白乙酰化发生在H3和H4的N端比较保守的赖氨酸部位。组蛋白乙酰化可以通过其对组蛋白电荷和相互作用的蛋白质的影响来调节基因转录。
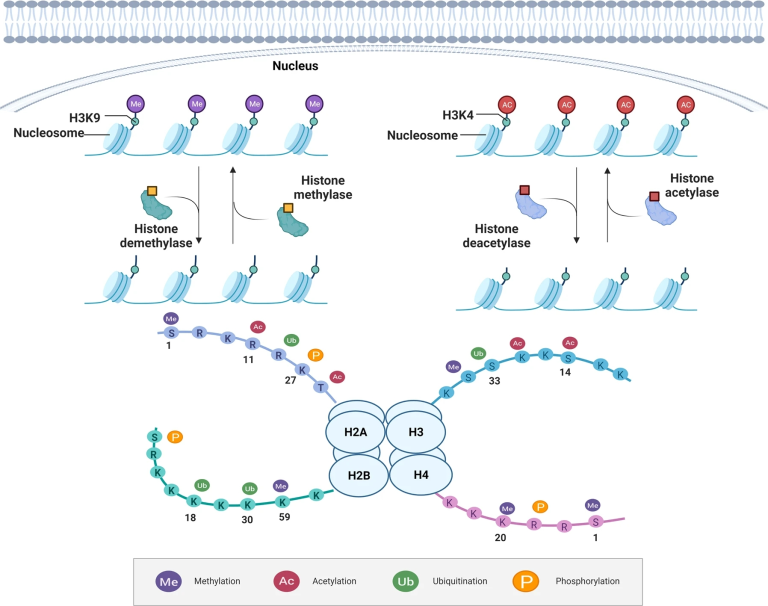
图2 组蛋白修饰包括:甲基化(methylation)、乙酰化(acetylation)、磷酸化(phosphorylation)、腺苷酸化(adenylation)、泛素化(ubiquitination)、二磷酸腺苷核糖化(adenosine diphosphate ribosylation)等组蛋白修饰
非编码RNAs是指不编码蛋白质的RNAs,它们可以从DNA转录而来,但不能翻译成蛋白质,在RNA水平上执行各自的生物学功能(图3)。根据长度,非编码RNA可分为三类:<50 nt:微小RNA(miRNA)、小干扰RNA(siRNA)等。50-500 nt:核糖体RNA(ribosomal RNA)、转运RNA(transport RNA)、核小RNA(nuclear small RNA)、核仁小RNA(nucleolar small RNA)等。>500 nt:长的mRNA样ncRNA、无多聚腺苷酸尾巴的长链非编码RNA(long noncoding RNAs (lncRNAs))等。
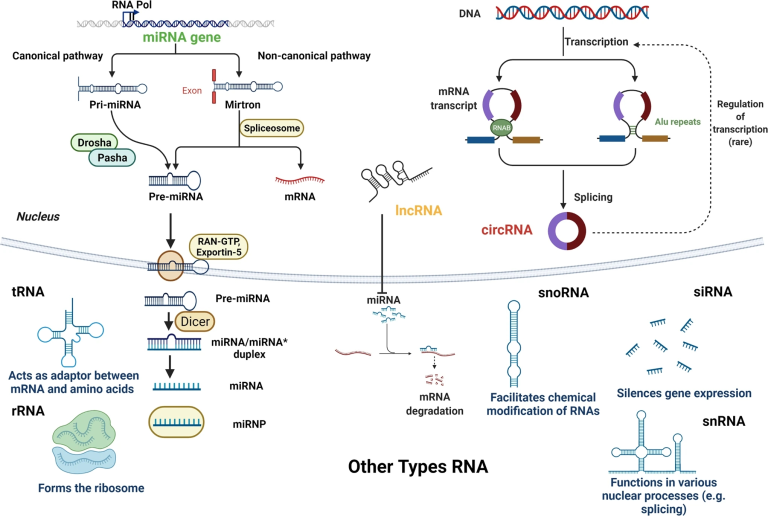
图3 非编码RNA在表观遗传调控中的不同作用机制。(1)<50 nt:miRNAs促进mRNAs沉默或降解,siRNA沉默基因表达;(2)50-500nt:snoRNA修饰rRNA,snRNA与蛋白质因子结合并剪接mRNA,tRNA运输氨基酸合成蛋白质,rRNA与蛋白质结合形成核糖体参与蛋白质合成;(3)>500 nt:lncRNA调节基因表达,cirRNA结合miRNA并解除miRNA的抑制从而提高靶基因的表达水平
心血管病中的表观调控机制
近年来,心血管疾病中的表观遗传学调控机制已经被阐明。表观遗传学与心血管疾病的相关性主要体现在心血管疾病相关酶的功能和表达上(图4)[43-63]。

图4 心血管病中的表观遗传学调控机制重大发现
多项研究表明,DNA甲基化在心血管疾病中起着重要作用(表2)。
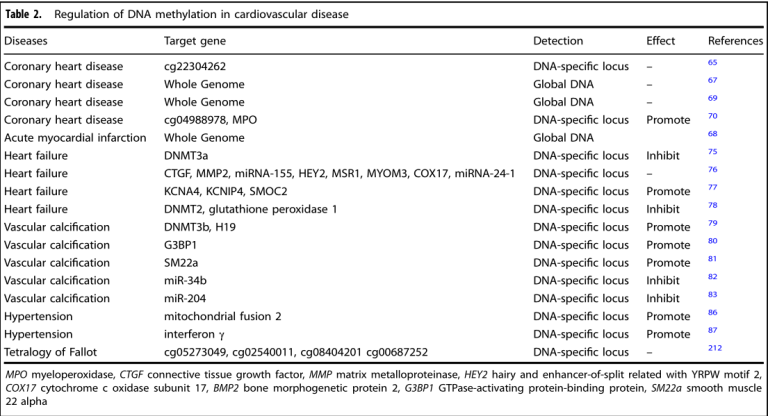
表2 与心血管病相关的DNA甲基化修饰
Westman等人的研究发现基因组三个区域(SLC9A1、SLC1A5和TNRC6C基因区域)的DNA甲基化水平与心血管疾病风险相关。其中SLC1A5的一个CpG位点(CG22304262)甲基化水平可能影响SLC1A5的表达并与冠心病的发病相关。对急性心肌梗死(AMI)模型小鼠的研究发现有5个基因(Ptpn6、Csf1r、Col6a1、Cyba和Map3k14)通过调节DNA甲基化参与急性心肌梗死的过程。
DNA甲基化的队列研究发现3个基因(CDC42BPB、MAN2A2和RPTOR)与心肌梗死因子相关。在全基因组关联分析中,人们发现了34个与急性心肌梗死相关的新的DNA甲基化位点,其中4个位点(Cg21566642位于基因间区;cg05575921、cg04988978和cg25769469分别调控AHRR、MPO和PTCD2)与冠心病有关。
最近的研究表明,DNA甲基化参与了心脏肥大和心力衰竭,调控异常的DNA甲基化对于进一步了解心力衰竭的发病机制具有重要意义。在一个研究心力衰竭的队列中,Glezeva等人76发现195个DNA甲基化区域的基因表达有变化,在心力衰竭患者的室间隔组织中,有5个基因的甲基化程度偏高。
血管钙化的特点是S-腺苷高半胱氨酸(SAH)水平的增加,H19基因启动子的低甲基化,以及Runx2依赖的血管平滑肌细胞成骨分化的激活。一些与DNA甲基化的分子有可能成为诊断血管钙化的生物标志物。高磷酸盐增加了平滑肌22a(SM22a)启动子区域的DNMTs活性,导致SM22a启动子甲基化,从而降低SM22a基因表达活性,促进成骨细胞转录因子核心结合因子1表达和ALP活性上调,最终导致血管钙化。
DNA甲基化在高血压的发生发展中起着重要作用。一项探索DNA甲基化与24小时血压表型之间关系的研究发现,在1,549,368个CpG位点中有72个DNA甲基化区域与24小时血压表型(24小时平均值)显著相关。
组蛋白甲基化修饰可以调节心血管疾病,组蛋白甲基转移酶G9a与PRC2的催化亚单位EZH2对基因沉默有协同作用。G9a可能是未来治疗早期心肌肥大的潜在目标。IL-6/SIL-6R诱导p-STAT3激活和含Jumonji结构域(JMJD)的蛋白招募,进而增加Runx2基因表达,增强成骨细胞分化和血管钙化。
研究发现,SIRT1通过调节内皮一氧化氮合酶(eNOS)的激活来抑制动脉粥样硬化,SIRT2在肾脏缺血-再灌注损伤和心肌梗死中促进细胞凋亡。HDAC3介导的eNOS K610的去乙酰化促进动脉粥样硬化。
血管钙化可由组蛋白乙酰化诱导,SIRT6、HDAC4和HDAC9可能参与这一过程。SIRT1也可以通过下调Runx2和骨钙素的表达来抑制血管钙化,并可能成为其临床预防和治疗的新的干预目标和策略。
研究表明,组蛋白乙酰化与高血压的发生和发展密切相关。一些研究还表明,HDACs、SIRT1、SIRT3和含溴域蛋白4(BRD4)蛋白表达水平的变化与细胞增殖、炎症和病理性血管重塑有关,从而调节高血压和肺动脉高压的病理过程。

表3 各类心血管病中的组蛋白修饰
非编码RNAs在心血管疾病中起着关键的调节作用。这些非编码RNA可以在人类血液、尿液和其他体液中检测到,可以作为生物标记物用于疾病的早期诊断和预防。
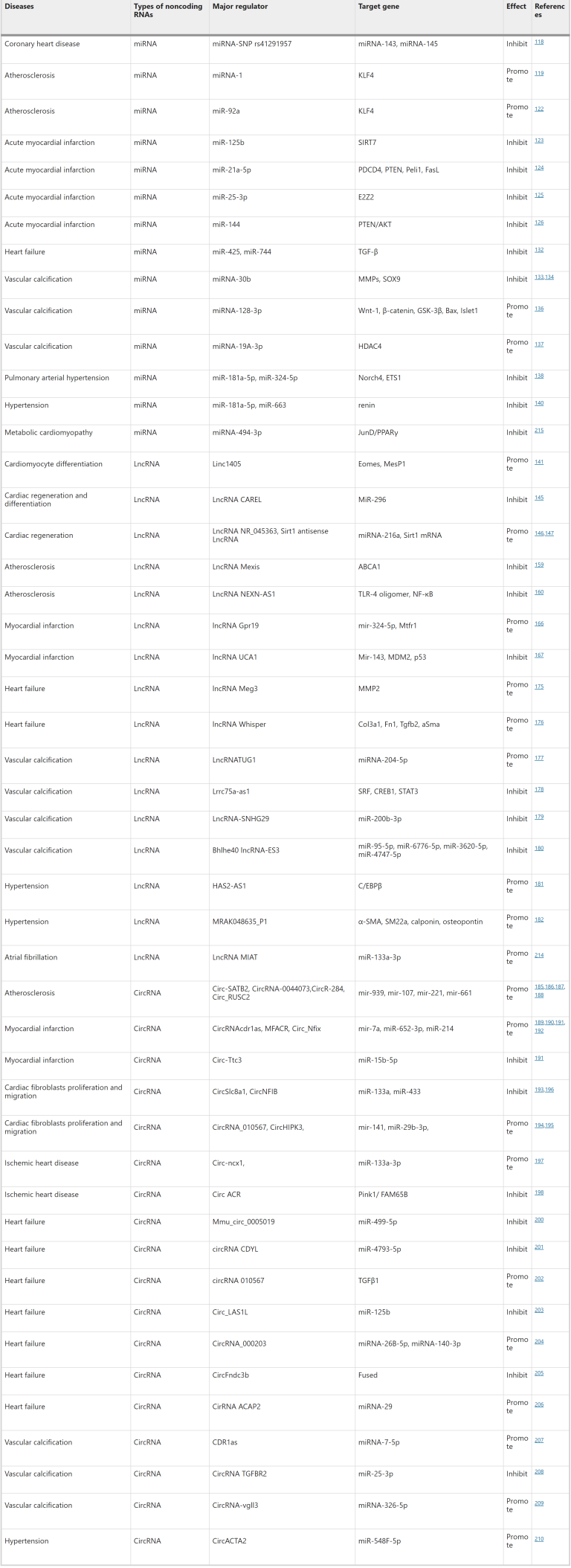
表4 心血管病相关的各类非编码RNA
miRNAs
miRNAs的过度表达可以引起冠心病和急性冠状动脉综合征。一些研究表明,miRNAs可用于预测冠心病和急性冠状动脉综合征的发展并用于治疗冠心病和急性冠状动脉综合征。
最近的研究表明,外泌体miRNAs在心力衰竭中发挥着重要作用。这些miRNAs可以作为射血分数降低的心力衰竭的生物标志物并作为逆转心脏重塑的治疗靶标。
血管钙化与miRNA也密切相关,miRNA-30b可以通过抑制mTOR信号通路,维持线粒体的平衡,防止血管钙化,并通过靶向抑制SOX9,减少骨形态发生蛋白2(BMP2)的激活,防止成骨细胞分化,防止血管钙化。
高血压是由几个基因的表达不平衡引起的,而miRNA可以调节这些基因以防止高血压的发生。
LncRNA
LncRNA在心血管疾病的发生过程中是一把双刃剑,既有积极的一面,又有消极的一面。它们作为诊断标志物也很有用,lncRNA SENCR在诊断早发冠心病(CAD)方面有一定的价值。
LncRNAs通过调节炎症反应、血管内皮细胞的凋亡和自噬、泡沫细胞的形成、脂质代谢和其他机制在动脉粥样硬化中起着关键作用。LncRNAs也可作为动脉粥样硬化的生物标志物,并可能在未来作为动脉粥样硬化疾病的潜在治疗目标。
LncRNAs是心肌梗死的早期指标,并通过控制自噬、细胞凋亡和其他过程在心肌梗死的发病机制中起着关键作用。它们是心肌梗塞的潜在治疗靶标。
近年来,越来越多的证据表明lncRNA在心力衰竭进展中的作用。lncRNA LIPCAR、COL1A1和H19可被视为预测和评估心力衰竭风险的生物标志物,而lncRNA Meg3在心脏重塑后期下调。
LncRNA在血管钙化的发展中具有极其重要的意义。LncRNATUG1上调成骨细胞特异性蛋白,促进钙化性主动脉瓣病成骨细胞分化,LncRNATUG1可作为钙化性主动脉瓣病发病机制中成骨分化的正向调节因子。Huang等人179报道,lncRNA-SNHG29下调miRNA-200b-3p,促进FGFR1和FGF23的表达,抑制成骨因子(Runx2和BMP2),防止VSMC钙化。180 Bhlhe40过表达抑制lncRNA-ES3表达,降低ALP活性和骨钙素的分泌。
LncRNAs被认为与高血压的发展有关。MRAK048635_P1的下调可作为高血压患者血管重塑的一个重要因素。
CircRNAs
冠心病和心肌梗死密切相关。CircRNAs调节几个关键途径,包括血管平滑肌细胞增殖和迁移、心脏再生修复和凋亡以及Gsk3b信号途径,这些途径在心脏功能障碍的发生过程中非常重要。
CirRNAs调节参与心肌细胞肥大、纤维化、自噬和凋亡的基因的表达,这些基因参与了心力衰竭的发展。CirRNAs可作为关键的调节因素,改善心肌梗塞的预后,延缓心衰的发展。
血管钙化和高血压存在关联。CDR1as是一种cirRNA,可加速HPASMC成骨细胞的分化和钙化。CircRNAs有望成为血管钙化和高血压的诊断生物标志物。CircRNA-vgll3的过表达可以靶向减弱miRNA-326-5p的抑制作用并增强脂肪源间充质干细胞的成骨分化。